
【题目】亚磷酸![]() 是二元酸,
是二元酸,![]() 溶液存在电离平衡:
溶液存在电离平衡:![]() 亚磷酸与足量NaOH溶液反应,生成
亚磷酸与足量NaOH溶液反应,生成![]() .
.

![]() 写出亚磷酸与少量NaOH溶液反应的离子方程式 _______________;
写出亚磷酸与少量NaOH溶液反应的离子方程式 _______________;
![]() 某温度下,
某温度下,![]() 的
的![]() 溶液pH的读数为
溶液pH的读数为![]() ,即此时溶液中
,即此时溶液中![]() ,除
,除![]() 之外其他离子的浓度由小到大的顺序是 _____________,该温度下
之外其他离子的浓度由小到大的顺序是 _____________,该温度下![]() 电离平衡的平衡常数
电离平衡的平衡常数![]() ___________。
___________。![]() 第二步电离忽略不计,结果保留两位有效数字
第二步电离忽略不计,结果保留两位有效数字![]()
![]() 向
向![]() 溶液中滴加NaOH溶液至中性,所得溶液中
溶液中滴加NaOH溶液至中性,所得溶液中![]() ___________
___________ ![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() .
.
![]() 亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式 _____________;
亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式 _____________;
![]() 电解
电解![]() 溶液也可得到亚磷酸,装置示意图如图:说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
溶液也可得到亚磷酸,装置示意图如图:说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
![]() 阴极的电极反应式为 ________________;
阴极的电极反应式为 ________________;
![]() 产品室中反应的离子方程式为 ______________。
产品室中反应的离子方程式为 ______________。
【答案】![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
(1)根据酸碱中和反应的关系书写反应方程式;根据弱电解质电离的特点分析各离子浓度的大小;计算电离平衡常数;(2)根据亚磷酸具有强还原性书写与碘反应的化学反应方程式;(3)根据电解![]() 溶液可得到亚磷酸书写电极反应方程式;
溶液可得到亚磷酸书写电极反应方程式;
![]() 亚磷酸是二元酸,亚磷酸和少量氢氧化钠反应生成
亚磷酸是二元酸,亚磷酸和少量氢氧化钠反应生成![]() 、
、![]() ,所以该反应方程式为:
,所以该反应方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
![]() 的
的![]() 溶液pH的读数为
溶液pH的读数为![]() ,氢离子浓度小于亚磷酸浓度,所以亚磷酸是二元弱酸,在水中分步电离,且第一步电离程度大于第二步,两步电离中都有氢离子生成,所以氢离子浓度最大,离子浓度大小顺序是
,氢离子浓度小于亚磷酸浓度,所以亚磷酸是二元弱酸,在水中分步电离,且第一步电离程度大于第二步,两步电离中都有氢离子生成,所以氢离子浓度最大,离子浓度大小顺序是![]() ,
,
![]()
![]()
![]()
起始时各物质浓度![]()
![]() 0 0
0 0
反应的各物质的浓度![]()
![]()
![]()
平衡时各物质的浓度![]()
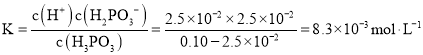
故答案为:![]() ,
,![]() ;
;
![]() 溶液呈中性,则
溶液呈中性,则![]() ,溶液呈电中性,则
,溶液呈电中性,则![]() ,所以
,所以![]() ,故答案为:
,故答案为:![]() ;
;
![]() 碘具有强氧化性,亚磷酸具有强还原性,所以亚磷酸和碘能发生氧化还原反应生成氢碘酸和磷酸,反应方程式为:
碘具有强氧化性,亚磷酸具有强还原性,所以亚磷酸和碘能发生氧化还原反应生成氢碘酸和磷酸,反应方程式为:
![]() ,故答案为:
,故答案为:![]() ;
;
![]() 阴极上氢离子得电子发生还原反应,电极反应式为
阴极上氢离子得电子发生还原反应,电极反应式为![]() ,故答案为:
,故答案为:![]() ;
;
![]() 产品室中
产品室中![]() 和氢离子结合生成亚磷酸,反应离子方程式为:
和氢离子结合生成亚磷酸,反应离子方程式为:![]() ,故答案为:
,故答案为:![]() 。
。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列与盐的水解有关的是
① ![]() 与
与 ![]() 溶液可作焊接金属中的除锈剂 ②用
溶液可作焊接金属中的除锈剂 ②用 ![]() 与
与 ![]() 两种溶液可作泡沫灭火剂 ③草木灰与铵态氮肥不能混合施用 ④实验室盛放
两种溶液可作泡沫灭火剂 ③草木灰与铵态氮肥不能混合施用 ④实验室盛放 ![]() 溶液的试剂瓶不能用磨口玻璃塞
溶液的试剂瓶不能用磨口玻璃塞
A.①②③B.②③④C.①④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,再让乙烯与溴水反应。请回答下列问题:
(1)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生了加成反应,其理由是________(填序号)。
①使溴水褪色的反应不一定是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质不一定是乙烯
④使溴水褪色的物质就是乙烯
(2)乙同学推测此乙烯中一定含有的一种杂质气体是________,它与溴水反应的化学方程式是________________。在实验前必须全部除去,除去该杂质的试剂可用________。
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用![]() 试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________。
试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还含有SiO2(不溶于水和酸)、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
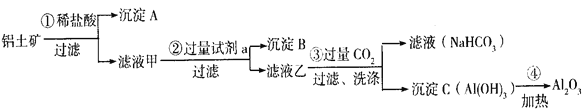
(1)沉淀A、B的成分分别是__________、__________;步骤②中的试剂a是__________;(以上均填化学式)
(2)试写出步骤③中发生反应的离子方式__________、__________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | -33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)戊装置中冷凝管的进水口为___________(填“a”或“b”)。
(2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为________________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到___________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;②_______________________________。
(4)如果缺少乙装置,可能产生的后果是___________________;己装置的作用是__________________。
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________(填标号)。
a.FeCl3溶液(滴有KSCN) b.H2O2溶液 C.溴水 d.AgNO3溶液
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38 gSnCl4,则SnCl4的产率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下面实验装置设计实验制备SO2并进行相关探究活动。
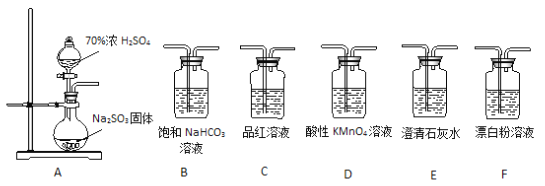
(1)装置A中反应的化学方程式为________________________。
(2)甲同学认为利用上述装置也可证明亚硫酸酸性强于次氯酸,请写出正确的装置连接顺序:A→_________→_________→C→F。
(3)乙同学从上面装置中选择合适的装置验证亚硫酸与碳酸的酸性强弱,其中用到C、D装置。则C装置的作用是________________________,通过______________________现象即可证明亚硫酸酸性强于碳酸。
(4)丙同学将A中产生的足量的SO2通入下图装置G中,G中有白色沉淀生成。该沉淀的化学式为_________。
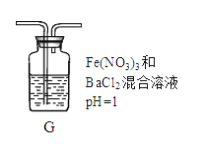
推测产生沉淀的原因可能是(不考虑空气的影响)
原因一:SO2在酸性条件下被NO3―氧化;
原因二:SO2被Fe3+氧化;
原因三:__________________。
若是原因二,需证明Fe3+的还原产物,其实验操作及现象是________________________。
(5)实验中发现Na2SO3可能部分变质,现需测定Na2SO3的纯度,称15.0 g Na2SO3样品,配成250 mL溶液,取25.00 mL溶液,用0.20 mol·L―1酸性KMnO4溶液进行滴定,达到滴定终点时消耗KMnO4溶液20.00 mL。达到滴定终点时锥形瓶中溶液颜色变化是______________,样品中Na2SO3质量分数是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、人类生产、社会可持续发展密切相关,下列说法正确的是( )
A.合成材料、光伏材料和复合材料都是新型无机非金属材料
B.晋代![]() 抱扑子
抱扑子![]() 中记载有“丹砂烧之成水银,积变又还成丹砂”是指加热时丹砂
中记载有“丹砂烧之成水银,积变又还成丹砂”是指加热时丹砂![]() 熔融成液态,遇冷又重新凝结成HgS晶体
熔融成液态,遇冷又重新凝结成HgS晶体
C.煤的干馏是化学变化,煤的气化、液化和石油的分馏都是物理变化
D.![]() 本草经集注
本草经集注![]() 中记载了区别硝石
中记载了区别硝石![]() 和朴硝
和朴硝![]() 的方法:“以火烧之,紫青烟起,乃真硝石也”这是运用了“焰色反应”的原理
的方法:“以火烧之,紫青烟起,乃真硝石也”这是运用了“焰色反应”的原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素的单质和化合物很多,利用所学物质结构与性质的知识去认识和理解它们。
(1)溴的核外电子排布式为__。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在。使氢氟酸分子缔合作用力是___。
(3)下列曲线表示卤族元素某种性质随核电荷数递增的变化趋势,正确的是___。

(4)已知高碘酸有两种形式,化学式分别为H5IO6(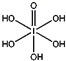 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6___HIO4(填“>”、“<”或“=”)。IO
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6___HIO4(填“>”、“<”或“=”)。IO![]() 的VSEPR模型为__。
的VSEPR模型为__。
(5)铜与氯形成化合物的晶胞如附图所示(黑点代表铜粒子)。

①该晶体的化学式为__。
②一定条件下,Cu2O比CuO更稳定的原因是__。
③已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则该晶体的边长为__pm。(用含ρ、NA的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5 表示。有关说法正确的是

A. 该装置为原电池,b为原电池的负极
B. 中间室Na+移向右室,Cl-移向左室,a极区溶液的pH减小
C. 当左室有4.48L(标准状况下)CO2生成时,右室产生的N2为0.8mol
D. b电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com