
【题目】为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,再让乙烯与溴水反应。请回答下列问题:
(1)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生了加成反应,其理由是________(填序号)。
①使溴水褪色的反应不一定是加成反应
②使溴水褪色的反应就是加成反应
③使溴水褪色的物质不一定是乙烯
④使溴水褪色的物质就是乙烯
(2)乙同学推测此乙烯中一定含有的一种杂质气体是________,它与溴水反应的化学方程式是________________。在实验前必须全部除去,除去该杂质的试剂可用________。
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用![]() 试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________。
试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________。
【答案】不能 ①③ ![]()
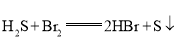
![]() 溶液(答案合理即可) 若乙烯与
溶液(答案合理即可) 若乙烯与![]() 发生取代反应,必定生成
发生取代反应,必定生成![]() ,溶液的酸性会明显增强,若乙烯与
,溶液的酸性会明显增强,若乙烯与![]() 发生加成反应,则生成
发生加成反应,则生成![]() ,溶液的酸性变化不大,故可用
,溶液的酸性变化不大,故可用![]() 试纸予以验证
试纸予以验证
【解析】
根据乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,该淡黄色的浑浊物质应该是具有还原性的硫化氢与溴水发生氧化还原反应生成的硫单质,反应方程式为![]() ,据此分析解答。
,据此分析解答。
(1)根据乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,则可能是该还原性气体与溴水发生氧化还原反应,使溴水褪色,则溴水褪色不能证明是乙烯与溴水发生了加成反应,所以①③正确,故答案为:不能;①③;
(2)淡黄色的浑浊物质是具有还原性的硫化氢与溴水发生氧化还原反应生成的硫单质,反应方程式为![]() ;选用的除杂试剂能够除去硫化氢气体,但是不能与乙烯反应,也不能引入新的气体杂质,根据除杂原则,可以选用
;选用的除杂试剂能够除去硫化氢气体,但是不能与乙烯反应,也不能引入新的气体杂质,根据除杂原则,可以选用![]() 溶液,故答案为:
溶液,故答案为:![]() ;
;![]() ;
;![]() 溶液(答案合理即可);
溶液(答案合理即可);
(3)若乙烯与![]() 发生取代反应,必定生成
发生取代反应,必定生成![]() ,溶液的酸性会明显增强,若乙烯与
,溶液的酸性会明显增强,若乙烯与![]() 发生加成反应,则生成
发生加成反应,则生成![]() ,溶液的酸性变化不大,故可用
,溶液的酸性变化不大,故可用![]() 试纸予以验证,故答案为:若乙烯与
试纸予以验证,故答案为:若乙烯与![]() 发生取代反应,必定生成
发生取代反应,必定生成![]() ,溶液的酸性会明显增强,若乙烯与
,溶液的酸性会明显增强,若乙烯与![]() 发生加成反应,则生成
发生加成反应,则生成![]() ,溶液的酸性变化不大,故可用
,溶液的酸性变化不大,故可用![]() 试纸予以验证。
试纸予以验证。


科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.1 mol·L1的HA溶液中逐滴加入0.1mol·L1的NaOH溶液,溶液中水所电离的c水(H+)随加入NaOH溶液体积的变化如图所示,下列说法正确的是
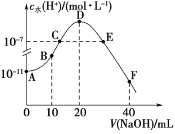
A.HA的电离常数Ka约为1×105
B.B点的溶液中粒子浓度满足关系:c(HA)>c(Na+)>c(A)
C.C、E两点因为对水的电离的抑制作用和促进作用相同,所以溶液均呈中性
D.F点的溶液呈碱性,粒子浓度满足关系c(OH)=c(HA)+c(A)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用以下流程从铜沉淀渣中回收铜、硒、碲等物质。某铜沉淀渣,其主要成分如表。沉淀渣中除含有铜![]() 、硒
、硒![]() 、碲
、碲![]() 外,还含有少量稀贵金属,主要物质为Cu、
外,还含有少量稀贵金属,主要物质为Cu、![]() 和
和![]() 。某铜沉淀渣的主要元素质量分数如下:
。某铜沉淀渣的主要元素质量分数如下:
Au | Ag | Pt | Cu | Se | Te | |
质量分数 |
|
|
|
|
|
|
![]() 、
、![]() 、
、![]() 为同主族元素,其中
为同主族元素,其中![]() 在元素周期表中的位置_________。其中铜、硒、碲的主要回收流程如下:
在元素周期表中的位置_________。其中铜、硒、碲的主要回收流程如下:
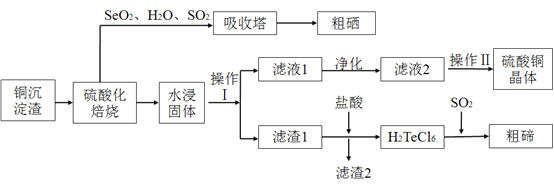
![]() 经过硫酸化焙烧,铜、硒化铜和碲化铜转变为硫酸铜。其中碲化铜硫酸化焙烧的化学方程式如下,填入合适的物质或系数:
经过硫酸化焙烧,铜、硒化铜和碲化铜转变为硫酸铜。其中碲化铜硫酸化焙烧的化学方程式如下,填入合适的物质或系数:![]() ____
____![]()
![]()
![]() ____
____![]() ____
____![]() ____
____![]()
![]() 与吸收塔中的
与吸收塔中的![]() 反应生成亚硒酸。焙烧产生的
反应生成亚硒酸。焙烧产生的![]() 气体进入吸收塔后,将亚硒酸还原成粗硒,其反应的化学方程式为____________ ;
气体进入吸收塔后,将亚硒酸还原成粗硒,其反应的化学方程式为____________ ;
![]() 沉淀渣经焙烧后,其中的铜转变为硫酸铜,经过系列反应可以得到硫酸铜晶体。滤液2经过_____ 、过滤、洗涤、干燥可以得到硫酸铜晶体。
沉淀渣经焙烧后,其中的铜转变为硫酸铜,经过系列反应可以得到硫酸铜晶体。滤液2经过_____ 、过滤、洗涤、干燥可以得到硫酸铜晶体。
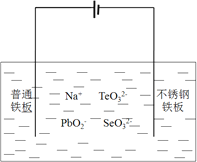
![]() 目前碲化镉薄膜太阳能行业发展迅速,被认为是最有发展前景的太阳能技术之一。用如下装置可以完成碲的电解精炼。研究发现在低的电流密度、碱性条件下,随着
目前碲化镉薄膜太阳能行业发展迅速,被认为是最有发展前景的太阳能技术之一。用如下装置可以完成碲的电解精炼。研究发现在低的电流密度、碱性条件下,随着![]() 浓度的增加,促进了Te的沉积。写出Te的沉积的电极反应式为__________。
浓度的增加,促进了Te的沉积。写出Te的沉积的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
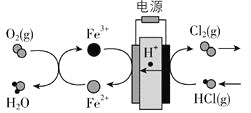
负极区发生的反应有_________![]() 写反应方程式
写反应方程式![]() 。电路中转移
。电路中转移![]() 电子,需消耗氧气__________
电子,需消耗氧气__________![]() 标准状况
标准状况![]() 。
。
![]() 电解法转化
电解法转化![]() 可实现
可实现![]() 资源化利用。电解
资源化利用。电解![]() 制HCOOH的原理示意图如下。
制HCOOH的原理示意图如下。

![]() 写出阴极
写出阴极![]() 还原为
还原为![]() 的电极反应式:________。
的电极反应式:________。
![]() 电解一段时间后,阳极区的
电解一段时间后,阳极区的![]() 溶液浓度降低,其原因是_____。
溶液浓度降低,其原因是_____。
![]() 可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接
可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接![]() 或
或![]() ,可交替得到
,可交替得到![]() 和
和![]() 。
。
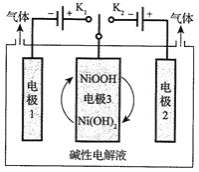
![]() 制
制![]() 时,连接_______________。产生
时,连接_______________。产生![]() 的电极反应式是_________。
的电极反应式是_________。
![]() 改变开关连接方式,可得
改变开关连接方式,可得![]() 。
。
![]() 结合
结合![]() 和
和![]() 中电极3的电极反应式,说明电极3的作用:___________。
中电极3的电极反应式,说明电极3的作用:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体 X 和气体 Y 各 0.16mol 充入 ![]() 恒容密闭容器中,发生反应:
恒容密闭容器中,发生反应:![]()
![]() ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前 ![]() 的平均速率
的平均速率 ![]()
B.该温度下此反应的平衡常数 ![]()
C.其他条件不变,再充入 ![]() Z ,平衡时 X 的体积分数不变
Z ,平衡时 X 的体积分数不变
D.其他条件不变,降低温度,反应达到新平衡前 v(逆)> v(正)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
![]() 已知:
已知:![]() ,则反应
,则反应![]() ______ 。
______ 。
![]() 天然气的一个重要用途是制取
天然气的一个重要用途是制取![]() ,其原理为:
,其原理为:![]() 。一定条件下,在密闭容器中,通入物质的量浓度均为
。一定条件下,在密闭容器中,通入物质的量浓度均为![]() 的
的![]() 与
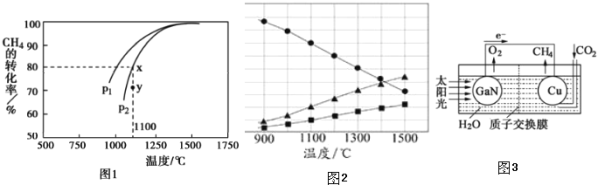
与![]() ,在发生反应时,测得
,在发生反应时,测得![]() 的平衡转化率与温度及压强的关系如图1所示,
的平衡转化率与温度及压强的关系如图1所示,
![]() 该反应的平衡常数表达式为______ 。
该反应的平衡常数表达式为______ 。
![]() 压强
压强![]() ______
______ ![]() 填“大于”或“小于”
填“大于”或“小于”![]() ;压强为
;压强为![]() 时,在Y点:
时,在Y点:![]() 正
正![]() ______
______ ![]() 逆
逆![]() 填“大于“、“小于”或“等于“
填“大于“、“小于”或“等于“![]() 。
。
![]() 天然气中的少量
天然气中的少量![]() 杂质常用氨水吸收,产物为
杂质常用氨水吸收,产物为![]() 。一定条件下向
。一定条件下向![]() 溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为______ 。
溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为______ 。
![]() 工业上又常将从天然气分离出的
工业上又常将从天然气分离出的![]() ,在高温下分解生成硫蒸气和
,在高温下分解生成硫蒸气和![]() ,若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示,
,若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图2所示,![]() 在高温下分解反应的化学方程式为______ 。
在高温下分解反应的化学方程式为______ 。
![]() 科学家用氮化镓材料与铜组装如图3的人工光合系统,利用该装置成功地实现了以
科学家用氮化镓材料与铜组装如图3的人工光合系统,利用该装置成功地实现了以![]() 和
和![]() 合成
合成![]() 。
。
![]() 写出铜电极表面的电极反应式为______ 。
写出铜电极表面的电极反应式为______ 。
![]() 为提高该人工光合系统的工作效率,可向装置中加入少量______
为提高该人工光合系统的工作效率,可向装置中加入少量______ ![]() 选填“盐酸”或“硫酸”
选填“盐酸”或“硫酸”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】洗煤和选煤过程中排出的煤矸石(主要含Al2O3、SiO2及Fe2O3)会占用大片土地,造成环境污染。某课题组利用煤矸石制备聚合氯化铝流程如下:
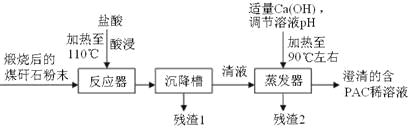
已知:聚合氯化铝([Al2(OH)nCl6-n]m(1≤n≤5,m≤10),商业代号PAC)是一种新型、高效絮凝剂和净水剂。
(1)酸浸的目的是___________________________;实验需要的500mL3.0 mol·L-1的盐酸,配制时所需要的玻璃仪器除量筒、烧杯、玻璃棒外还有______________________。
(2)若m=n=2,则生成PAC的化学方程式是_____________________。
(3)从含PAC的稀溶液中获得PAC固体的实验操作方法是_______、_________、_________。
(4)为了分析残渣2中铁元素的含量,某同学称取5.000g残渣2,先将其预处理使铁元素还原为Fe2+,并在容量瓶中配制成100mL溶液;然后移取25.00mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定,消耗标准溶液20.00mL。已知反应式为Fe2++MnO4-+H+—Fe3++Mn2++H2O(未配平)。判断滴定终点的依据是_______________________;残渣2中铁元素的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚磷酸![]() 是二元酸,
是二元酸,![]() 溶液存在电离平衡:
溶液存在电离平衡:![]() 亚磷酸与足量NaOH溶液反应,生成
亚磷酸与足量NaOH溶液反应,生成![]() .
.

![]() 写出亚磷酸与少量NaOH溶液反应的离子方程式 _______________;
写出亚磷酸与少量NaOH溶液反应的离子方程式 _______________;
![]() 某温度下,
某温度下,![]() 的
的![]() 溶液pH的读数为
溶液pH的读数为![]() ,即此时溶液中
,即此时溶液中![]() ,除
,除![]() 之外其他离子的浓度由小到大的顺序是 _____________,该温度下
之外其他离子的浓度由小到大的顺序是 _____________,该温度下![]() 电离平衡的平衡常数
电离平衡的平衡常数![]() ___________。
___________。![]() 第二步电离忽略不计,结果保留两位有效数字
第二步电离忽略不计,结果保留两位有效数字![]()
![]() 向
向![]() 溶液中滴加NaOH溶液至中性,所得溶液中
溶液中滴加NaOH溶液至中性,所得溶液中![]() ___________
___________ ![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() .
.
![]() 亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式 _____________;
亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式 _____________;
![]() 电解
电解![]() 溶液也可得到亚磷酸,装置示意图如图:说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
溶液也可得到亚磷酸,装置示意图如图:说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
![]() 阴极的电极反应式为 ________________;
阴极的电极反应式为 ________________;
![]() 产品室中反应的离子方程式为 ______________。
产品室中反应的离子方程式为 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示有关物质检验的实验结论正确的是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀产生 | 该溶液中一定含有SO42- |
B | 向某溶液中加入盐酸,将生成的气体通入品红溶液中,品红溶液褪色 | 该溶液一定含有 SO32- |
C | 将某气体通入品红溶液中,品红溶液褪色 | 说明酸性:H2SO3>H2CO3 |
D | 某气体先通入足量的酸性 KMnO4 溶液,再通入澄清石灰水中有浑浊 | 该气体一定是 CO2 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com