
【题目】A、B、C、D是原子序数依次递增的前四周期元素,A元素的正化合价与负化合价的代数和为零;B元素原子的价电子结构为nsnnpn;C元素基态原子s能级的电子总数比p能级的电子总数多1;D元素原子的M能层全满,最外层只有一个电子。请回答:
(1)A元素的单质为A2,不能形成A3或A4,这体现了共价键的___性;B元素单质的一种空间网状结构的晶体熔点>3550℃,该单质的晶体类型属于________;基态D原子共有___种不同运动状态的电子。
(2)A与C形成的最简单分子的中心原子杂化方式是___________,该分子与D2+、H2O以2:1:2的配比结合形成的配离子是_________(填化学式),此配离子中的两种配体的不同之处为_____(填标号)。
①中心原子的价层电子对数 ②中心原子的孤电子对的对数 ③中心原子的化学键类型 ④VSEPR模型
(3)1molBC—中含有的π键数目为______;写出与BC-互为等电子体的分子和离子各一种______、______。
(4)D2+的硫酸盐晶体的熔点比D2+的硝酸盐晶体的熔点高,其原因是______。
(5)D3C具有良好的电学和光学性能,其晶体的晶胞结构如图所示,D+和C3—半径分别为apm、bpm,D+和C3—都是紧密接触的刚性小球,则C3—的配位数为_____,晶体的密度为____g·cm-3。

【答案】 饱和 原子晶体或共价晶体 29 sp3 [Cu(H2O)2(NH3)2]2+ ② 2NA CO或N2 C22- 硫酸铜的晶格能比硝酸制的晶格能高 6 (103×1030)/(4NA (a+b)3)或(206×1030)/(8NA (a+b)3)
【解析】试题分析: B元素原子的价电子结构为nsnnpn,n=2,B是C元素;A的原子序数小于B,A元素的正化合价与负化合价的代数和为零,A是H元素;C元素基态原子s能级的电子总数比p能级的电子总数多1,C是N元素;D元素原子的M能层全满,最外层只有一个电子,D是Cu元素。
解析:(1)H元素的单质为H2,不能形成H3或H4,这体现了共价键的饱和性;原子晶体熔点高,C元素单质的一种空间网状结构的晶体熔点>3550℃,该单质的晶体类型属于原子晶体;原子核外有几个电子就有几种运动状态,基态铜原子核外有29个电子,所以有29种不同运动状态的电子。 (2)H与N形成的最简单分子是NH3,N原子的价电子对数是![]() ,所以N原子杂化方式是sp3,NH3与Cu2+、H2O以2:1:2的配比结合形成的配离子是[Cu(H2O)2(NH3)2]2+,[Cu(H2O)2(NH3)2]2+中NH3分子、H2O分子中心原子的价层电子对数都是4,故①相同; NH3分子中心原子的孤电子对的对数是1,H2O分子中心原子的孤电子对的对数是2,故②不同;NH3分子、H2O分子的中心原子的化学键都是共价键,故③相同; ④VSEPR模型都有4个电子对,故④相同; (3) CN-中含有碳氮三键,1molBC-中含有的π键数目为2NA;等电子体是原子数、价电子数相同的分子或离子, 与CN-互为等电子体的分子和离子有CO、 C22-。 (4)离子晶体的熔点与晶格能有关,晶格能越大熔点越高,硫酸铜的晶格能比硝酸铜的晶格能高,硫酸铜的熔点比硝酸铜晶体的熔点高。 (5)根据晶胞图,离N3-最近的Cu+有6个,所以N3-的配位数为6;根据均摊原则,每个晶胞含有Cu+数
,所以N原子杂化方式是sp3,NH3与Cu2+、H2O以2:1:2的配比结合形成的配离子是[Cu(H2O)2(NH3)2]2+,[Cu(H2O)2(NH3)2]2+中NH3分子、H2O分子中心原子的价层电子对数都是4,故①相同; NH3分子中心原子的孤电子对的对数是1,H2O分子中心原子的孤电子对的对数是2,故②不同;NH3分子、H2O分子的中心原子的化学键都是共价键,故③相同; ④VSEPR模型都有4个电子对,故④相同; (3) CN-中含有碳氮三键,1molBC-中含有的π键数目为2NA;等电子体是原子数、价电子数相同的分子或离子, 与CN-互为等电子体的分子和离子有CO、 C22-。 (4)离子晶体的熔点与晶格能有关,晶格能越大熔点越高,硫酸铜的晶格能比硝酸铜的晶格能高,硫酸铜的熔点比硝酸铜晶体的熔点高。 (5)根据晶胞图,离N3-最近的Cu+有6个,所以N3-的配位数为6;根据均摊原则,每个晶胞含有Cu+数![]() ,每个晶胞含有N3-数
,每个晶胞含有N3-数![]() ,所以晶胞的摩尔质量是206g/mol,晶胞的体积是
,所以晶胞的摩尔质量是206g/mol,晶胞的体积是![]() ,晶体的密度为(206×1030)/(8NA (a+b)3)g·cm-3。
,晶体的密度为(206×1030)/(8NA (a+b)3)g·cm-3。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10% NaOH溶液洗;⑤水洗;⑥分液。正确的操作顺序是( )
A.②⑥④⑥⑤⑥③①B.①②⑥③④⑤
C.④⑥②⑥③①⑤D.②⑥④⑥①⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.25℃时在25 mL氢氧化钠溶液中逐滴加入0.2 mol/L醋酸溶液,滴定曲线如下图所示.下列说法正确的是__________________
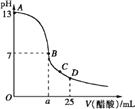
A.滴定终点时俯视读数则测定的氢氧化钠浓度偏高
B.B、C、D三点的溶液中水的电离程度为B>C>D
C.D点,c(CH3COO-)+ c(CH3COOH)>2c(Na+)
D.B点为滴定终点
E.B点时c(CH3COO-)=c(Na+)
F. 若由体积相等的氢氧化钠和醋酸溶液混合而且恰好呈中性,则混合前c(NaOH)< c(CH3COOH)
G.滴定前的氢氧化钠溶液的浓度为0.1mol/L
Ⅱ.(1)为了检验某残留物中铁元素的含量,先将残留物预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,写出滴定过程中反应的离子方程式:________________________________________KMnO4应装在___________滴定管中(填“酸式”或“碱式”)滴定前是否要滴加指示剂?___(填“是”或“否”),滴定终点的判断方法:_____________________________
(2)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜加入______________调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________________。[Fe(OH)3的Ksp=2.6×10-39]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于晶体和非晶体,下列说法中正确的( )
A. 铁是非晶体
B. 晶体和非晶体在熔化过程中温度都上升
C. 晶体熔化时吸热,非晶体熔化时不吸热
D. 晶体有固定熔点,非晶体没有固定熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对伞花烃(图I)常用作染料、医药、香料的中间体。下列说法错误的是
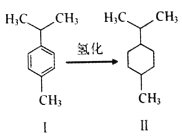
A. 常温对伞花烃呈液态且难溶于水
B. 图Ⅱ物质的一氯代物有5种结构
C. 对伞花烃最多有9个碳原子共平面
D. 图中氢化反应既是加成反应又是还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解法制备硼酸[H3BO3或B(OH) 3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。下列有关说法正确的是( )
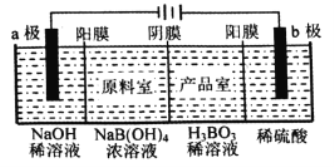
A. 阴极与阳极产生的气体体积比为1:2 B. b极的电极反应式为2H2O-2eˉ=O2↑+4H+
C. 产品室中发生的反应是B(OH)3+OHˉ=B(OH)4ˉ D. 每增加1 mol H3BO3产品,NaOH溶液增重22g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年大部分地区爆发了流感流感常伴随发热高烧等症状。布洛芬是一种常用的儿童退热药,它的BHC合成法如下
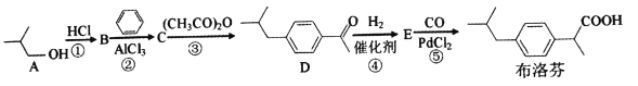
(1)A的名称是__________,B的核磁共振氢谱有__________种吸收峰。
(2)①反应需用浓盐酸而不用稀盐酸,其原因是______________________________。
(3)E的分子式是__________,官能团的名称是__________。
(4)③反应的化学方程式是____________________,反应类型是__________。
(5)满足下列条件的布洛芬的同分异构体有__________种
a遇FeCl3溶液显紫色 b.分子中有5种不同化学环境的氢 c.能发生银镜反应
(6)请写出由苯和( CH3COOCH2CO)2O为原料合成![]() 的线路图(其他试剂任选)___________
的线路图(其他试剂任选)___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:C(s)+CO2(g) ![]() 2CO(g),下列说法不正确的是( )
2CO(g),下列说法不正确的是( )
A. 增大CO2浓度可以加快反应速率
B. 升高温度可以加快反应速率
C. 容器体积不变时,向其中充入N2,反应速率不变
D. 增加碳的质量可以加快反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com