
 CO2在高温高压下所形成的晶体其晶胞如图所示.该晶体的类型属于
CO2在高温高压下所形成的晶体其晶胞如图所示.该晶体的类型属于科目:高中化学 来源: 题型:
 A、B、C、D、E、F均为周期表中前四周期的元素.请按要求回答下列问题.
A、B、C、D、E、F均为周期表中前四周期的元素.请按要求回答下列问题.| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 1 |
| 4 |
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,烧杯内盛有浓HNO3,在烧杯中放入用导线相连的铁、铅两个电极,已知原电池停止工作时,Fe、Pb都有剩余.试依次写出Fe电极上可能发生的电极反应式.
如图所示,烧杯内盛有浓HNO3,在烧杯中放入用导线相连的铁、铅两个电极,已知原电池停止工作时,Fe、Pb都有剩余.试依次写出Fe电极上可能发生的电极反应式.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A、在830℃,等物质的量的CO和H2O反应达到平衡时,CO的转化率为50% |
| B、在500℃时,反应达到平衡后,增大压强,化学平衡常数K减小 |
| C、恒温、恒容条件下,若混合气体的平均相对分子质量一定,不能确定可逆反应是否达到平衡 |
| D、上述正向反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、针对H7N9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、活性银离子、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学核心 |
| B、肌红蛋白、蚕丝、过氧化氢酶、鱼油充分水解后均可得到氨基酸 |
| C、嫦娥三号月球车玉兔号在进入第二个月夜休眠前,出现了机构控制异常情况,其病因或为月尘,即月球上直径小于10微米的浮尘,月尘分散在空气中形成的分散系属于胶体 |
| D、某些铝硅酸盐形成的分子筛中有许多笼状空穴和通道,常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、催化剂及催化剂载体等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol SO2和1 mol O2 在一定条件下反应,反应后分子总数大于2NA |
| B、25℃时,在pH=2的1.0 L H2SO4溶液中含有H+数目为0.01NA |
| C、在二氧化硅的晶体中,1mol SiO2含有Si-O键数目为4NA |
| D、25mL 18 mol?L-1浓硫酸与足量Zn反应,转移电子数为0.225NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
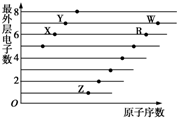
| A、X和R在同一周期 |
| B、原子半径:W>R>X |
| C、气态氢化物的稳定性:Y>X |
| D、X、Z形成的化合物中不可能含有共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com