
 如图所示,烧杯内盛有浓HNO3,在烧杯中放入用导线相连的铁、铅两个电极,已知原电池停止工作时,Fe、Pb都有剩余.试依次写出Fe电极上可能发生的电极反应式.
如图所示,烧杯内盛有浓HNO3,在烧杯中放入用导线相连的铁、铅两个电极,已知原电池停止工作时,Fe、Pb都有剩余.试依次写出Fe电极上可能发生的电极反应式.

科目:高中化学 来源: 题型:
 如图,在半透膜袋里盛有淀粉的氯化钠溶液,将半透膜袋悬挂在蒸馏水中,回答下列问题:(知识支持:淀粉遇碘单质变蓝)
如图,在半透膜袋里盛有淀粉的氯化钠溶液,将半透膜袋悬挂在蒸馏水中,回答下列问题:(知识支持:淀粉遇碘单质变蓝)查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1.恒温条件下,容积为1L的恒容容器中,硫可以发生如下转化,其反应过程和能量关系如图所示.
已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1.恒温条件下,容积为1L的恒容容器中,硫可以发生如下转化,其反应过程和能量关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
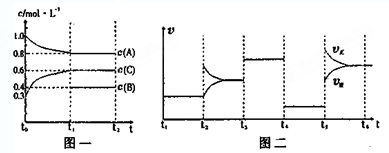
| t1-t2 | t2-t3 | t3-t4 | t4-t5 | t5-t6 |
| K1 | K2 | K3 | K4 | K5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol的2H35Cl分子中的中子数是2NA |
| B、标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA |
| C、铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标准状况下) |
| D、将2.24L(标准状况下)CO2通入1L 0.15 mol?L-1的NaOH溶液中,所得CO2-3和HCO-3物质的量均为0.05N |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c1 |
| c2 |
| A、4 | B、7 | C、10 | D、13 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com