
【题目】甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。甲组同学采用如右图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4 g铜。

(1)仪器a的名称是_______。
(2)在铜与硝酸的反应中,硝酸所表现出的化学性质主要有_______。
(3)仪器c中收集的气体主要是_______。(填分子式)
【答案】分液漏斗 酸性和强氧化性 NO
【解析】
(1)根据装置图可知仪器的名称;
(2)根据反应中N元素的化合价部分未变化生成硝酸铜,部分降低生成氮的氧化物分析;
(3)铜与硝酸反应生成盐为硝酸铜,浓硝酸反应产生气体是NO2,稀硝酸反应产生的气体是NO,NO2可与水反应产生NO气体。
(1)根据装置图可知仪器a的名称是分液漏斗;
(2)在Cu与硝酸的反应中,N元素的化合价部分未变化生成硝酸铜,硝酸表现酸性,部分被还原,降低生成氮的氧化物,硝酸表现强氧化性,因此在铜与硝酸的反应中,硝酸表现酸性和氧化性;
(3)Cu与一定浓度的硝酸反应,若硝酸为浓硝酸,发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;若为稀硝酸,则发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O。反应产生的气体被水吸收时,若其中含有NO2,在集气瓶中就会发生反应:3NO2+H2O =2HNO3+NO,所以最后收集的到的气体是NO。


科目:高中化学 来源: 题型:
【题目】有机物的结构可用键线式简化表示,如CH3-CH=CH-CH3可表示为![]() ,有一种有机物X的键线式如图所示。
,有一种有机物X的键线式如图所示。

(1)X的分子式为_______________________。
(2)有机物Y是X的同分异构体,且属于芳香族化合物。则Y的结构简式是_____________。
(3)Y在一定条件下可发生反应生成高分子化合物,该反应的化学方程式是_________________。
(4)Y可以与溴水反应,该反应的化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往含I一和Cl-的稀溶液中逐滴加入AgNO3溶液,产生沉淀的质量m(沉淀)与加入AgNO3
溶液的体积V( AgN03)的关系如图所示。已知:Ksp(AgCl)=1.8×l0-10, Ksp( AgI) =l.5xl0-16,则原溶液中c(I一)/c(Cl-)的比值为

A. (V2- Vl)/Vl B. Vl/V2 C. Vl/( V2- Vl) D. V2/Vl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
实验目的:探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后褪色的原因。
(分析与猜想)根据过氧化钠与水反应的原理:![]() ,往过氧化钠固体完全溶解反应后的溶液中滴加酚酞本应只会变红而不会褪色,而实验中发现酚酞变红后又褪色。
,往过氧化钠固体完全溶解反应后的溶液中滴加酚酞本应只会变红而不会褪色,而实验中发现酚酞变红后又褪色。
(1)由此提出如下的猜想:
A.氧气有漂白性B B.氢氧化钠有漂白性 C.______
(2)根据以上实验分析发现:过氧化钠与水反应过程中,钠元素形成了稳定的化合物,溶液中还生成了一种不很稳定、具有漂白性的物质![]() ,
,![]() 的化学式是______。
的化学式是______。
(3)可用右图装置对溶液中不很稳定的物质进行探究,在①处装入的物质是______(填选项,下同),②处装入的物质是______。
A.酚酞试剂 B.过氧化钠与水反应后的溶液
C.二氧化锰 D.氢氧化钠固体配制的溶液
(4)气体③是______,过氧化钠与水反应的化学方程式没有写出![]() 来,原因是______。
来,原因是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯MnCO3是广泛用于电子行业的强磁性材料。MnCO3为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于100℃开始分解。
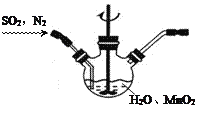
Ⅰ.实验室以MnO2为原料制备MnCO3
(1)制备MnSO4溶液:
①主要反应装置如右图,缓缓通入经N2稀释的SO2气体,发生反应H2SO3+MnO2![]() MnSO4+H2O。下列措施中,目的是加快化学反应速率的是________(填标号)。
MnSO4+H2O。下列措施中,目的是加快化学反应速率的是________(填标号)。
A.MnO2加入前先研磨
B.搅拌
C.提高混合气中N2比例
②已知实验室制取SO2的原理是Na2SO3+2H2SO4(浓) ![]() 2NaHSO4+SO2↑+H2O。选择下图所示部分装置与上图装置相连制备MnSO4溶液,应选择的装置有________(填标号)
2NaHSO4+SO2↑+H2O。选择下图所示部分装置与上图装置相连制备MnSO4溶液,应选择的装置有________(填标号)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
③若用空气代替N2进行实验,会对实验中的SO2利用率_______(选填“增大、无影响、减小”)。
(2)制备MnCO3固体:
实验步骤:①向MnSO4溶液中边搅拌边加入饱和NH4HCO3溶液生成MnCO3沉淀,反应结束后过滤;② ……;③在70-80℃下烘干得到纯净干燥的MnCO3固体。
步骤②需要用到的试剂有________。
Ⅱ.设计实验方案
(3)利用沉淀转化的方法证明KSP(MnCO3) < KSP(NiCO3):________。
(已知NiCO3为难溶于水的浅绿色固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为了探究钠与CO2的反应,利用如图装置进行实验。(已知PdCl2能被CO还原为黑色的Pd)

(1)装置②中用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是_______。
A. H2SO4溶液 B. CCl4 C. 苯 D. 稀硝酸
(2)请将图中各装置按顺序连接(填装置接口字母):c接______,______接____,____接______,____接____。
(3)装置④的作用是__________。
(4)检查完装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到_________时再点燃酒精灯。
(5)若反应过程中CO2足量,钠与CO2充分反应后,生成的固体物质可能有多种情况,该同学提出以下猜想:
①生成的固体物质为Na2CO3
②生成的固体物质为Ns2CO3和C的混合物
③生成的固体物质为Ns2CO3和Na2O的混合物
④生成的固体物质为Ns2O和C的混合物
假如反应过程中有下列两种情况:
I. 观察到装置⑤PdCl2溶液中有黑色沉淀,若装置①中固体成分只有一种,且向固体中加入稀盐酸可产生能使澄清石灰水变浑浊的气体,写出该情况下钠与CO2反应的化学方程式____。
II. 装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入足量的稀盐酸中产生224ml(标准状况)CO2气体,溶液中残留固体的质量为___________。
(6)设计实验方案证明装置①中加入的金属钠部分被氧化____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤并转移
⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为____________________。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、______________。
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为________ g,要完成本实验该同学应称出________ g NaOH。
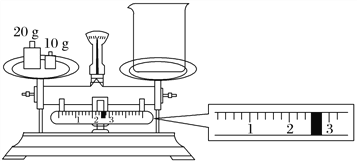
(3)使用容量瓶前必须进行的一步操作是____________________________________________。
(4)在配制过程中,其它操作都是正确的(按烧杯的实际质量),下列操作会引起误差偏低的是________。
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容后塞上瓶塞反复倒转摇匀,静置后,液面低于刻度线,再加水至刻度线
C.称量时药品和砝码位置放反
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32﹣、SO42﹣、Cl﹣中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )

A. 原溶液一定存在CO32﹣和SO42﹣,一定不存在Fe3+
B. 原溶液一定存在Cl﹣,可能存在Na+
C. 原溶液中c(Cl﹣)≥0.1molL﹣1
D. 若原溶液中不存在Na+,则c(Cl﹣)<0.1molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com