
【题目】如图中C%表示某反应物在体系中的百分含量,v表示反应速率,p表示压强,t表示反应时间。图(A)为温度一定时,压强与反应速率的关系曲线;图(B)为压强一定时,在不同时间C%与温度的关系曲线。同时符合以下两个图像的反应是( )
A 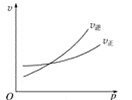 B
B 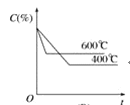
A.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
B.N2O3(g)![]() NO2(g)+NO(g) ΔH>0
NO2(g)+NO(g) ΔH>0
C.3NO2(g)+H2O(l)![]() 2HNO3(l)+NO(g) ΔH<0
2HNO3(l)+NO(g) ΔH<0
D.CO2(g)+C(s)![]() 2CO(g) ΔH>0
2CO(g) ΔH>0
【答案】A
【解析】
由图A可知,到达平衡后,增大压强逆反应速率增大更大,平衡向逆反应移动,说明气体反应物的化学计量数之和小于气体生成物的化学计量数之和,由图B可知,温度越高平衡时反应物的百分含量越高,说明升高温度,平衡向逆反应移动,故正反应为放热反应。
由图(B)可知,温度越高,平衡时反应物的百分含量越高,平衡向逆反应移动,温度升高平衡向吸热的方向移动,逆反应吸热,正反应为放热反应,ΔH<0,故A正确;B、D项错误;
图(A)中正逆反应速率相等时达到平衡,平衡后增大压强,正逆速率都增大,但逆反应速率更大,平衡逆移,增大压强平衡向气体分子数减小的方向移动,逆反应方向应气体分子数减小,C项错误;
故选A。


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】氮气可以作食品包装、灯泡等的填充气。一种实验室制备氮气的方法是:NH4Cl+NaNO2=NaCl+2H2O+N2↑ 。反应发生后即停止加热,反应仍可持续进行,直至反应完全。下列说法正确的是
A.该反应只有在低温下才能自发进行
B.NH4Cl的电子式: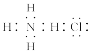
C.元素的电负性:Cl>O>H
D.①和②示意图表示的钠原子,电离出最外层一个电子所需要的能量:①>② ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理电池废料以节约资源、保护环境。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(由Al箔、LiFePO4活性材料、少量不溶于酸碱的导电剂组成)中的资源,部分流程如图:
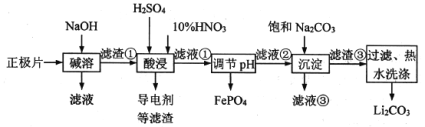
已知:Ksp(Li2CO3)=1.6×10-3。部分物质的溶解度(S)如表所示:
T/℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g | S(LiH2PO4)/g |
20 | 1.33 | 34.2 | 0.039 | 126 |
80 | 0.85 | 30.5 | —— | —— |
(1)将回收的废旧锂离子电池进行预放电、拆分破碎、热处理等预处理,筛分后获得正极片。下列分析你认为合理的是__________。
A.废旧锂离子电池在处理之前需要进行彻底放电,否则在后续处理中,残余的能量会集中释放,可能会造成安全隐患。
B.预放电时电池中的锂离子移向负极,不利于提高正极片中锂元素的回收率。
C.热处理过程可以除去废旧锂离子电池中的难溶有机物、碳粉等。
(2)写出碱溶时主要发生反应的离子方程式:________。
(3)为提高酸浸的浸出率,除粉碎、搅拌、升温外,还可采用的方法有______。(写出一种即可)
(4)酸浸时产生标况下3.36 L NO时,溶解LiFePO4________mol(其他杂质不与HNO3反应)。
(5)若滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3后,沉淀中的Li元素占原Li元素总量的90%,计算滤液③中c(CO32-)=__________mol/L。
(6)流程中用“热水洗涤”的原因是________。
(7)工业上将回收的Li2CO3、FePO4粉碎与足量炭黑混合高温灼烧再生制备LiFePO4,写出反应的化学方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气的主要成分是一氧化碳和氢气,可用于合成甲醇、二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1 kJ/mol
CO(g)+3H2(g) △H1=+206.1 kJ/mol
②CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H2=+247.3 kJ/mol
2CO(g)+2H2(g) △H2=+247.3 kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图所示:

则反应前5min的平均反应速率v(H2)=______。10min时,改变的外界条件可能是_______(填代号)。
A.压缩体积 B.增大体积 C.升高温度 D.加入催化剂
(2)如图所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。
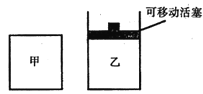
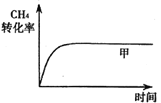
已知甲容器中CH4的转化率随时间变化的图像如图所示,请在图中画出乙容器中CH4的转化率随时间变化的图像_______。
(3)反应③中△H3=________。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见表:
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
此时反应③中正、逆反应速率的关系式是________(填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
(4)800K时向下列三个密闭容器中各充入2 mol H2、1 mol CO,发生反应:2H2(g)+CO(g)CH3OH(g) △H<0,若三容器初始体积相同,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。
甲. 乙.
乙. 丙.
丙.
①达到平衡时,平衡常数K(甲)________K(乙);K(乙)________K(丙)(填“>”、“<”或“=”)。
②达到平衡时H2的浓度c(H2)(甲)________c(H2)(乙);c(H2)(乙)________c(H2)(丙)(填“>”、“<”或“=”)。
(5)在以甲醇为燃料的电池中,电解质溶液为碱性,负极的电极反应式为_________,甲醇应用于燃料电池比甲醇直接用作燃料燃烧的优点是_______(回答一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用![]() 晶体来配制
晶体来配制![]() 的
的![]() 溶液100mL,下列有关说法正确的是( )
溶液100mL,下列有关说法正确的是( )
A.要完成实验需称取16.0g![]() 晶体
晶体
B.本实验只需要用到的仪器有托盘天平、药匙、玻璃棒、烧杯、100mL的容量瓶
C.定容时俯视刻度线会导致所配溶液浓度偏高
D.配制时若容量瓶不干燥,含有少量的蒸馏水,会导致溶液浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝(熔点660℃)是一种应用广泛的金属,工业上用![]() (熔点2045℃)和冰晶石(
(熔点2045℃)和冰晶石(![]() )混合熔融后电解制得。请回答下列问题:
)混合熔融后电解制得。请回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,其原因是__________,冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,请写出铝与V2O5在高温下反应的化学方程式:___________。
(2)将![]() 液和
液和![]() 溶液混合制取
溶液混合制取![]() 。该实验用于盛装NaF溶液的试剂瓶_________(填“能”或“不能”)用玻璃瓶,原因是_______。
。该实验用于盛装NaF溶液的试剂瓶_________(填“能”或“不能”)用玻璃瓶,原因是_______。
(3)下列关于铝元素的叙述不正确的是__________(填序号)。
A.铝是人类最早使用的金属
B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成![]() 。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________,水源中的
。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________,水源中的![]() 对人类健康会产生危害,为了降低水源中
对人类健康会产生危害,为了降低水源中![]() 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将![]() 还原为N2,此时铝主要以
还原为N2,此时铝主要以![]() 的形式存在于溶液中,请写出该反应的离子方程式:__________,当该反应转移5mol电子时,产生的
的形式存在于溶液中,请写出该反应的离子方程式:__________,当该反应转移5mol电子时,产生的![]() 在标况下的体积约为_______L。
在标况下的体积约为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们的生活密切相关,请回答:
(1)在生活中要注意饮食平衡,蛋白质属于_______(填序号,下同)食物,番茄属于______食物;①酸性 ②碱性
(2)有四种常见药物①阿司匹林、②青霉素、③胃舒平、④麻黄碱. 某同学胃酸过多,应该服用______(填序号,下同);从用药安全角度考虑,使用前要进行皮肤敏感性测试的是_____;由于具有兴奋作用,国际奥委会严禁运动员服用的是_________;
(3)苹果汁是人们喜爱的饮品,由于其中含有Fe2+,现榨的苹果汁在空气中会由浅绿色变为棕黄色,若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有________(填序号);①氧化性 ②还原性 ③碱性 ④酸性
(4)食用植物油进入人体后,在酶的作用下水解为高级脂肪酸和_________(写名称),进而被氧化成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料;
(5)硫酸亚铁可用于治疗缺铁性贫血,某贫血患者每天须补充1.4g铁元素,则服用的药物中含硫酸亚铁的质量至少为_________g;
(6)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(﹣NH2)和____(写结构简式或名称).人体中共有二十多种氨基酸,其中人体自身________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸;
(7)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水.写出葡萄糖在体内被氧化的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列说法正确的是 ( )
A.pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合,混合后溶液pH=7
B.碳酸钠溶液中:2c(Na+) =c(CO32-)+c(HCO3-) +c(H2CO3)
C.将0.1 mol·L-1的氢氧化钠溶液与pH=1的稀硫酸等体积混合,混合后的溶液pH=7
D.pH相同的醋酸钠溶液、苯酚钠溶液、碳酸钠溶液、氢氧化钠溶液c(CH3COONa)>c(Na2CO3) >c(C6H5ONa ) >c(NaOH )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)与氢气或与水在催化剂作用下的反应如下:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △H1=-17kJ/mol;
H2S(g)+CO(g) △H1=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H2=-35kJ/mol。
H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列问题:
(1)两个反应在热力学上趋势均不大,其原因是:________________。
(2)反应CO(g)+H2O(g)![]() H2(g)+CO2(g)的△H=_______。
H2(g)+CO2(g)的△H=_______。
(3)羰基硫、氢气、水蒸气共混体系初始投料比不变,提高羰基硫与水蒸气反应的选择性的关键因素是______。
(4)在充有催化剂的恒压密闭容器中只进行反应Ⅰ![]() 设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示:
设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示:

①m1______m2(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
②温度高于T0,COS转化率减小的可能原因为:i有副应发生;ii______;iii______。
(5)在充有催化剂的恒压密闭容器中进行反应Ⅱ.COS(g)与H2O(g)投料比分别为1:3和1:1,反应物的总物质的量相同时,COS(g)的平衡转化率与温度的关系曲线如图所示:
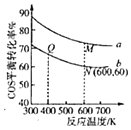
①M点对应的平衡常数______Q点![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ;
;
②N点对应的平衡混合气中COS(g)物质的量分数为______;
③M点和Q点对应的平衡混合气体的总物质的量之比为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com