
【题目】实验室欲用![]() 晶体来配制
晶体来配制![]() 的
的![]() 溶液100mL,下列有关说法正确的是( )
溶液100mL,下列有关说法正确的是( )
A.要完成实验需称取16.0g![]() 晶体
晶体
B.本实验只需要用到的仪器有托盘天平、药匙、玻璃棒、烧杯、100mL的容量瓶
C.定容时俯视刻度线会导致所配溶液浓度偏高
D.配制时若容量瓶不干燥,含有少量的蒸馏水,会导致溶液浓度偏低
科目:高中化学 来源: 题型:
【题目】对于体积相同的①(NH4) 2SO4、②NH4HSO4、③H2SO4溶液,下列说法正确的是( )
A.溶液的pH相同时,3种溶液物质的量浓度大小顺序是③>②>①
B.溶液的pH相同时,将3种溶液稀释相同倍数,pH变化最大的是①
C.溶液的pH相同时,由水电离出的![]() 大小顺序是③>②>①
大小顺序是③>②>①
D.若3种溶液的物质的量浓度都相同,则溶液的pH大小顺序是①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3-
B.含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br-
C.![]() =0.1mol·L-1的溶液:Na+、K+、SO32-、NO3-
=0.1mol·L-1的溶液:Na+、K+、SO32-、NO3-
D.水电离产生的c(H+)为1×10-l2mol·L-1的溶液:AlO2-、Na+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组设计实验对化学反应速率和限度有关问题进行探究:
I.甲小组用如图所示装置进行镁粉分别与盐酸、醋酸(均为0.1mol/L40.00mL)的反应,请回答相关问题:
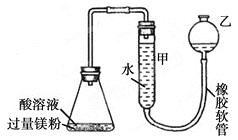
①每次实验至少需要用电子天平(能称准1mg)称取镁粉___g;
②装置中有刻度的甲管可以用代替___(填仪器名称),按图连接好装置后,检查装置气密性的方法是___。实验结束后读取气体体积时应该注意的问题是___(至少回答两点)。
II.乙小组为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图甲、乙所示的实验。请回答相关问题:
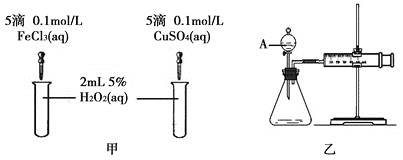
①定性分析:如图甲可通过观察___(填现象),定性比较得出结论。有同学提出将FeCl3溶液改为___(写出试剂及物质的量浓度)更为合理,其理由是___。
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中还需要测量的数据是___。
III.丙小组设计实验探究KI溶液和FeCl3溶液反应存在一定的限度。已知该反应为:2Fe3++2I-=2Fe2++I2。请完成相关的实验步骤和现象。实验步骤如下:
①取5mL0.1molL-1KI溶液,再滴加56滴(约0.2mL)0.1molL-1FeCl3溶液
②充分反应后,将溶液分成两份
③取其中一份,滴加试剂CCl4,用力振荡一段时间,CCl4层出现紫红色,说明反应生成碘。
④另取一份,滴加试剂___溶液(填试剂名称),若现象___,则说明该反应有一定的限度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产铅蓄电池时,在两极板上的铅、锑合金棚架上均匀涂上膏状的PbSO4,干燥后再安装,充电后即可使用,发生的反应是Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。下列对铅蓄电池的说法错误的是( )
2PbSO4+2H2O。下列对铅蓄电池的说法错误的是( )
A.需要定期补充硫酸
B.工作时铅是负极,PbO2是正极
C.工作时负极上发生的反应是Pb-2e-+SO42-=PbSO4
D.工作时电解质的密度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中C%表示某反应物在体系中的百分含量,v表示反应速率,p表示压强,t表示反应时间。图(A)为温度一定时,压强与反应速率的关系曲线;图(B)为压强一定时,在不同时间C%与温度的关系曲线。同时符合以下两个图像的反应是( )
A 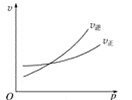 B
B 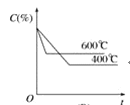
A.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
B.N2O3(g)![]() NO2(g)+NO(g) ΔH>0
NO2(g)+NO(g) ΔH>0
C.3NO2(g)+H2O(l)![]() 2HNO3(l)+NO(g) ΔH<0
2HNO3(l)+NO(g) ΔH<0
D.CO2(g)+C(s)![]() 2CO(g) ΔH>0
2CO(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献。蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%~18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法,其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应式为:2(-NH2)+H2SO4+2H+![]() ;
;
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7;
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量。
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为_________;
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石。
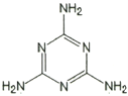
①三聚氰胺的结构如图所示,其化学式为_________,含氮量(氮元素的质量分数)为_________;
②下列关于三聚氰胺的说法中,正确的有_________;
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入_________g的三聚氰胺就可使奶粉“达标”。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料,印泥及朱红雕刻漆器等。某温度时,HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
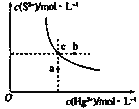
A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小
B.图中a点对应的是饱和溶液
C.向c点的溶液中加入Hg(NO3)2,则c(S2-)减小
D.升高温度可以实现c点到b点的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用软锰矿制备高锰酸钾,主要实验步骤如下:
步骤一:将软锰矿(主要成分为MnO2)、KClO3和KOH固体按一定比例混合后加热熔融可制得绿色K2MnO4;
步骤二:将反应后固体充分溶解、过滤,向滤液中通入过量CO2气体使溶液显酸性,K2MnO4在酸性条件下反应得到KMnO4、MnO2和K2CO3,最后分离得到高锰酸钾晶体(粗产品)。
请回答下列问题:
(1)步骤一加热熔融应在________(填序号)进行。
A.铁坩埚 B.氧化铝坩埚 C.瓷坩埚 D.石英
(2)为进一步提高粗产品(高锰酸钾晶体)的纯度,常采用的实验方法是_____________。
(3)KMnO4、MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等物质的量的氯气消耗KMnO4与MnO2的物质的量之比为________________。
(4)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡),记录的现象如表:
滴入KMnO4溶液的次序(假设每滴溶液体积相等) | 滴入的KMnO4溶液紫色褪去的时间 |
先滴入第1滴 | 1min |
褪色后再滴入第2滴 | 15s |
褪色后再滴入第3滴 | 3s |
褪色后再滴入第4滴 | 1s |
请分析高锰酸钾溶液褪色时间变化的原因:_________。
(5)我国《室内空气质量标准》规定室内空气中甲醛(HCHO)含量不得超过0.08mg/m3。我校某同学通过查阅资料,拟采用如下方法测定2019年暑假新装修的焕然一新的明德楼教室内空气中甲醛的含量。
测定原理:5HCHO+4KMnO4+6H2SO4=2K2SO4+4MnSO4+5CO2↑+11H2O。
实验操作:用容积为1000mL用注射器抽取空气,缓慢注入酸性高锰酸钾溶液中(装置如图),当酸性高锰酸钾溶液正好褪色时,停止注入。

①用0.1000mol/L的酸性KMnO4溶液配制实验中使用的酸性KMnO4溶液l000mL,需0.1000mol/L的酸性KMnO4溶液的体积为___________。
②装置中多孔玻璃球泡的作用是__________。
③该同学在206教室内不同地点抽取空气,并缓慢注入酸性高锰酸钾溶液中。当第250次将注射器中空气全部缓慢注入酸性高锰酸钾溶液中时,酸性高锰酸钾溶液恰好褪色。请通过计算判断,该教室空气中甲醛含量________(填“已”或“未”)超标。若未超标,该教室内空气中甲醛(HCHO)含量为________mg/m3;若已超标,请举出减少室内空气污染的一条合理措施:_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com