
【题目】25℃时,下列说法正确的是 ( )
A.pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合,混合后溶液pH=7
B.碳酸钠溶液中:2c(Na+) =c(CO32-)+c(HCO3-) +c(H2CO3)
C.将0.1 mol·L-1的氢氧化钠溶液与pH=1的稀硫酸等体积混合,混合后的溶液pH=7
D.pH相同的醋酸钠溶液、苯酚钠溶液、碳酸钠溶液、氢氧化钠溶液c(CH3COONa)>c(Na2CO3) >c(C6H5ONa ) >c(NaOH )
【答案】C
【解析】
A.醋酸是弱电解质,氢氧化钠是强电解质,所以pH=2的醋酸浓度大于pH=12的NaOH,二者等体积混合,醋酸有剩余,溶液呈酸性,混合溶液pH<7,故A错误;
B.碳酸钠溶液中存在物料守恒,c(Na+) =2[c(CO32-)+c(HCO3-) +c(H2CO3)],故B错误;
C.pH=1的硫酸中c(H+)=0.1mol/L,NaOH是强电解质,二者等体积混合,恰好反应生成强酸强碱盐硫酸钠和水,溶液呈中性,pH=7,故C正确;
D.pH相同的醋酸钠溶液、苯酚钠溶液、碳酸钠溶液、氢氧化钠溶液,酸根离子水解程度越大,其钠盐浓度越小,水解程度CO32->![]() >CH3COO-,所以钠盐浓度c(CH3COONa)>c(
>CH3COO-,所以钠盐浓度c(CH3COONa)>c(![]() )>c(Na2CO3),氢氧化钠是强碱,浓度最小,故D错误;
)>c(Na2CO3),氢氧化钠是强碱,浓度最小,故D错误;
故选C。


 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
【题目】研究碳、氮、硫等元素化合物的性质或转化对建设生态文明、美丽中国具有重要意义。
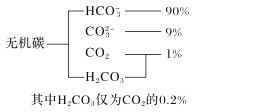
(1)海水中无机碳的存在形式及分布如图所示,用离子方程式表示海水呈弱碱性的主要原因______________________。已知春季海水pH=8.1,预测冬季海水碱性将会_______(填“增强”或“减弱”),理由是_________________。
(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)===CH3OH(g) ΔH<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是________(填字母)。
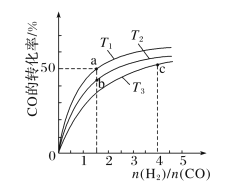
A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.c点状态下再通入1molCO和4molH2,新平衡中H2的体积分数增大
D.a点状态下再通入0.5molCO和0.5molCH3OH,平衡不移动
(3)NO加速臭氧层被破坏,其反应过程如下图所示:
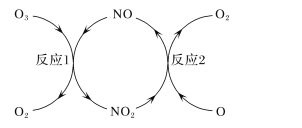
①NO的作用是_________________。
②已知:O3(g)+O(g)===2O2(g) ΔH=-143kJ·mol-1
反应1:O3(g)+NO(g)===NO2(g)+O2(g) ΔH1=-200.2kJ·mol-1 。
反应2:热化学方程式为____________________________。
(4)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-759.8kJ·mol -1,反应达到平衡时,N的体积分数随n(CO)n(NO)的变化曲线如下图。
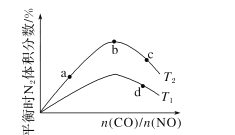
①b点时,平衡体系中C、N原子个数之比接近________。
②a、b、c三点CO的转化率从小到大的顺序为________;b、c、d三点的平衡常数从大到小的顺序为__________。
③若n(CO)n(NO)=0.8,反应达平衡时,N的体积分数为20%,则NO的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中C%表示某反应物在体系中的百分含量,v表示反应速率,p表示压强,t表示反应时间。图(A)为温度一定时,压强与反应速率的关系曲线;图(B)为压强一定时,在不同时间C%与温度的关系曲线。同时符合以下两个图像的反应是( )
A 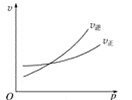 B
B 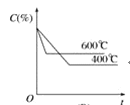
A.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
B.N2O3(g)![]() NO2(g)+NO(g) ΔH>0
NO2(g)+NO(g) ΔH>0
C.3NO2(g)+H2O(l)![]() 2HNO3(l)+NO(g) ΔH<0
2HNO3(l)+NO(g) ΔH<0
D.CO2(g)+C(s)![]() 2CO(g) ΔH>0
2CO(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)。
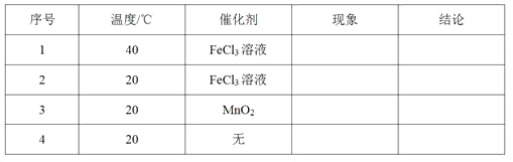
①实验1、2研究的是__________对H2O2分解速率的影响。
②实验2、3的目的是_______________对H2O2分解速率的影响。
(2)查文献可知,Cu2+对H2O2分解也有催化作用,为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
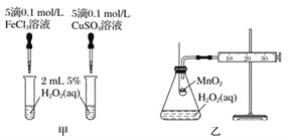
①定性如图甲可通过观察_______,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是_________。
②定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是__________。
(3)酸性高锰酸钾溶液和草酸溶液可发生反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,实验时发现开始反应速率较慢,溶液褪色不明显,但一段时间后突然褪色,反应速率明显加快。对此展开讨论:
①某同学认为KMnO4与H2C2O4的反应是______热反应,导致_______________;
②从影响化学反应速率的因素看,你认为还可能是________的影响。要证明你的猜想,实验方案是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料,印泥及朱红雕刻漆器等。某温度时,HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
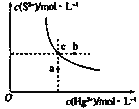
A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小
B.图中a点对应的是饱和溶液
C.向c点的溶液中加入Hg(NO3)2,则c(S2-)减小
D.升高温度可以实现c点到b点的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法错误的是 ( )
A.28克氮气所含的原子数目为2NA;
B.在标况下,0.5NA氯分子所占体积约是11.2L;
C.只有在标况下NA氧气分子的物质的量才是1mol;
D.在70℃、1×105Pa下,46克NO2与标况下46克四氧化二氮均含有3NA原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100mol·L-1的NaOH溶液分别滴定均为20.00mL0.100mol·L-1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是

A. I表示的是滴定醋酸的曲线
B. pH =7时,滴定醋酸消耗的V(NaOH)>20.00mL
C. V(NaOH)= 20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H-H键的键能为436kJ· mol-1,H-N键的键能为391 kJ· mol-1,根据热化学方程式:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4 kJ· mol-1,可知N≡N键的键能是
2NH3(g) △H=-92.4 kJ· mol-1,可知N≡N键的键能是
A.431 kJ· mol-1B.649 kJ· mol-1C.945.6 kJ· mol-1D.896 kJ· mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在接触法制硫酸中,将SO2与空气按1∶3的体积比混合(空气中氮气与氧气的体积比为4∶1)后进入接触室,在一定条件下反应达到平衡后,气体总体积减少为原来的88%(体积均在相同情况下测定),求反应达到平衡时SO2的转化率_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com