
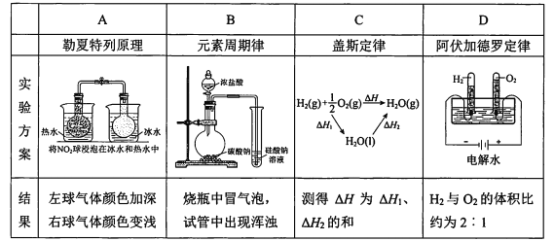
【题目】下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
A. AB. BC. CD. D
【答案】B
【解析】
A、2NO2![]() N2O4是放热反应;
N2O4是放热反应;
B、比较元素的非金属性,应用元素最高价氧化物对应水化物的酸性比较;
C、△H=△H1+△H2;
D、在同温同压下,气体的体积比等于方程式的计量数之比等于气体的物质的量之比;
A、2NO2![]() N2O4是放热反应,升高温度,平衡向生成二氧化氮的方向移动,颜色变深,可以作为勒夏特列原理的依据,故A符合;
N2O4是放热反应,升高温度,平衡向生成二氧化氮的方向移动,颜色变深,可以作为勒夏特列原理的依据,故A符合;
B、比较元素的非金属性,应用元素最高价氧化物对应水化物的酸性比较,浓盐酸不是氯的最高价氧化物对应水化物,无法比较氯和碳的非金属性;生成的二氧化碳中含有HCl气体,氯化氢与二氧化碳都能与硅酸钠溶液反应生成硅酸沉淀,故也无法比较碳和硅的非金属性,不能证明元素周期很,故B不符合;
C、△H=△H1+△H2,化学反应的热效应只与起始和终了状态有关,与变化途径无关,可以证明盖斯定律,故C符合;
D、在同温同压下,气体的体积比等于方程式的计量数之比等于气体的物质的量之比,电解水生成的氧气和氢气体积比等于物质的量之比,可以证明阿伏加德罗定律,故D符合;
故选B。


科目:高中化学 来源: 题型:
【题目】原子团SCN化合价为-1价,在很多方面跟卤素原子相似,因此称为“拟卤素”。拟卤素离子与卤离子还原性强弱顺序为Cl-<Br-<SCN-<I-,又知氧化性I2>S,下列反应不正确的是( )
A. (SCN)2+2Br-=Br2+2SCN-
B. (SCN)2+H2S=2H++2SCN-+S↓
C. 4H++2SCN-+MnO2![]() Mn2++(SCN)2↑+2H2O
Mn2++(SCN)2↑+2H2O
D. (SCN)2+2I-=2SCN-+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1 r溶液的H+的浓度也是0.01 mol·L–1,s通常是难溶于水的有机混合物。上述物质的转化关系如图所示。下列说法正确的是( )
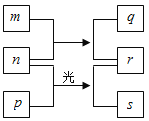
A. 原子半径的大小W<X<YB. 元素的非金属性Z>X>Y
C. Z的氧化物的水化物为强酸D. Y的氢化物常温常压下为液态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、D同主族,B、C、D、E同周期,B、A可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙,C是地壳中含量最高的金属元素。短周期中,B原子半径最大,E的最高价氧化物对应水化物酸性最强。
(1)E的最高价氧化物对应的水化物的分子式为________________;
(2)D与E可形成分子式为D2E2的物质,该物质为浅黄色油状液体,有特殊气味,是一种重要的工业添加剂。则D2E2的结构式为______________;
(3)B、C、D、E、A简单离子半径由大到小的顺序为_______________(用离子符号表示)
(4)用电子式表示化合物甲的形成过程________;
(5)C元素的单质能与B元素的最高价氧化物的水化物发生反应,写出该反应离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不能按![]() (“→”表示一步完成)的关系相互转化的是( )
(“→”表示一步完成)的关系相互转化的是( )
选项 | a | b | c |
A | Fe | FeCl2 | FeCl3 |
B | Si | SiO2 | SiF4 |
C | HNO3 | NO | NO2 |
D | Al | Al2O3 | Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )

A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气的主要成分为CH4,可将CH4设计成燃料电池,来解决能源问题,装置如图所示。在标准状况下,持续通入甲烷,消耗甲烷VL。下列说法错误的是

A. 当0<V≤33.6 L时,负极反应式为CH4+10OH--8e-== CO32-+7H2O
B. 正极反应式为O2 +4H+ +4e-==2H2O
C. 当V=67.2 L时,电池总反应方程式可写为CH4+2O2+NaOH== NaHCO3+2H2O
D. 电解质溶液中的Na+向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求在下列空格中填空。
(1)一定量的乙醇与苯的混合物与足量的金属钠反应,可生成11.2L氢气(在标准状况下),将此混合物燃烧能生成108g水。
①求混合物中苯的质量__________________
(2)某种烃A的蒸气折合成标况下的密度是3.214g/L,已知该烃的碳氢质量比为5∶1,求:
①该烃的相对分子质量:_________,
②如果该烃的一氯取代物有4种,写出该烃的结构简式:___________________________________________
(3)5.8g有机物完全燃烧,只生成CO2和H2O蒸气,其体积比为1:1(同压同温),若把它们通过碱石灰,碱石灰质量增加18.6g,同量的有机物与0.1mol乙酸完全发生酯化反应.又知该有机物对空气的相对密度为2。(注意:羟基不能直接连在双键上)
①有机物的分子式___________________________________________________________
②有机物的结构简式___________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+2ICl(g)![]() I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
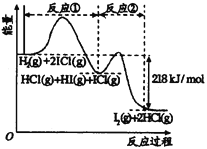
下列有关说法正确的是
A. 反应①为吸热反应
B. 反应①和②均是同种元素间发生的氧化还原反应
C. 反应①比反应②的速率慢,与相应正反应的活化能有关
D. HI(g)+ICl(g) ![]() I2(g)+HCl(g) △H=-218 kJ/mol
I2(g)+HCl(g) △H=-218 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com