
【题目】Ⅰ.某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.800g 试样溶于水,加入过量KI 固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3 标准溶液滴定,到达滴定终点时,平均消耗Na2S2O3 标准溶液40.00 mL。(已知:2Cu2++4I-=2CuI↓+I2;I2+2S2O32-=S4O62-+2I-。)
(1)可选用________作滴定指示剂,滴定终点的现象是________________。
(2)该试样中CuCl2·2H2O 的质量百分数为________________。
Ⅱ.25℃,两种酸的电离平衡常数如表,按要求回答下列问题。
K1 | K2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
(1)用离子方程式表示亚硫酸钠溶液呈碱性的原因________________________________。
(2)浓度均为0.1mol/L的Na2SO3和Na2CO3的溶液中SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为________________________________。
(3)亚硫酸钠溶液中通入少量CO2气体的化学方程式________________________________。
【答案】淀粉溶液 淀粉由蓝色变成无色且半分钟不变化 85.5% SO32-+H2O![]() HSO3-+OH- SO32->CO32->HCO3->HSO3- Na2SO3+CO2+H2O= NaHSO3+ NaHCO3
HSO3-+OH- SO32->CO32->HCO3->HSO3- Na2SO3+CO2+H2O= NaHSO3+ NaHCO3
【解析】
Ⅰ.(1)向含碘的溶液中加入淀粉溶液,溶液变蓝色,再向溶液中加入Na2S2O3溶液,由于碘被Na2S2O3还原为碘离子,溶液蓝色逐渐褪去,当溶液蓝色刚好消失时,碘正好完全反应,从而进行滴定终点的判定;
(2)根据电子转移守恒及I2+2S2O32-═S4O62-+2I-,可得关系式:2Cu2+~I2~2Na2S2O3,则n(CuCl22H2O)=n(Na2S2O3),根据m=nM计算CuCl22H2O的质量,进而计算CuCl22H2O的质量百分数;
Ⅱ.(1)SO32-发生水解,离子方程式为:SO32-+H2O![]() HSO3-+OH-,使溶液呈碱性;
HSO3-+OH-,使溶液呈碱性;
(2)SO32-水解程度小于CO32-,浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-);
(3)亚硫酸钠溶液中通入少量CO2气体的化学方程式为:Na2SO3+CO2+H2O= NaHSO3+ NaHCO3。
Ⅰ.(1)硫代硫酸钠滴定碘单质,利用碘单质遇淀粉变蓝选择指示剂为淀粉,滴入最后一滴Na2S2O3溶液,溶液蓝色褪去,且半分钟内不变色,说明滴定到达终点,
故答案为:淀粉溶液;淀粉由蓝色变成无色且半分钟不变化。
(2)由2Na2S2O3+I2═Na2S4O6+2NaI,2Cu2++4I-═2CuI↓+I2,可得关系式:2Cu2+~I2~2Na2S2O3,则n(CuCl22H2O)=n(Na2S2O3)=0.1000mol/L×0.0400L=0.004mol,故m(CuCl22H2O)=0.004mol×171g/mol=0.684g,所以试样中CuCl22H2O的质量百分数为0.684g/0.800g×100%=85.8%,
故答案为:85.5%。
Ⅱ.(1)Na2SO3是强电解质,全部电离,电离方程式为:Na2SO3=2Na++SO32-,SO32-发生水解,离子方程式为:SO32-+H2O![]() HSO3-+OH-,使溶液呈碱性,
HSO3-+OH-,使溶液呈碱性,
故答案为:SO32-+H2O![]() HSO3-+OH-。
HSO3-+OH-。
(2)依据电离平衡常数大小比较,H2SO3Ki1=1.54×10-2、Ki2=1.02×10-7,H2CO3Ki1=4.3×10-7、Ki2=5.6×10-11。说明SO32-水解程度小于CO32-,浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-),
故答案为:c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-)。
(3)由于H2SO3Ki1=1.54×10-2、Ki2=1.02×10-7,H2CO3Ki1=4.3×10-7、Ki2=5.6×10-11,所以亚硫酸钠溶液中通入少量CO2气体的化学方程式为:Na2SO3+CO2+H2O=NaHSO3+NaHCO3,
故答案为:Na2SO3+CO2+H2O=NaHSO3+NaHCO3。


科目:高中化学 来源: 题型:
【题目】某固体混合物X可能是由Na2SiO3、Fe、Na2CO3、 BaCl2中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计实验方案如下图所示(所加试剂均过量)。

下列说法不正确的是:
A. 气体A一定是混合气体
B. 沉淀A一定是H2SiO3
C. 白色沉淀B在空气中逐渐变灰绿色,最后变红褐色
D. 该固体混合物一定含有Fe、Na2CO3、BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,某同学设计了一个燃料电池并探究氯碱工业的原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。请按要求回答相关问题:
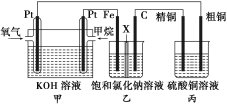
(1)甲烷燃料电池的负极反应为__________________________。
(2)石墨(C)极的电极反应为______________________________。
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的体积为________L。
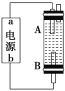
(4)某同学利用甲烷燃料电池设计电解法制取漂白液的实验装置(如图)。若用于制漂白液,a为电池的______极,电解质溶液最好用______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下,向盛有食盐的2L恒容密闭容器中加入0.2molNO2、0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) △H1<0平衡常数K1
NaNO3(s)+ClNO(g) △H1<0平衡常数K1
②2NO(g)+Cl2(g)![]() 2ClNO(g) △H2<0 平衡常数K2
2ClNO(g) △H2<0 平衡常数K2
10分钟时反应达到平衡,测得容器内体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol/(Lmin)。下列说法不正确的是( )
A.反应4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) 的平衡常数为
2NaNO3(s)+2NO(g)+Cl2(g) 的平衡常数为![]()
B.平衡后c(Cl2)=2.5×10-2mol/L
C.其它条件保持不变,反应在恒压条件下进行,则平衡常数K2增大
D.平衡时NO2的转化率为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列8组物质或粒子:
①14N和14C
②16O和18O
③氰酸铵(NH4CNO)与尿素[CO(NH2)2]
④足球烯(C60)和金刚石
⑤CH3CH2CH2CH3和CH(CH3)3
⑥CH3CH2CH3和CH3(CH2)2CH3
⑦![]() 和
和![]()
⑧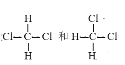
(1)互为同素异形体的是____________(填编号,下同),
(2)互为同位素的是____________,
(3)互为同系物的是____________,
(4)互为同分异构体的是____________。
Ⅱ.回答下列有关有机化学的问题:
(5)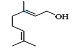 的分子式为____________,该物质所含官能团名称是____________。
的分子式为____________,该物质所含官能团名称是____________。
(6)苯与浓硫酸和浓硝酸混合加热产生硝基苯的反应方程式为____________,反应类型是____________。
(7)下列能使酸性高锰酸钾溶液褪色的是____________。
A.乙醇 B.聚乙烯 C.苯 D.甲苯 E.戊烷 F.苯乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:(图中涉及物质为气态)

(1)如图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式______。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表,
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表,
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请完成下列问题:
①试比较K1、K2的大小,K1______K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_______(填序号字母)。
a .容器内N2,H2,NH3的浓度之比为1:3:2 b. υ(N2)正=3υ(H2)逆
c .容器内压强保持不变 d. 混合气体的密度保持不变
③在400℃时,当测得NH3和N2,H2的物质的量分别为1mol和2mol,3mol时,则该反应的υ(N2)正______υ(N2)逆(填写“>,“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A. 某元素原子的第二电子层电子排布图为![]()
B. 某元素在某种化合物中的化合价为+4
C. 某元素的原子最外层上电子数为6
D. 某元素的外围电子排布式为5s25p1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于小苏打水溶液的表述正确的是
A. c (Na+)=c (HCO3-) + c (CO32-) + 2c (H2CO3)
B. c (Na+) + c (H+) = c (HCO3-) + 2c (CO32-) +c (OH-)
C. HCO3- 的电离程度大于HCO3-的水解程度
D. 存在的电离有:NaHCO3=Na++HCO3—,HCO3— ![]() H++CO32—,
H++CO32—,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林是一种治疗心脑血管疾病的药物,可由化合物![]() 和
和![]() 在一定条件下合成得到(部分反应条件略)。
在一定条件下合成得到(部分反应条件略)。

请回答下列问题:
(1)![]() 的名称为______,
的名称为______,![]() 的反应类型为______。
的反应类型为______。
(2)![]() 的分子式是______。
的分子式是______。![]() 的反应中,加入的化合物
的反应中,加入的化合物![]() 与银氨溶液可发生银镜反应,该银镜反应的化学方程式为____________________________________。
与银氨溶液可发生银镜反应,该银镜反应的化学方程式为____________________________________。
(3)![]() 为取代反应,其另一产物分子中的官能团名称是____________。
为取代反应,其另一产物分子中的官能团名称是____________。![]() 完全燃烧最少需要消耗 ____________
完全燃烧最少需要消耗 ____________![]() 。
。
(4)![]() 的同分异构体
的同分异构体![]() 是芳香酸,
是芳香酸, ,
,![]() 的核磁共振氢谱只有两组峰,
的核磁共振氢谱只有两组峰,![]() 的结构简式为____________,
的结构简式为____________,![]() 的化学方程式为________________________。
的化学方程式为________________________。
(5)上图中,能缩合成体型高分子化合物的酚类单体是____________ ,写出能检验该物质存在的显色反应中所用的试剂及实验现象__________________________________________。
(6)已知:![]() 的原理为:①C6H5OH+
的原理为:①C6H5OH+ +C2H5OH和②
+C2H5OH和②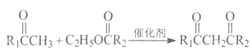 +C2H5OH,
+C2H5OH,![]() 的结构简式为____________。
的结构简式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com