
����Ŀ��(1)������ͼ�е�������ϵ�������C-H�ļ���Ϊ______________��

(2)X(s)+3Y(g)![]() Z(g)+3W(g)����H=��akJ/mol��һ�������£���2molX��2molYͨ��2L�ĺ����ܱ������У���Ӧ10s��ﵽƽ�⣬�������0.5molZ��
Z(g)+3W(g)����H=��akJ/mol��һ�������£���2molX��2molYͨ��2L�ĺ����ܱ������У���Ӧ10s��ﵽƽ�⣬�������0.5molZ��
����10s�ڣ�Y��ƽ����Ӧ����Ϊ_____________����10sʱ��X�����ʵ���Ϊ__________��Y��Ũ��Ϊ_______��10s�ڣ�X��Y��Ӧ�ų�������QΪ______��
���жϸ÷�Ӧ�Ƿ�ﵽƽ���������__________������ĸ����
A.ѹǿ����ʱ��ı� B.������ܶȲ���ʱ��ı�
C.c(Y)����ʱ��ı� D.��λʱ��������Z��W�����ʵ���֮��Ϊ1��2
���𰸡�414kJ/mol 0.075mol/(L��s) 1.5mol 0.25mol/L 0.5akJ BC
��������
(1)���÷�Ӧ��H=��Ӧ���ܼ���-�������ܼ��ܷ������
(2)�ٸ������ʷ�Ӧת����ϵ��������Z�����ʵ������㷴Ӧ���ĵ�X��Y�����ʵ������ٽ��c=![]() ����10sʱY���ʵ�Ũ�ȣ�����v=
����10sʱY���ʵ�Ũ�ȣ�����v=![]() ����Y�ķ�Ӧ���ʣ��������ʷ�Ӧ�����仯�뷴Ӧ�����ʵ������Ӧ����10s�ڷų���������
����Y�ķ�Ӧ���ʣ��������ʷ�Ӧ�����仯�뷴Ӧ�����ʵ������Ӧ����10s�ڷų���������
�����÷�Ӧ�ﵽƽ��ʱ���κ����ʵ����ʵ�����Ũ�ȼ�������������жϡ�
(1)����ͼ֪��C(s)����Ϊ717kJ/mol����������Ϊ(864��2)kJ/mol=432kJ/mol��C(s)+2H2(g)=CH4(g) ��H=-75kJ/mol���÷�Ӧ��H=��Ӧ���ܼ���-�������ܼ���=-75kJ/mol����C-H�ļ���=![]() kJ/mol=414kJ/mol��
kJ/mol=414kJ/mol��
(2)���ɷ���ʽX(s)+3Y(g)![]() Z(g)+3W(g) ��H=-akJ/mol��֪��ÿ��Ӧ����1molZ����ͬʱ����1molX������3molY����Ӧ�ų�����akJ����Ӧ���е�10s��ﵽƽ�⣬��ʱ��Ӧ����0.5molZ����ͬʱ�ų�0.5akJ������������0.5molX��1.5molY�������Y��ʾ�ķ�Ӧ����Ϊv(Y)=
Z(g)+3W(g) ��H=-akJ/mol��֪��ÿ��Ӧ����1molZ����ͬʱ����1molX������3molY����Ӧ�ų�����akJ����Ӧ���е�10s��ﵽƽ�⣬��ʱ��Ӧ����0.5molZ����ͬʱ�ų�0.5akJ������������0.5molX��1.5molY�������Y��ʾ�ķ�Ӧ����Ϊv(Y)=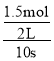 =0.075mol/(L��s)����ʱX�����ʵ�������2mol-0.5mol=1.5mol��
=0.075mol/(L��s)����ʱX�����ʵ�������2mol-0.5mol=1.5mol��
��A.�÷�Ӧ�Ƿ�Ӧǰ�������������ķ�Ӧ����ϵ��ѹǿʼ�ղ��䣬��˲��ܸ���ѹǿ����ʱ��ı��жϷ�Ӧ�Ƿ���ƽ��״̬��A����
B.����Ӧδ�ﵽƽ��״̬������������ᷢ���仯��������ܶ�Ҳ�ᷢ���ı䣬��������������ܶȲ���ʱ��ı䣬��Ӧ�ﵽƽ��״̬��B��ȷ��
C.��Ӧδ�ﵽƽ��״̬��Y�����ʵ�����Ũ�Ⱦͻ�仯����c(Y)����ʱ��ı䣬˵����Ӧ����ƽ��״̬��C��ȷ��
D.���ݷ���ʽ��֪��Z��W������������߸ı�����ʵ����ı���1��3�������Ƿ�ﵽƽ�⣬��λʱ��������Z��W�����ʵ���֮�Ȳ�����Ϊ1��2����˲��ܾݴ��жϷ�Ӧ�Ƿ���ƽ��״̬��D����
�ʺ���ѡ����BC��


 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��һ����Ϣ���ϵ����Ӽ�������ͬ�����£�A������ͬ�������������88.25������A�����и�Ԫ�����������ֱ�Ϊw(C)��54.4%��w(H)��7.4%��w(O)��18.1%��w(Cl)��20.1%��A�ڲ�ͬ�����¿ɷ�����ͼ��ʾ��һϵ�б仯��
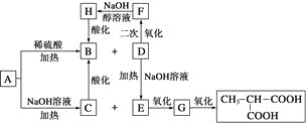
��ش��������⣺
(1)A�ķ���ʽΪ__________��
(2)D���Ӻ��еĹ�������________________��
(3)����ת����ϵ�Ļ�ѧ����ʽ�У�����ˮ�ⷴӦ����________��(������)��
(4)д����ѧ����ʽ��
��A��ϡ���Ṳ�ȣ�____________________________________________________��
��E������G��__________________________________________________��
��F���������ƴ���Һ���ȣ�__________________________________________��
(5)��B��Ϊͬ���칹�����������״�������ʹ���____�֡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ƣ�Na2S2O4���׳Ʊ��շۣ��ǹ�ҵ����Ҫ�Ļ�ԭ��Ư����Ҳ����Ҫ��ʳƷ����������ijѧϰС��ģ�ҵ�������ʵ����ȡ���շۡ�
��֪��Na2S2O4�ǰ�ɫ���壬��ԭ�Ա�Na2SO3ǿ�������ᷴӦ��2S2O42-+4H+��3SO2��+S��+2H2O����
��һ��п�۷�
����1������ͼ��ʽ���¶ȿ�����40��45�棬������ƿ����ҺpH��3��3.5ʱ��ֹͣͨ��SO2����Ӧ��õ�ZnS2O4��Һ��
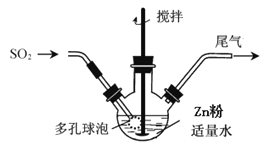
����2�����õ���ZnS2O4��Һ����NaOH��Һ�У����ˣ�����ΪZn��OH��2������Һ�м���һ����ʳ�Σ���������Na2S2O42H2O���塣
����3���������ˣ����Ҵ�ϴ�ӣ���120��140����ȷ����õ�Na2S2O4��
�����������Ʒ�
����4������ͼ��ʽ����װ���е�Zn�ۺ�ˮ����HCOONa��Na2CO3��Һ���Ҵ����¶ȿ�����70��83�棬����ͨ��SO2��ά����ҺpH��4��6����5��8Сʱ��ַ�Ӧ��Ѹ�ٽ���45��55�棬����������ˮNa2S2O4��
����5�������ˣ����Ҵ�ϴ�ӣ�����õ�Na2S2O4��
�ش��������⣺
��1������1�����з�����Ӧ�Ļ�ѧ����ʽ��______�������ж�����ݵ�������______��
��2������2�С�����Һ�м���һ����ʳ�Σ���������Na2S2O42H2O���塱��ԭ���ǣ��ñ�Ҫ�Ļ�ѧ���������˵����______��
��3�����ַ����п����¶ȵļ��ȷ�ʽ��______��
��4����������ʵ������жϣ�Na2S2O4��ˮ���Ҵ��е��ܽ���Ϊ��______��
��5�������Ʒ�������Na2S2O4���ܷ�ӦΪ______��
��6�����ַ�����Ƚϣ�п�۷���Ʒ���ȸߣ����ܵ�ԭ����______��
��7���������¸������Լ������ʵ��֤�������Ʒ��ƵõIJ�Ʒ�к���Na2SO4��
ϡ���ᡢϡ���ᡢϡ���ᡢAgNO3��Һ��BaCl2��Һ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʵ����ʵ��������Ӧ���۲���ȷ����(����)
ѡ�� | ��ʵ | ���� |
A | ��ҵ�������У��ڿ�ʯ�����Σ�����ʯ���������� | ����Ӧ��ĽӴ�������ӿ컯ѧ��Ӧ���� |
B | A��B��֧�Թ��зֱ��������5%��H2O2����B�Թ��м���MnO2��B�Թ��в������ݿ� | ��������������ʱ���������Ըı仯ѧ��Ӧ���� |
C | ����������ͬ��Na2S2O3��Һ��H2SO4��Һ��Ӧ��������Һ���¶ȣ��������������ʱ���� | ��������������ʱ�����߷�Ӧ�¶ȣ���ѧ��Ӧ���ʼӿ� |
D | һ�������£�H2(g)��I2(g) | c(I2)����I2���ʵ������� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��ZΪ������Ԫ�أ�Xԭ�ӵ�����������Z��Y��������֮�ͣ�Z��Yλ��ͬһ���ڣ�Yԭ�Ӻ�����3��δ�ɶԵ��ӣ��ǽ���Z��һ�ֹ��嵥�ʿɵ��硣�ش��������⣺
��1��Y�����ڱ��е�λ���ǵ�______���ڵ�_____�壬��ԭ�ӽṹʾ��ͼΪ_______________��Y��Z֮���γɵĻ�ѧ������__________��
��2��X��Y��Z����Ԫ����ԭ�Ӱ뾶������__________(��Ԫ�ط���)��X���ʼȿ������ᷴӦ���ֿ���������������Һ������������Ϊ__________(�����ʽ)����������Y���ʷ�Ӧ�Ļ�ѧ����ʽΪ____________________________________��
��3��Z�����������ĵ���ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
(1)�±��Ǹ�С���о�Ӱ���������(H2O2)�ֽ����ʵ�����ʱ�ɼ���һ�����ݣ���10mL H2O2��ȡ150mLO2�����ʱ��(��)
| 30% H2O2 | 15% H2O2 | 10% H2O2 | 5% H2O2 |
������������ | ��������Ӧ | ��������Ӧ | ��������Ӧ | ��������Ӧ |
���������� | 360 | 480 | 540 | 720 |
MnO2���������� | 10 | 25 | 60 | 120 |
�ٸ��о�С������Ʒ���ʱ��������Ũ�ȡ�___________��____________�����ضԹ�������ֽ����ʵ�Ӱ�졣
�ڴ�����Ӱ���������ֽ����ʵ���������ѡһ����˵�������ضԷֽ������к�Ӱ�죿_______________________��
(2)��������ͬ���ۼ�״̬��ͬ��MnO2�ֱ���뵽5mL 5%(�ܶ�Ϊ1.0g/cm3)��˫��ˮ�У����ô����ǵ�ľ�����ԡ��ⶨ������£�
ʵ�� ��� | ������MnO2�� | ���� ��� | �۲��� | ��Ӧ��� �����ʱ�� |
A | ��ĩ״ | ��ϲ��� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 5span>���� |
B | ��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
�� д��H2O2�����ֽ�Ļ�ѧ��Ӧ����ʽ________________�����ʵ��A��H2O2��5�����ڵ�ƽ����Ӧ����________________�����������С�������λ���֣�
�� ʵ����˵���������õĴ�С��____________________�йء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ������ȷ����
A.������������������۷ֱ���ȫȼ�գ����߷ų���������
B.��ѧ��ӦA2(g)��2B2(g)===2AB2(g)�����仯��ͼ��ʾ���÷�ӦΪ���ȷ�Ӧ
C.��25����101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g)+O2(g)![]() 2H2O(l)��H= -285.8kJ��mol-1
2H2O(l)��H= -285.8kJ��mol-1
D.��ϡ��Һ�У�H+(aq)+OH-(aq)![]() H2O(l)��H=-57.3kJ��mol-1��������0.5molH2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��������̷ų�����������57.3kJ
H2O(l)��H=-57.3kJ��mol-1��������0.5molH2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��������̷ų�����������57.3kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�ķ���ʽ����ȷ����
A. �������죺2Fe+Al2O3![]() 2Al+Fe2O3
2Al+Fe2O3
B. �˹��̵���N2+3H2![]() 2NH3
2NH3
C. �ô�������ۣ�CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
D. ��ʪ��ĵ���KI��ֽ����Cl2��Cl2+2I-=2Cl-+I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.����������������Һ��Ӧ��H++OH-=H2O
B.̼������ˮ������ӷ���ʽ��HCO3-+H2O![]() H3O++CO32��
H3O++CO32��
C.ˮ��Һ��NaHSO3�ĵ��뷽��ʽ��NaHSO3=Na++H++SO32-
D.��С�մ�����θ����ࣺHCO3-��H��=CO2����H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com