
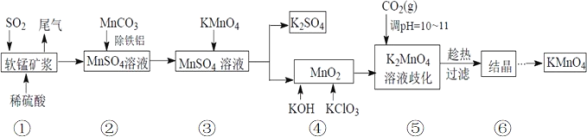
【题目】高锰酸钾是中学化学中常用的强氧化剂。某化学研究小组用软锰矿(主要成分为MnO2另含有少量铁、铝等金属的化合物)吸收燃煤尾气中的SO2,并制取MnO2和K2SO4,而后又用MnO2 制取KMnO4。设计生产流程如下:请回答下列问题:
 20℃时,相关物质的溶解度数据见下表:
20℃时,相关物质的溶解度数据见下表:
(1)若将SO2气体通入下列溶液中,溶液不会褪色的是___。
A.紫色石蕊试液 B.品红溶液 C.新制氯水 D.酸性高锰酸钾溶液
(2)用 MnCO3 除去液体中的 Fe3+时发生的离子方程式__________。
(3)步骤④中应在______中熔化;
A.瓷坩埚 B.铁坩埚 C.石英坩埚 D.蒸发皿
当溶液调 pH达10~11时,停止通入 CO2。若 CO2过多,会造成的后果是:______。
(4)在此生产流程中,可循环使用的物质是(填名称)________。
步骤⑤中发生反应的化学方程式为_________;
步骤⑤之后,趁热过滤的理由是________。
【答案】A 3MnCO3+2Fe3++3H2O=3Mn2++2Fe(OH)3↓+3CO2↑ B CO2与K2CO3反应生成KHCO3,结晶时会同一起结晶析出,降低产品的纯度 MnO2、CO2、KMnO4 3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2↓ 防止KMnO4结晶析出,提高 KMnO4的产量
【解析】
(1)根据SO2的性质分析判断;
(2)MnCO3与溶液中的H+发生反应,使溶液中Fe3+形成Fe(OH)3沉淀而除去;
(3)KOH是碱,能够与SiO2在高温下反应,据此分析;
根据K2CO3与CO2及H2O反应转化为KHCO3分析;
(4)根据反应流程分析判断物质及反应的方程式。
(1)A.SO2与溶液中的水反应产生H2SO3,H2SO3是酸,具有酸的通性,可以使紫色石蕊试液变为红色,不褪色,A符合题意;
B.SO2具有漂白性,能够使品红溶液的红色褪去,B不符合题意;
C.新制氯水中含有HClO,HClO是具有强氧化性的物质,可以将有色物质氧化变为无色,因此具有漂白作用,C不符合题意;
D.酸性高锰酸钾溶液具有强的氧化性,SO2具有还原性,二者发生氧化还原反应而使溶液的紫色褪去,D不符合题意;
故合理选项是A;
(2)MnCO3与溶液中的H+发生反应,使溶液中c(OH-)增大,导致溶液中Fe3+形成Fe(OH)3沉淀而除去,则用MnCO3除去液体中的Fe3+时发生的离子方程式为:3MnCO3+2Fe3++3H2O=3Mn2++2Fe(OH)3↓+3CO2↑;
(3)KOH是碱,在高温下能够与SiO2反应,所以不能使用含有SiO2的容器反应;
A.瓷坩埚中含有SiO2,不能熔化KOH,A不符合题意;
B.铁坩埚中不含有SiO2,与Fe不能反应,可以熔化KOH,B符合题意;
C.石英坩埚主要成分是SiO2,与KOH在高温下反应,所以不能熔化KOH,C不符合题意;
D.蒸发皿主要成分是硅酸盐,其中含有SiO2,可以与KOH在高温下发生反应,不能在高温下熔融KOH,D不符合题意;
故合理选项是B;
向含有KOH的溶液中通入CO2气体,调整溶液的pH至10~11,二者反应产生K2CO3和水,若通入CO2过多,则又会发生反应:K2CO3+CO2+H2O=2KHCO3,结晶时会同KMnO4一起结晶析出,降低产品的纯度;
(4)向软锰矿(主要成分为MnO2)浆中加入稀硫酸,并通入SO2气体,发生氧化还原反应产生MnSO4,向该酸性溶液中加入MnCO3,消耗溶液中的H+,使溶液中的Fe3+、Al3+形成Fe(OH)3、Al(OH)3沉淀而除去,MnCO3与H+反应,产生Mn2+和CO2,向MnSO4溶液中加入KMnO4溶液,发生氧化还原反应产生MnO2,向其中再加入KOH、KClO3,发生氧化还原反应,产生K2MnO4,向该碱性溶液中通入CO2,调整溶液的pH至10~11,KOH与CO2反应产生K2CO3,K2MnO4发生歧化反应产生KMnO4、MnO2,CO2转化为MnCO3,所以在该流程中,能够循环利用的物质有MnO2、CO2、KMnO4;
步骤⑤中K2MnO4在CO2存在条件下,发生歧化反应产生KMnO4、MnO2,发生反应的化学方程式为3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2↓;
步骤⑤之后,要趁热过滤,这是由于温度高,KMnO4的溶解度大,温度降低,KMnO4的溶解度降低,导致KMnO4的产量降低,高温过滤就可以防止KMnO4结晶析出,从而提高 KMnO4的产量。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】铜及其化合物在工农业生产和日常生活中有着广泛的用途。请回答下列问题:
(1)基态铜原子的核外电子排布式为___。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2![]() NF3+3NH4F
NF3+3NH4F
①上述化学方程式中的5种物质所属的晶体类型有__![]() 填序号
填序号![]() 。
。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
②F、N、O三种元素的第一电离能由大到小的顺序为__![]() 用元素符号表示
用元素符号表示![]()
(3)铜晶体铜原子的堆积方式为面心立方最密堆积。每个铜原子周围距离最近的铜原子数目为___。
(4)某X原子的外围电子排布式为3s23p5,铜与X形成化合物的晶胞如图所示(黑点代表铜原子)。
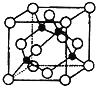
![]() 该晶体的化学式为___。
该晶体的化学式为___。
②已知该晶体的密度为ρg·cm-3,阿伏加德罗常数的数值为NA,则该晶体中晶胞的棱长为__pm(只写计算式![]() 。
。
(5)合成氨工艺的一个重要工序是铜洗,其目的是用铜液![]() 醋酸二氨合铜(I)、氨水
醋酸二氨合铜(I)、氨水![]() 吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3[Cu(NH3)3CO]Ac(Ac表示醋酸根
吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3[Cu(NH3)3CO]Ac(Ac表示醋酸根![]()
①如果要提高上述反应的反应速率,可以采取的措施是___。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
②铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为___。
③NH3的氮原子的杂化类型为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是( )
A. 沸点:戊烷>2,2-二甲基戊烷>2,3-二甲基丁烷>丙烷
B. 密度:CCl4>CHCl3>H2O>苯
C. 含氢质量分数:甲烷>乙烷>乙烯>乙炔>苯
D. 等质量的物质燃烧耗O2量:苯>乙烷>乙烯>甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是( )
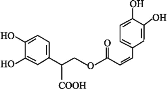
A.迷迭香酸的分子式为:C17H15O8
B.1 mol迷迭香酸最多能与9 mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
D.1 mol迷迭香酸最多能与含5 mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应产物中,有的同时生成多种同分异构体,有的则没有。其中一定不存在同分异构体的反应是:
A.异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B.2—氯丁烷(![]() )与NaOH乙醇溶液共热发生消去反应
)与NaOH乙醇溶液共热发生消去反应
C.甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D.![]() 邻羟基苯甲酸与NaHCO3溶液反应
邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为周期表的一小部分,A、B、C、D、E 的位置关系如图所示。其中 B 元素最高化合价是最低化合价绝对值的 3 倍,它的最高价氧化物中含氧 60%。下列说法正确的( )
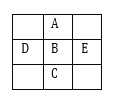
A.D、B、E 三种元素的非金属性逐渐减小
B.B 元素最高价氧化物对应的水化物是强酸
C.A 元素是空气中含量最多的元素
D.气态氢化物的稳定性顺序: D > B > E
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知mX(g)+nY(g)![]() gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是
gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.升高温度,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,Y的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
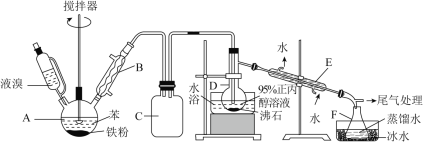
【题目】溴苯和1-溴丙烷是重要的医药中间体。某化学兴趣小组设计如下方案制得两种有机物,实验步骤如下:
I.连接装置后,检査气密性。向各容器中加入一定量的药品。
II.将液溴滴入装置A中,保持75℃水浴加热装置C10min。
III.反应完毕后,将装置F馏出液分离,得1-溴丙烷的粗产品。
IV.将分出的粗产品,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,进一步提纯得1-溴丙烷。
有关数据如下:
苯 | 溴 | 溴苯 | 1-溴丙烷 | 正丙醇 | |
密度/gcm-3 | 0.88 | 3.10 | 1.50 | 1.36 | 0.8 |
沸点/℃ | 80 | 59 | 156 | 71 | 97.1 |
水中溶解度 | 难溶 | 难溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)写出装置A中发生反应的方程式:________。
(2)装置B的作用________。
(3)步骤IV中第一步水洗的目的主要是________。
(4)制得的溴苯中含有少量的苯,提纯溴苯的实验操作名称________。
(5)从锥形瓶内分离出1-溴丙烷粗产品,所采用的操作名称是________![]() 检验1-溴丙烷中的溴原子,需加入的试剂
检验1-溴丙烷中的溴原子,需加入的试剂![]() 按照先后顺序写
按照先后顺序写![]() ________。
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某澄清透明的溶液中可能存在:Fe2+、Cu2+、Mg2+、SO32-、Br-、SO42-等离子中的一种或几种,现进行如下实验:
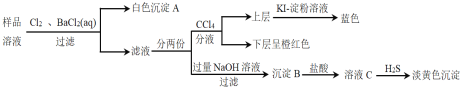
下列说法不正确的是:
A.溶液中一定不存在Mg2+、Cu2+B.溶液中一定不存在SO32-
C.溶液中一定存在Fe2+、Br-、SO42-D.沉淀B中可能含有氢氧化镁,肯定含有氢氧化铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com