
����Ŀ��ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽���������Ի�ѧ��Ӧ���ʵ�Ӱ������ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������·���������t3 <t2 <t1��
ʵ���� | H2C2O4��Һ | ����KMnO4��Һ | �¶� ���棩 | ��Һ��ɫ������ɫ����ʱ�䣨s�� | ||
Ũ����mol/L�� | �����mL�� | Ũ����mol/L�� | �����mL�� | |||
�� | 0.10 | 2.0 | 0.01 | 4.0 | 25 | t1 |
�� | 0.20 | 2.0 | 0.01 | 4.0 | 25 | t2 |
�� | 0.20 | 2.0 | 0.01 | 4.0 | 50 | t3 |
��ش�
��1����֪��Ӧ��H2C2O4ת��ΪCO2�ݳ���KMnO4ת��ΪMnSO4��ÿ����1molH2C2O4ת��_______mol���ӡ����۲쵽��ɫ�պ���ȥ���μӷ�Ӧ��H2C2O4��KMnO4�����ʵ���֮��Ϊn(H2C2O4)��n(KMnO4)=_________��
��2��ʵ��ٲ��KMnO4��Һ����ɫʱ��Ϊt1=40s�����Ի��ǰ����Һ����ı仯�����ʱ����ƽ����Ӧ������(KMnO4)��___________mol/(L��min)��
��3�����ݱ��е�ʵ��ں�ʵ������ݣ����Եõ��Ľ�����__________________________��
��4����С��ͬѧ���ݾ��������n(Mn2+)��ʱ��仯���Ƶ�ʾ��ͼ����ͼa��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+)��ʱ��仯������Ӧ����ͼb��ʾ��

��С��ͬѧ����ͼb��ʾ��Ϣ������µļ��裬����������ʵ��̽����
�ٸ�С��ͬѧ����ļ�����__________________________________________��
�����������С��ͬѧ���ʵ�鷽��������д���пհף�
ʵ���� | H2C2O4��Һ | ����KMnO4��Һ | �¶� ���棩 | ���Թ��м����������� | ��Һ��ɫ������ɫ����ʱ�䣨s�� | ||
Ũ�ȣ�mol/L�� | �����mL�� | Ũ�ȣ�mol/L�� | �����mL�� | ||||
�� | 0.20 | 2.0 | 0.01 | 4.0 | 50 | _____ | t4 |
������С��ͬѧ����ļ��������Ӧ�۲쵽��������___________________________��
���𰸡�25��20.01�����������䣬�����¶ȣ���Ӧ��������Mn2+�Է�Ӧ�������MnSO4��Һ��ɫ������ɫ���죬����ʱ��t4<t3
��������
��1��H2C2O4��̼Ԫ�صĻ��ϼ�Ϊ+3�ۣ����ڷ�Ӧ��ת��ΪCO2����̼Ԫ�صĻ��ϼ���+3���ߵ�+4����ÿ����1molH2C2O4ת��2����4-3��mol���ӣ��ڷ�Ӧ��KMnO4ת��ΪMnSO4���ɵ�ʧ������Ŀ�غ�ɵ÷�Ӧ����ʽ��2MnO4-��5H2C2O4��6H+===2Mn2+��10CO2��+8H2O����μӷ�Ӧ��H2C2O4��KMnO4�����ʵ���֮��Ϊ5:2���ʴ�Ϊ��2��5��2��
��2����ʵ����У�KMnO4��Һ�ij�ʼŨ��Ϊ��0.01mol/L��4.0ml��6ml=![]() mol/L��40s����Һ��ɫ��˵��KMnO4�������꣬�仯��Ũ��Ҳ��
mol/L��40s����Һ��ɫ��˵��KMnO4�������꣬�仯��Ũ��Ҳ��![]() mol/L�����䷴Ӧ����Ϊ��
mol/L�����䷴Ӧ����Ϊ��![]() mol/L��
mol/L��![]() min=0.01mol/L���ʴ�Ϊ��0.01��
min=0.01mol/L���ʴ�Ϊ��0.01��
��3����ʵ��ں�ʵ��۶Աȿ�֪�����߷�Ӧ��Ũ����ͬ����Ӧ���¶Ȳ�ͬ��ʵ�������Һ��ɫʱ��϶̣�˵����Ӧ���ʽϿ죬��ɵý��ۣ������������䣬�����¶ȣ���Ӧ��������
��4������ͼb�����߿ɵã���Ӧ��ʼ��ѧ��Ӧ��������Ͽ죬˵����������MnSO4�Է�Ӧ�д����ã��ʴ�Ϊ��Mn2+�Է�Ӧ������ã�
��Ҫ��֤���裬����ж���ʵ�飬�ɱ������ݿ�֪����ʵ��۽��жԱȣ�������������ͬʱ������MnSO4���弴�ɣ��ʴ�Ϊ��MnSO4��
������С��ͬѧ����ļ��������Mn2+�Ը÷�Ӧ�д����ã���Ӧ���ʼӿ죬��Һ��ɫ��ʱ�����̣��ʴ�Ϊ����Һ��ɫ������ɫ���죬����ʱ��t4<t3��


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO��H2�ϳ�CH3OH�Ļ�ѧ����ʽΪCO(g)+2H2(g) ![]() CH3OH(g) AH<0,������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
CH3OH(g) AH<0,������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. �¶ȣ�T1>T2>T3
B. ����Ӧ���ʣ�v(a)>v(c), v(b)>v(d)
C. ƽ�ⳣ����K(a)>K(c)��K(b)=K(d)
D. ƽ��Ħ��������M(a)<M(c)��M(b)<M(d)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�����仯����������������Ӧ����㷺�����������ͺ����²��ϵ�Ӧ�ñ��ܹ�ע����������������ѭ���ѽ�ˮ�������Ĺ�������ͼ��ʾ�������������¶�������أ����¶ȵ���570��ʱ����ӦFe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g)���谭ѭ����Ӧ�Ľ��С�
3Fe(s)+4CO2(g)���谭ѭ����Ӧ�Ľ��С�

��֪��i. Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g);��H1=+19.3 kJ��mol��1
3FeO(s)+CO2(g);��H1=+19.3 kJ��mol��1
ii. 3FeO(s)+H2O(g)![]() Fe3O4(s)+H2(g);��H2=��57.2 kJ��mol��1
Fe3O4(s)+H2(g);��H2=��57.2 kJ��mol��1
iii. C(s)+CO2(g)![]() 2CO(g);��H3=+172.4 k]��mol��1
2CO(g);��H3=+172.4 k]��mol��1
��������ѭ���ѽ�ˮ�������ܷ�Ӧ���Ȼ�ѧ����ʽ��___________��
(2)T1��ʱ����ij�����ܱ������м���һ������Fe2O3��̿�ۣ�������ӦFe2O3(s)+3C(s)![]() 2Fe(s)+3CO(g)����Ӧ�ﵽƽ�����t1ʱ�̣��ı�ij������V(��)��ʱ��(t)�ı仯��ϵ��ͼ��ʾ����t1ʱ�̸ı������������___________(��д��ĸ)��
2Fe(s)+3CO(g)����Ӧ�ﵽƽ�����t1ʱ�̣��ı�ij������V(��)��ʱ��(t)�ı仯��ϵ��ͼ��ʾ����t1ʱ�̸ı������������___________(��д��ĸ)��

a.�����¶Ȳ��䣬ѹ������ b.����������䣬�����¶�
c.����������䣬������̼�� d.����������䣬����COŨ��
(3)��һ���¶��£���ij����ɱ�ĺ�ѹ�ܱ�����(p��)����1molCO2��������̼��������Ӧ��ƽ��ʱ��ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ
��650��ʱ���÷�Ӧ��ƽ������յ�������___________��
��T��ʱ������ƽ����ϵ���ٳ���һ������V(CO2)�UV(CO)=5�U4�Ļ�����壬ƽ��___________(����������������������������)�ƶ���
��925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��KpΪ___________��[�����ѹ(p��)=������ѹ(p��)�������������ij���ʵ�ƽ���ѹ�������ʵ���Ũ��Ҳ���Ա�ʾ��ѧƽ�ⳣ��������Kp]

(4)��ԭ���ԭ�����Գ�ȥ���Է�ˮ�е�������ϩ��AsO3������ԭ������ͼ��ʾ(������ڲ�Ϊ���������)

�ڳ��۹����У�����������е�FeΪԭ��ص�___________��(����������������)��д��C2HCl3�������ת��Ϊ����ĵ缫��ӦʽΪ___________��
(5)��֪25��ʱ��Ksp[Fe(OH)3]=4.0��10��38�����¶�������ʵ����������100mL5mol��L��1FeCl3��Һ��Ϊʹ���ƹ����в����ֻ���������������Ҫ����2mol��L��1������_________mL(���Լ����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(NH4)2SO4��һ�ֳ����Ļ��ʣ�ij������ʯ�ࡢNH3��H2O��CO2�Ʊ�(NH4)2SO4�Ĺ����������£�

����˵����ȷ����
A. ͨ��NH3��CO2��˳����Ի���
B. ����2Ϊ����Һ����Ũ������ȴ�ᾧ�����ˣ��ɵ�(NH4)2SO4
C. ������з�Ӧ�����ӷ���ʽΪCa2++2NH3+CO2+H2O=CaCO3��+2NH4+
D. ͨ���NH2��CO2��Ӧ�������ҹ���������CO2��ѭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ĺ�������(CaO2)�ǰ�ɫ�ķ�ĩ��������ˮ���������Ҵ��������������½�Ϊ�ȶ�����һ������ˮ����ֳ���������������ʻ�ˮ��Ʒ�����䡣ʵ���ҿ��ø�����ȡCaO2��8H2O���پ���ˮ�Ƶ�CaO2��CaO2��8H2O��0��ʱ�ȶ���������ʱ��������ͷֽ⣬������130��ʱ��Ϊ��ˮCaO2��
���Ʊ��������£�
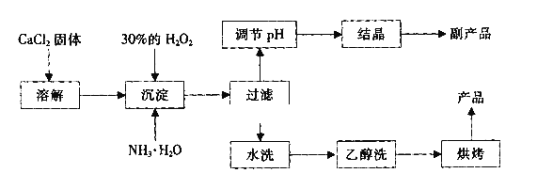
(1)�û�ѧ����ʽ��ʾ��������������ˮ����ֳ��������ԭ����_______________��
(2)Ϊ�˿��Ƴ����¶�Ϊ0�����ң���ʵ�����˲�ȡ�ķ�����__________________��
(3)���Ʒ��ĸ���ƷΪ___________(�ѧʽ)��Ϊ����߸���Ʒ�IJ��ʣ��ᾧǰҪ����Һ��pH���������ʷ�Χ���ɼ��������Լ��е�____________(��дA��B)��
A������ B����ˮ
(4)Ϊ�˼�����ˮϴ���Ƿ�ϸ�ȡ����ϴ��Һ���Թ��У��ٵμ�__________���м�顣
(5)�ⶨ��Ʒ��CaO2�ĺ�����ʵ�鲽���ǣ�
��һ����ȷ��ȡag��Ʒ��������ƿ�У�������������ˮ������bgKI���壬�ٵ�������2 mol��L��1��H2SO4��Һ����ַ�Ӧ��
�ڶ�������������ƿ�м��뼸�ε�����Һ��
����������μ���Ũ��Ϊc mol/L��Na2S2O3��Һ����Ӧ��ȫ������Na2S2O3��ҺVmL�� ����֪��I2+2S2O32-=2I-+S4O62-(��ɫ)��
����������˵����Ӧǡ����ȫ��������___________________________________��
��CaO2����������Ϊ______________________________________������ĸ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣�����������ĸ�ֱ����ijһԪ�ء����ݱ�������Ԫ�ػش����⣺

��1��Ԫ��B�����ڱ��е�λ����______��
��2���ϱ�������Ԫ���н�������ǿ����______����Ԫ�ط��ţ���
��3������������Ӧˮ����������ǿ������______���ѧʽ����
��4��A��C��D��Ԫ���γɻ�����ĵ���ʽΪ______���û������к��е���������______��
��5������F��G��HԪ�ؿ��γ���Ar������ͬ���Ӳ�ṹ�ļ����ӣ���Щ���ӵİ뾶�ɴ�С��˳����______�������ӷ��ű�ʾ����
��6��E����B��C�γɵij�����������ȼ�յķ���ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йشӺ�������ȡ���ʵ��ԭ����װ���ܴﵽʵ��Ŀ�ĵ���

A. ��װ�ü������麣��
B. ��װ���ҹ��˺����ҵĽ���Һ
C. ��װ�ñ��Ʊ�������������Һ��I��Cl2
D. ��װ�ö�������������Һ��I���Cl2β��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҽ��������X�����ӳ�θ���ڷ�ҩ�����͡���������
A.BaCO3B.BaOC.BaCl2D.BaSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڣ�50��ʱҺ���д���������ƽ�⣺2NH3(Һ)![]() NH4+��NH2-���������ӵ�ƽ��Ũ�Ⱦ�Ϊ1.0��10��15mol��L��1�������йأ�50��ʱ���ӻ�����������ȷ����(����)
NH4+��NH2-���������ӵ�ƽ��Ũ�Ⱦ�Ϊ1.0��10��15mol��L��1�������йأ�50��ʱ���ӻ�����������ȷ����(����)
A. ���ӻ�Ϊ1.0��10��15
B. ���ӻ�Ϊ1.0��10��30
C. ��Һ���м��백����(NaNH2)��Һ�������ӻ�����
D. ��Һ���м���NH4Cl��c(NH4+)�������ӻ�����ֵҲ��֮����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com