
【题目】请按要求填空:
(1)简单原子的原子结构可用下图形象地表示:

其中“●”表示质子或电子,“○”表示中子,则下列有关①②③的叙述正确的是__
A.①②③是三种不同的核素
B.①②③具有相同的质量数
C.①②③互为同位素
D.①②③是三种化学性质不同的粒子
(2)科学家已发现一种新型氢分子(H3),在相同条件下,等质量的H3和H2相同的是__
A 分子数 B 原子数 C 体积 D 电子数
(3)微粒AXn+ 核外有a个电子,则它的核内中子数为______
(4)与10克D2O含有相同电子数的NH3在标准状况下的体积是_____
【答案】AC BD ![]() 11.2L
11.2L
【解析】
(1)根据示意图不难看出①②③分别是H、D、T原子:
A.首先明确核素的定义,不同的原子即不同的核素,氕、氘、氚明显是三种不同的核素,A项正确;
B.质量数=质子数+中子数,氕、氘、氚的质量数分别为1、2、3,B项错误;
C.氕、氘、氚互为氢元素的同位素,C项正确;
D.同位素的化学性质几乎完全一样,物理性质有差别,D项错误;
答案选AC;
(2)![]() 的分子量为3,
的分子量为3,![]() 的分子量为2,等质量的
的分子量为2,等质量的![]() 和
和![]() ,其分子数为反比,即2:3:
,其分子数为反比,即2:3:
A.分子数为2:3,A项错误;
B.不管是![]() 还是
还是![]() ,都是由氢原子构成的,因此等质量的
,都是由氢原子构成的,因此等质量的![]() 和
和![]() 必然是由等量的氢原子构成的,B项正确;
必然是由等量的氢原子构成的,B项正确;
C.虽然在相同条件下,但是二者的分子数不同,因此体积不同,C项错误;
D.同B项,二者都是由等量的氢原子构成的,因此二者所含的电子数也是相等的,D项正确;
答案选BD;
(3)首先![]() 带有n个正电荷,表明其失去了n个电子,则
带有n个正电荷,表明其失去了n个电子,则![]() 有
有![]() 个电子,又因为电子数=质子数,质量数=质子数+中子数,不难得出其核内有
个电子,又因为电子数=质子数,质量数=质子数+中子数,不难得出其核内有![]() 个中子;
个中子;
(4)1个![]() 分子中有
分子中有![]() 个电子,一个
个电子,一个![]() 分子中有
分子中有![]() 个电子,可以发现二者的电子数相等,n(
个电子,可以发现二者的电子数相等,n(![]() )=
)=![]() ,则
,则![]() 的物质的量也为0.5mol,v(
的物质的量也为0.5mol,v(![]() )=
)=![]() 。
。


科目:高中化学 来源: 题型:
【题目】明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,含有少量氧化铁,利用明矾石制备K2SO4的工艺流程如图所示:

据此流程图回答下列问题:
(1)①焙烧炉中Al2(SO4)3与S反应的产物是两种氧化物,该反应的化学方程式为______;写出炉气的一种用途________。
(2)②中Al2O3参与反应的离子方程式为__________。
(3)③中调节pH不能用CO2的理由是____________________。
(4)工业冶炼金属铝需要定期更换补充阳极碳块的原因是__________________。
(5)纯净氢氧化铝经历两次__________________(填反应类型)可制得铝。以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池负极的电极反应式是__________________。
(6)现有明矾石1 625 t,按上述流程制得780 t Al(OH)3,忽略铝元素的损失,请计算明矾石中钾元素的质量分数为____________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘海醇为非离子型造影剂,适用于有造影剂反应的高危因素的病人。下面是以化合物A为原料合成碘海醇的路线:
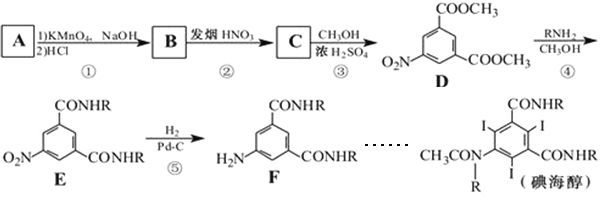
其中R-为-CH2CH(OH)CH2OH
请回答以下问题:
(1)物质D中含有的官能团为________。
(2)A是苯的同系物,相对分子量为106,则A的结构简式是_______________。
(3)写出A的侧链与氯气发生一氯取代的条件_____________。
(4)反应②的化学方程式______________。
(5)反应①→⑤中,属于氧化反应的是_____________(填序号)。
(6)写出能同时满足下列条件的D的两种同分异构体的结构简式:_________。
Ⅰ.苯环上有3个取代基,苯环上的一卤代物有2种;
Ⅱ.能发生银镜反应,水解产物之一能与FeCl3溶液发生显色反应;
Ⅲ.含有1个α-氨基酸的结构(例如:CH3CH(NH2)COOH属于α-氨基酸)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有三个不成对的电子;C元素可分别与A、B、D生成RC2型化合物,其中的DC2与C3互为等电子体。下列叙述中不正确的是
A. D原子的简化电子排布式为[Ar]3s23p4
B. B、C两元素的第一电离能大小关系为B>C
C. 用电子式表示AD2的形成过程为![]()
D. 由B60分子形成的晶体与A60相似,分子中总键能:B60>A60
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图像的说法正确的是
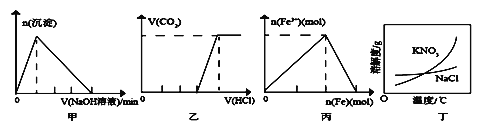
A. 图甲表示:向某明矾溶液中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与滴加NaOH溶液体积的关系
B. 图乙表示:向含等物质的量的NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量,生成气体的体积与滴加HCl溶液体积的关系
C. 图丙表示:在稀硝酸溶液中逐渐加入铁粉至过量,溶液中Fe3+物质的量与逐渐加入铁粉物质的量的变化关系
D. 除去混在硝酸钾中少量的氯化钠可用“蒸发浓缩、趁热过滤”的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
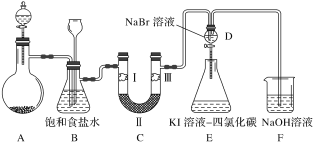
(1)制备氯气选用的药品为二氧化锰和浓盐酸,则相关的化学反应方程式为:_____。
(2)装置B中饱和食盐水的作用是___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入_____。(填字母)
a | b | c | d | |
Ⅰ | 干燥的 有色布条 | 湿润的 有色布条 | 湿润的 有色布条 | 干燥的 有色布条 |
Ⅱ | 碱石灰 | 无水CaCl2 | 浓硫酸 | 无水CaCl2 |
Ⅲ | 湿润的 有色布条 | 干燥的 有色布条 | 干燥的 有色布条 | 湿润的 有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为橙黄色,打开D装置中活塞,将D中少量溶液加入装置E中,振荡。观察到的现象是_________。经认真考虑,有同学提出该实验方案仍有不足,请说明其中原因___________。
(5)装置F中用足量NaOH溶液吸收剩余的氯气,试写出相应的化学方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如图装置(部分夹持装置已略去),以探究潮湿的Cl2与Na2CO3反应得到固体物质的成分。

(1)试剂X的化学式________。A中制取Cl2的离子方程式____________________。
(2)试剂Y的名称为______________。
(3)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中除含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究。
①提出合理假设。
假设1:存在两种成分:NaHCO3和____________________________;
假设2:存在三种成分:NaHCO3和__________________________。
②设计方案,进行实验。写出实验步骤以及预期现象和结论。_______
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。

(4)已知Cl2O与水反应生成次氯酸,则D中Cl2O进入E反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“●”代表一种元素,其中A代表氢元素。
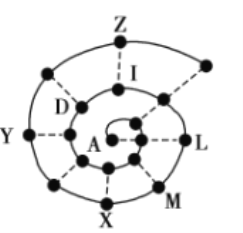
(1)X的元素符号为______,I元素在周期表中的位置为______。
(2)M与Z两种元素形成的化合物的化学式为______。
(3)下列说法正确的是______(填序号)。
a.I元素形成的单质通入LZ的溶液中可得Z元素形成的单质
b.虚线相连的元素处于同一主族
c.L元素形成的单质在D元素形成的单质中燃烧生成![]()
d.X、Y、M元素为同周期元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com