
【题目】凯里一中2018届高一(1)班的两名同学用酸碱中和滴定的方法测定烧碱溶液的浓度。过程如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准硫酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且30秒内颜色不再改变为止,测得所耗硫酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL蒸馏水,测得所耗盐酸为V2mL。
试回答下列问题:
(1)滴定时边滴边摇动锥形瓶,眼睛应观察______________;
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)锥形瓶中的溶液从_______色变为_______色时,且30秒种不变化,停止滴定。
(3)该小组在步骤中①错误是______________,由此造成的测定结果分别是_______,(填偏高、偏低或无影响)。
(4)步骤②缺少的操作是______________________。
(5)如下图,是某次滴定时的滴定管中的液面,则其读数为_______mL。

(6)根据下列数据

请计算待测烧碱溶液的浓度为______________mol/L。
【答案】B锥形瓶内溶液颜色的变化红无用待测溶液润洗锥形瓶2~3次偏高用标准盐酸润洗酸式滴定管22.59或22.600.1000
【解析】
分析:(1)滴定操作时,左手控制旋塞,右手震荡锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化;(2)随着滴入锥形瓶中硫酸的增多,溶液的PH 逐渐增大,溶液从红色变为无色时,且30秒种不变化,达到滴定终点;(3)锥形瓶不能用待测溶液润洗;若用待测液润洗,锥形瓶中碱的物质的量偏大,消耗酸体积偏大,由此造成的测定结果偏大;(4)滴定管用蒸馏水洗净后,要用待盛液润洗2~3次;(5)滴定管刻度从上到下依次增大;(6)每次消耗硫酸的体积为滴定前后的读数差。根据化学反应方程式计算。
解答:(1)为及时关闭旋塞减小误差,滴定操作时,眼睛应观察锥形瓶内溶液颜色的变化;(2)随着滴入锥形瓶中硫酸的增多,溶液的PH 逐渐增大,酚酞从红色变为无色时,且30秒种不变化,达到滴定终点;(3)锥形瓶不能用待测溶液润洗,步骤中①错误是用待测溶液润洗锥形瓶2~3次;若用待测液润洗,锥形瓶中碱的物质的量偏大,消耗酸体积偏大,由此造成的测定结果偏高;(4) 滴定管用蒸馏水洗净后,要用待盛液润洗2~3次;步骤②缺少的操作是用待盛液润洗2~3次;(5)精确到0.01 mL,读数为22.60;(6)两次平均消耗硫酸的体积为20.00 mL,
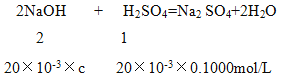
C=0.1000 mol/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(一)雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO![]() 2CO2(g)+N2(g)△H<O
2CO2(g)+N2(g)△H<O
①反应的速率-时间图像如图甲所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图乙所示.以下说法正确的是___________(填对应字母).
![]()

A.a1>a2 B.b1<b2 C.t1>t2
D.图乙中阴影部分面积更大 E.图甲中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是_________(填代号)

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
2NO2(g)![]() N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:______________.
(3)CH4和H2O(g) 在催化剂表面发生反应CH4+H2OCO+3H2,该反应在不同温度下的化学平衡常数如表:
温度/℃ | 800 | 1000 | 1200 | 1400 |
平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
①该反应是_________反应(填“吸热”或“放热”).
②T℃时,向1L密闭容器中投入l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O![]() CO+3H2的平衡常数K=______________.
CO+3H2的平衡常数K=______________.
(二)恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g) ![]() xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x=____________
(2)从反应开始到10s,B的平均反应速率为____________
(3)从反应开始到40s达平衡状态,A的平均反应速率为____________
(4)平衡时容器中B的体积分数为____________
(5)下列各项能表示该反应达到平衡状态是____________
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) =2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 将AlCl3溶液加热蒸干得到纯净的氯化铝晶体 B. 强电解质都易溶于水,所以BaSO4是弱电解质
C. 强酸溶液一定比弱酸溶液导电性强 D. 电解质溶液的导电过程会发生化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应的本质是旧化学健的断裂和新化学键的形成。已知某些化学键的键能数据如下:
化学键 | H—H | Cl—Cl | H—Cl |
键能/(kJ·mol-1) | 436 | 243 | 431 |
则下列热化学方程式不正确的是( )
A. ![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g)
Cl2(g)===HCl(g)
ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)===2HCl(g) ΔH=-183 kJ·mol-1
C. ![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g)
Cl2(g)===HCl(g)
ΔH=+91.5 kJ·mol-1
D.2HCl(g)===H2(g)+Cl2(g) ΔH=+183 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. C 、N 、O的第一电离能依次增大
B. NH3 、H3O+、NH4+ 均含有配位键
C. P4、 CCl4、 CH4 均为正四面体结构,键角均为109°28′
D.HClO 、 HClO3 、 HClO4的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,0.01 mol·L-1 MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱稀溶液反应的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A.-69.4 kJ·mol-1
B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1
D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请回答下列问题:
(1)已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是______________。D是双原子分子,相对分子质量为30,则D的分子式为______________。
(2)油脂A经下列途径可得到M。

图中②的提示: ![]()
反应①的反应类型是_________________。 反应②的化学方程式是 ________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,分子量为134,写出C一种可能的结构简式:________________________________。
(4)若将0.15 mol B与足量的金属钠反应,则需消耗___________g金属钠。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2CrO![]() +2H+Cr2O
+2H+Cr2O![]() +H2O。某科研小组用如图电解装置,由Na2CrO4溶液制取Na2Cr2O7溶液。下列有关叙述正确的是( )
+H2O。某科研小组用如图电解装置,由Na2CrO4溶液制取Na2Cr2O7溶液。下列有关叙述正确的是( )

A.CrO![]() 生成Cr2O
生成Cr2O![]() 的反应为非氧化还原反应,不能通过电解方法获得
的反应为非氧化还原反应,不能通过电解方法获得
B.a为电源正极
C.d口流出的NaOH溶液的浓度与c口通入的NaOH溶液的浓度相同
D.Na+从右侧通过阳离子交换膜进入左侧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com