
【题目】氢化铵与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述中错误的是( )
A.NH4H是离子化合物
B.NH4H溶于水所形成的溶液显酸性
C.NH4H与水反应时,NH4H是还原剂
D.NH4H固体投入少量的水中,有两种气体产生
【答案】B
【解析】
A.依据题意NH4H与氯化铵的结构相似,则性质也应相似,氯化铵是铵盐,属于离子化合物,因此NH4H也是离子化合物,由![]() 和H-构成的离子化合物,故A不符合题意;
和H-构成的离子化合物,故A不符合题意;
B.NH4H与水发生了氧化还原反应,NH4H+H2O=NH3H2O+H2↑,生成的NH3H2O是弱碱,水溶液中呈碱性,故B符合题意;
C.根据NH4H和H2O反应过程中化合价的升降,可知NH4H中H-化合价升高为0价,作还原剂,故C不符合题意;
D.该反应生成H2和NH3H2O,NH3H2O的浓度较大或加热时,会分解生成NH3,NH4H固体投入少量的水中,生成NH3H2O的浓度较大,且该反应为放热反应,因此最终有两种气体产生,故D不符合题意;
故答案为:B。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,0.1 mol N2(g)与0.3 mol H2(g)在恒容密闭容器中发生反应:N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-akJ·molˉ1(a>0)。下列说法正确的是
2NH3(g)ΔH=-akJ·molˉ1(a>0)。下列说法正确的是
A.容器内气体的压强不再发生变化,说明反应达到平衡状态
B.达到化学平衡状态时,正、逆反应速率都为零
C.相同时间内,断开H—H键的数目和生成N-H键的数目相等
D.平衡时容器内气体的浓度c(N2)∶c(H2)∶c(NH3)=1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将电石与水反应产生的气体通入酸性高锰酸钾溶液 | 溶液紫色褪去 | 证明有乙炔生成 |
B | 取CH3COONa溶液于试管中并加入几滴酚酞,再加热 | 溶液红色加深 | CH3COONa溶液显碱性且存在水解平衡 |
C | 向蔗糖溶液中加入稀硫酸,加热几分钟后加入新制Cu(OH)2悬浊液,加热煮沸 | 无红色沉淀生成 | 蔗糖没有发生水解反应生成葡萄糖 |
D | 向Na2S2O3溶液中滴加H2SO4溶液至过量 | 一段时间后溶液变浑浊 | Na2S2O3在该反应中只作氧化剂 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液A中可能只含有K+、Fe3+、Cu2+、Fe2+、Ag+、Mg2+、Al3+、NH4+、Cl-、NO3-、SO42-中的若干种,为检验确认其中所含的各离子,取1L溶液A,进行如下实验:

已知气体A、B的体积都为2.24L(标况下),沉淀B的物质的量为0.1mol,根据以上实验操作与现象,有关于该溶液的结论正确的是:
A.溶液A中肯定存在Fe2+、Ag+、Mg2+、NO3-
B.溶液A中一定不含Al3+
C.溶液A中可能含有Cu2+、Cl-
D.溶液A中c(NO3-)≥1.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
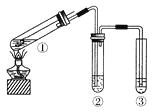
A. 上下移动①中铜丝可控制SO2的量
B. ②中选用品红溶液验证SO2的生成
C. ③中选用NaOH溶液吸收多余的SO2
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用电石制取乙炔的装置如下图所示,请填空:

(1)写出仪器的名称:①是________________,②是________________;
(2)制取乙炔的化学方程式是________________;
(3)仪器①中加入的是________________,其目的是________________;
(4)将乙炔通入KMnO4酸性溶液中观察到的现象是________________,乙炔发生了___________反应(填“加成”或“取代”或“氧化”,下同);
(5)为了安全,点燃乙炔前应________________,乙炔燃烧时的实验现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列转化的化学方程式,注明反应类型。
(1)甲苯→TNT ___________________
(2)乙烯→聚乙烯__________________
(3)1,3—丁二烯与氯气1,4—加成__________________
(4)溴乙烷和氢氧化钠的乙醇溶液共热___________________
(5)乙醇在铜催化下和氧气反应__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣![]() 主要成分为
主要成分为![]() 、
、![]() 和少量Fe、Cu的氧化物
和少量Fe、Cu的氧化物![]() 为原料制备
为原料制备![]() 实验过程如下:
实验过程如下:

![]() 酸溶过程中,
酸溶过程中,![]() 发生的化学方程式为______。
发生的化学方程式为______。
![]() 加入
加入![]() 的作用为______。
的作用为______。
![]() 下列关于分液漏斗及其使用方法的叙述,正确的是______
下列关于分液漏斗及其使用方法的叙述,正确的是______![]() 。
。
A 使用前要先检查玻璃塞和旋塞处是否漏液
B 将加入有机萃取剂后的混合液转移到分液漏斗中,塞上玻璃塞,用右手压住分液漏斗玻璃塞,左手握住旋塞,倒转漏斗,用力振荡,并不时旋开旋塞放气
C 分液时,必须塞紧上口玻璃塞,保证密封,以防止有机萃取剂挥发
D 本实验中,含![]() 的有机相一定从下口放出,水层从上口倒出
的有机相一定从下口放出,水层从上口倒出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com