
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质:
)等产品。下表列出了有关物质的部分物理性质:
名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 (d水=1g·cm-3) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体,易燃、易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶; 酸性:苯甲酸>醋酸
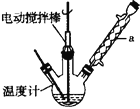
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作溶剂不参加反应)和2mL甲苯,搅拌升温至70℃ ,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。请回答下列问题:
(1)装置a的名称是 ________,主要作用是 ________;三颈瓶中发生反应的化学方程式为 ________,此反应的原子利用率理论上可达 ________(保留四位有效数字)。
(2)经测定,反应温度过高时,苯甲醛的产量有所减少,可能的原因是 ________。
(3)反应完毕后,反应混合液经过自然冷却至室温后,还应经过 ________、 ________
(填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是 ________ (按步骤顺序填字母)。
a.对混合液进行分液 b.与适量碳酸氢钠溶液混合振荡
c.过滤、洗涤、干燥 d.水层中加入盐酸调节pH=2
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取1.500g产品,溶于乙醇配成100mL溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol·L-1 KOH标准溶液滴定,到达滴定终点时消耗KOH溶液20.00mL。产品中苯甲酸的质量分数为 ________ (保留四位有效数字)。
③下列情况会使测定结果偏低的是 ________ (填字母)。
A.滴定终点时仰视读取耗碱量
B.锥形瓶洗净后还留有蒸馏水
C.配置KOH标准溶液时俯视定容
D.碱式滴定管滴定前有气泡,滴定终点时气泡消失
【答案】球形冷凝管 冷凝回流,防止甲苯的挥发而降低产品产率 ![]() 66.25%或0.6625 H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量 过滤 蒸馏 badc 81.33﹪或0.8133 C
66.25%或0.6625 H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量 过滤 蒸馏 badc 81.33﹪或0.8133 C
【解析】
(1)由仪器a结构可知为球形冷凝管,甲苯挥发会导致产率降低;
(2)三颈瓶中甲苯被过氧化氢氧化生成苯甲醛,同时还生成水;原子利用率=(预期产物的总质量÷全部反应物的总质量)×100%;
(3)温度过高时过氧化氢分解,实际参加反应的过氧化氢质量减小,影响产量;
(4)反应完毕后,反应混合液经过自然冷却至室温时,先过滤分离固体催化剂,再利用蒸馏的方法分离出苯甲酸;
(5)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸.
①先与碳酸氢钠反应之后为苯甲酸钠,再分液分离,水层中加入盐酸得到苯甲酸晶体,最后过滤分离得到苯甲酸;
②苯甲酸的物质的量等于消耗KOH物质的量,再计算产品中苯甲酸的质量分数;
③先分析错误操作对KOH的物质的量的影响,再根据苯甲酸的物质的量等于消耗KOH物质的量分析纯度测定的误差。
(1)仪器a具有球形特征的冷凝管,名称为为球形冷凝管,甲苯挥发会导致产率降低,冷凝回流,防止甲苯挥发导致产率降低,
故答案为:球形冷凝管;冷凝回流,防止甲苯的挥发而降低产品产率;
(2)三颈瓶中甲苯被过氧化氢氧化生成苯甲醛,同时还生成水,反应方程式为:![]() ,此反应中原子利用率=
,此反应中原子利用率=![]() ×100%=66.25%;
×100%=66.25%;
故答案为:球形冷凝管;冷凝回流,防止甲苯的挥发而降低产品产率; ![]() ;66.25%;
;66.25%;
(3)H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量,
故答案为H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量;
(4)反应完毕后,反应混合液经过自然冷却至室温时,先过滤分离固体催化剂,再利用蒸馏的方法分离出苯甲酸,
故答案为:过滤;蒸馏;
(5)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①先与碳酸氢钠反应之后为苯甲酸钠,再分液分离,水层中加入盐酸得到苯甲酸晶体,最后过滤分离得到苯甲酸,再洗涤、干燥得到苯甲酸,故正确的操作步骤是:dacb,
故答案为:dacb;
②苯甲酸为一元酸,则根据酸碱中和滴定原理可知,其物质的量等于消耗KOH物质的量,则1.500 g产品中苯甲酸的质量为0.020 L×0.1 mol/L×![]() ×122g/mol = 1.22 g,产品中苯甲酸的质量分数为
×122g/mol = 1.22 g,产品中苯甲酸的质量分数为![]() ×100%
×100% ![]() 81.33﹪或0.8133;
81.33﹪或0.8133;
故答案为:81.33﹪或0.8133;
③
A. 滴定终点时仰视读取耗碱量,导致V(标准)偏大,即KOH的物质的量偏大,则苯甲酸的物质的量偏大,使最终产品纯度偏高,故A项错误;
B. 在锥形瓶中加水,对测定结果无影响,故B项错误;
C. 配置KOH标准溶液时俯视定容,则导致V(标准)偏小,即KOH的物质的量偏小,则苯甲酸的物质的量偏小,使最终产品纯度偏低,故C项正确;
D. 碱式滴定管开始尖嘴处留有气泡,达滴定终点时气泡消失,即KOH的物质的量偏大,则苯甲酸的物质的量偏大,使最终产品纯度偏高,故D项错误;
答案选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/LNaOH溶液500mL。根据溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是__________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是__________。

(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)__________。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1cm~2cm处
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器
②不宜贮存溶液
③不能用来加热
④使用之前要检查是否漏水
这些叙述中正确的是__________(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)根据计算用托盘天平称取的NaOH固体质量为______g。固体应放在_______中称量。
(5)下面操作造成所配溶液浓度偏高的是__________(填字母)。
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D. 摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是 。
(2)完成以下实验步骤:组装好实验装置,首先 ___________ ,再加入实验药品。接下来的实验操作是 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是 。
(3)若去掉装置B,则导致测定结果 (填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见 。
【方案2】按以下步骤测定样品中A1N的纯度:

(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作是 。A1N的纯度是 (用m1、m2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素T、Q、R、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族族序数相等。它们的最高价氧化物的水化物依次为甲、乙、丙、丁。下列叙述不正确的是
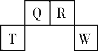
A. R的氢化物可以既有极性键又有非极性键
B. 常温下丁的浓溶液可用T单质所制的容器来盛装
C. 丁的浓溶液与Q的单质加热发生反应,可生成体积比为1:2的两种气体
D. 甲、乙、丙、丁受热均易分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人造空气(氧气与氦气的混合气)可用于减轻某些病痛或供深水潜水员使用。标准状况下,5.6 L“人造空气”的质量是2.4 g,其中氧气与氦气的质量比是( )
A. 1∶1 B. 2∶1 C. 1∶4 D. 2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.配制480 mL 0.3 mol/L NaOH溶液。具体如下:
(1)需_________g NaOH。
(2)配制过程中,下列仪器不会用到的是_____(填字母),尚缺少的玻璃仪器有_____、______。
A.托盘天平 B.250 mL容量瓶 C.玻璃棒 D.胶头滴管
(3)实验过程中两次用到玻璃棒,其作用分别是: _____________、_______________。
(4)下列操作的正确顺序是:B→_____→_____→____→____→____→G (用字母表示)。
A.冷却 B.称量C.洗涤 D.定容E.溶解 F.转移 G.摇匀
Ⅱ.乙同学用18.4 mol/L浓硫酸配制100 mL 3.6 mol/L的稀硫酸。用100 mL量筒量取20.0 mL浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。你认为此法是否正确?________若不正确,指出其中错误之处______。
Ⅲ.在配制物质的量浓度溶液时,判断下列操作出现的后果。(填“偏低”、“偏高”或“无影响”)
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体:________。
(2)配制氢氧化钠溶液时,容量瓶中有少量水:_______。
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度:______。
(4)转移时不慎将溶液倒在瓶外:__________;
(5)定容时俯视容量瓶刻度线:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期律和元素周期表,下列推断不合理的是( )
A. 第84号元素的最高化合价是+7
B. 第七周期0族元素的原子序数为118
C. 第35号元素的单质在常温常压下是液体
D. 位于第四周期第VA族的元素为非金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com