
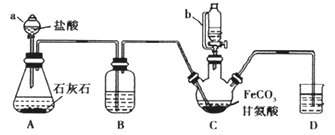
����Ŀ���ʰ�������[(NH2CH2COO)2Fe]��һ�ֲ���ǿ������ijѧϰС������FeCO3��ʰ���(NH2CH2COOH)�Ʊ��ʰ���������ʵ��װ������ͼ��ʾ���гֺͼ���������ʡ�ԣ���
�й������������±�
�ʰ��� | ������ | �ʰ������� |
������ˮ�������Ҵ� | ������ˮ���Ҵ� | ������ˮ���������Ҵ� |
���Ի����� | ǿ���ԡ�ǿ��ԭ�� |
ʵ����̣�
��ϳɣ�װ��C��ʢ��0.2 mol FeCO3��200 mL 1.0 mol��L1�ʰ�����Һ�����������ᡣʵ��ʱ���ȴ�����a�Ļ�������װ��C�п����ž����Ȳ����Ͻ��裬��ͨ������b��C�м�����������������Һ����p�ȵ�6���ң�ʹ��Ӧ���ַ�Ӧ��
����룺��Ӧ�������ˣ�����Һ��������Ũ����������ˮ�Ҵ������ˡ�ϴ�Ӳ����
�ش��������⣺
��1������C��������___________����a��ȣ�����b���ŵ���_______��
��2��װ��Bʢװ���Լ�Ϊ_____________��
��3���ϳɹ��̼���������������Ǵٽ�FeCO3�ܽ��______________��
��4����������������Һ����pH������6���ʰ������������½���ԭ��������ӷ���ʽ��ʾΪ________________��
��5������II��ϴ�Ӳ���Ϊ________��
��6�������Ʒ���Ƿ���Fe3+������Լ���_________��д��ѧ�����
��7����ʵ���Ƶ�15.3 g �ʰ�������(M=204g/mol)�����������_______����
���𰸡�������ƿ ƽ����ѹ��ʹҺ��˳������ ����NaHCO3��Һ ��ֹFe2+������ Fe2++2OH= Fe(OH)2�� ��©���м����Ҵ�����û���壬���Ҵ���Ȼ���£��ظ�2-3�� KSCN 75
��������
�������з�Ӧ���輰ʵ��װ��ͼ��֪��װ��AΪ�����ʯ��ʯ��Ӧ����CO2�ķ���װ�ã����ɵ�CO2���������ž�װ��C�еĿ�����װ��BΪCO2�ľ���װ�á�װ��CΪ�ʰ����FeCO3��Ӧ�Ʊ��ʰ��������ķ�Ӧװ�á����������ʱ���֪����������л�ԭ�ԣ�����ȷ��FeCO3������������Ӧ���������øʰ��������������Ҵ������иʰ��������ķ��롢ϴ�ӵȲ�����
��1������CΪ������ƿ������aΪ��Һ©��������bΪ��ѹ��Һ©�������a��˵��b����ƽ������ѹǿ��ʹ©����Һ��˳�����£�
��2��װ��B�������dz�ȥCO2�����л��е�HCl����ֹ���ʵ����ɸ��ţ��ʿ�ѡ��NaHCO3��Һ��
��3����������������ʣ���������л�ԭ�ԣ����Ա�֤Fe2+����������
��4��pH������6����Һ��c(OH-)�ϴ�Fe2+��OH-��Ӧ����Fe(OH)2���������ӷ���ʽΪ��Fe2++2OH= Fe(OH)2����
��5���ʰ��������������Ҵ�������
��6��Fe3+��KSCN��Ӧ��������Ѫ��ɫ��������һ����KSCN�����м��飻
��7��15.3g�ʰ������������ʵ���Ϊ![]() ��200 mL 1.0 mol��L1�ʰ�����Һ�иʰ�������ʵ���Ϊ
��200 mL 1.0 mol��L1�ʰ�����Һ�иʰ�������ʵ���Ϊ![]() ��FeCO3�����ʵ���Ϊ0.2 mol�������Ͽ�����0.1mol�ʰ��������������Ϊ
��FeCO3�����ʵ���Ϊ0.2 mol�������Ͽ�����0.1mol�ʰ��������������Ϊ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��̽����������ȡ:
I:��Ҫ�Լ�����������
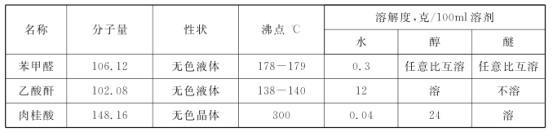
ע��:����������ˮ����ˮ�ⷴӦ
II :��Ӧ����.
ʵ�����Ʊ������Ļ�ѧ����ʽΪ:  +(CH3CO2)O
+(CH3CO2)O![]()
![]() +CH3COOH
+CH3COOH
III��:ʵ�鲽�輰����
����250 mL������ƿ�У���ͼ�ף�����3 ml��3. 15 g��0. 03 mol����������ı���ȩ��8 ml��8. 64g��0. 084 mol��������������������Լ���ϸ��4.2 g��ˮ̼��ء����ÿ��������ܻ�����������45min�����ڷ�Ӧ�ж�����̼�ݳ����ɹ۲쵽��Ӧ�����д�����ĭ���֡�
�ڷ�Ӧ��ϣ��ڽ�������ӦҺ�з�������20 mLˮ������������̼�����кͷ�ӦҺ��pH����8��Ȼ�����ˮ����������ͼ�ң�����������ƿ�е�ʣ��Һ����ȴ�������̿���10-15 min�����г��ȹ��ˡ��ڽ����£���HCl���뵽��Һ�У������岻������ʱ�����ˣ��õ���Ʒ����������ù���3.0 g��
IV����ͼ��ʾװ��:
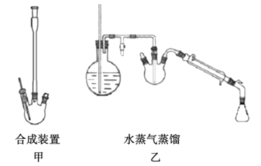
�ش���������:
��1���ϳ�ʱװ�ñ����Ǹ���ģ�������___________����Ӧ��ɺ��������20mLˮ��Ŀ����________��
��2����Ӧ��ɺ���������̼�����кͣ�Ŀ����_____��
��3������ڽ���ˮ��������ȥ��������______������жϴﵽ�����յ�__________��
��4���������̿���10- 15 min�����г��ȹ��ˣ�����Һ��ȴ�����£����ȹ��˵�Ŀ����_______��
��5������һ���ᴿ�ֲ�Ʒ��Ӧ�õIJ���������______����ʵ���Ʒ�IJ���Լ��_______��������С�����һλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��û�ѧ����ش��������⣺
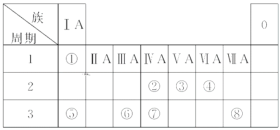
(1)��������Ԫ���У�����������ˮ����������ǿ�Ļ�����Ļ�ѧʽ��________(�ѧ���ţ���ͬ)������������ˮ���������ǿ�Ļ�����Ļ�ѧʽ��________������������ˮ���������Ե���������Ļ�ѧʽ��________��
(2)����ܵ���̬�⻯����ȶ����ɴ�С��˳����___________________��
(3)�ܡ��ݡ��ļ����Ӱ뾶�ɴ�С��˳���� ___________________��
(4)�ڡ��ۡ��ߵ���ۺ������������ǿ������˳����_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������Ҵ���ȡ��ϩ���õ�ʯ����Ҫ�ɷ�ΪCaC2��������CaS����ȡ��Ȳ��
��1��ʵ������ȡ��ϩ�Ļ�ѧ����ʽΪ_____________________________����������ȡ��ϩ�ķ���װ����_______����ѡ���ţ�

a b c d
��2���Ʊ���ϩ����ʱ�������¶ȹ��߶��۲쵽��Һ��ڣ�ͬʱ���ŵ��д̼�����ζ���������ɡ�����ϩ������Ʊ������У�Ũ����û�����ֵ�������________��
a ��ˮ�� b ��ˮ�� c ǿ������ d ����
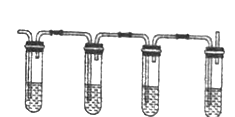
�� �� �� ��
��ͬѧ�������ʵ��ȷ�������������������ϩ�Ͷ�������
��ͼ����������������װ��ʢ�ŵ��Լ��ֱ��ǣ�������Ҫ����ѡ�����ţ���
��_______________����_______________����_______________����______________��
A Ʒ����Һ B NaOH��Һ C Ũ���� D ���Ը��������Һ
��3��ʵ�����Ʊ���Ȳ�Ļ�ѧ��Ӧ����ʽΪ_________________________________��ʵ��������ȲʱΪ�����ʯ��ˮ��Ӧ���ڼ��ң����÷�Һ©�����Ƶ����⣬ͨ��������_________����ˮ��Ϊ��ȥ��Ȳ�л��е������������ʣ��ɽ�����ͨ��___________��ѡ���ţ���
a����KMnO4��Һ b CCl4 c NaOH��Һ d CuSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪijƯ���Ľṹ����֪��W��Y��Z�Dz�ͬ���ڡ���ͬ����Ķ�����Ԫ�أ�W��Y��Zԭ������������֮�͵���Xԭ��������������W��X��Ӧ�ļ����Ӻ�������Ų���ͬ�����������������
![]()
A.W��X��Ӧ�ļ����ӵİ뾶��X>W
B.YԪ�������ڱ��е�λ��Ϊ�����ڵ�IVA��
C.��W���Ȼ����ˮ��Һ�������ɲ����տɵõ�W��������
D.��Ư���ṹ�У�Y��Xԭ�ӵ�����������8���ӽṹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ�����Ʊ�����������һϵ�����ʵ���װ��(�г��豸����)��
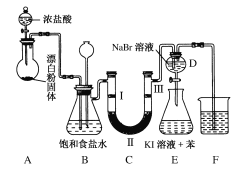
(1)װ��A�������ķ���װ�ã�����ʢ��Ũ���������������________����д���÷�Ӧ��Ӧ�Ļ�ѧ����ʽ�� ___________________________________��
(2)ʵ���ҳ������¼��ַ�����ȡ������
a.����������Ũ���ᷴӦ��������д���䷴Ӧ�����ӷ���ʽ______________��
b.�������Ũ���ᷴӦ���������÷�Ӧ�����������뻹ԭ��������ʵ���֮��Ϊ____��
(3)װ��B�б���ʳ��ˮ��������________��ͬʱװ��BҲ�ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������д����������ʱB�е�����____________________________��
(4)װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ�Ϊ��C�Т����η������ʵ����Ӧ��________(����ĸ���)��
��� | �� | �� | �� |
a | �������ɫ���� | ��ʯ�� | ʪ�����ɫ���� |
b | �������ɫ���� | ��ˮ����ͭ | ʪ�����ɫ���� |
c | ʪ�����ɫ���� | Ũ���� | �������ɫ���� |
d | ʪ�����ɫ���� | ��ˮ�Ȼ��� | �������ɫ���� |
(5)���װ��D��E��Ŀ���DZȽ��ȡ��塢�ⵥ�ʵ������ԡ���Ӧһ��ʱ���������װ��D��������Һ����װ��E�У����۲쵽��������________________��������________(������������������)˵���嵥�ʵ�������ǿ�ڵ⣬ԭ����_________________��
(6)װ��F��������_________�����ձ��е���Һ����ѡ�������е�________(����ĸ���)��
a.����NaOH��Һ b.����Ca(OH)2��Һ
c.����Na2SO3��Һ d.����Na2CO3��Һ
(7)��������Ư�ۣ��ⶨƯ����Ч�ɷֵ�������������ȡ1.000 gƯ������ƿ�У���ˮ�ܽ⣬������Һ��pH���Ե���Ϊָʾ������0.100 0 mol/LKI��Һ���еζ�����Һ�����ȶ�dz��ɫʱΪ�ζ��յ㡣��Ӧԭ��Ϊ��3ClO-+I-=3Cl-+IO3-��IO3-+5I-+3H2O=6OH-+3I2��ʵ�����������±���ʾ��
����� | 1 | 2 | 3 |
KI��Һ���/mL | 19.98 | 20.02 | 20.00 |
��Ư������Ч�ɷֵ���������Ϊ________�����ζ�������δ�������Һ���ֲ���dz��ɫʱ��ֹͣ�ζ�����ⶨ�����________(����ƫ������ƫ����������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˾����˶����ⷢ������Ϊ����������ȱ��ʱ�����Ƿ�����Ӧ���������ᣬ��ṹ��ʽΪ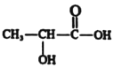 �����й��������˵����ȷ���ǣ� ��
�����й��������˵����ȷ���ǣ� ��
A.�����ϵͳ����Ϊ1-�ǻ�����
B.�����������ͬ�����ŵ�����ͬ���칹��(��������)��3��
C.����ȿɷ���ȡ����Ӧ����ȥ��Ӧ�ֿɷ����ӳɷ�Ӧ
D.���ᷢ�����۷�Ӧ�ķ���ʽΪn +nH2O
+nH2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ������ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ������ͼ��ʾװ��ʱ��ʵ�飺
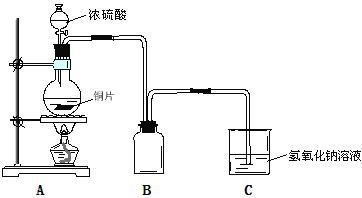

��1��B�������ռ�ʵ���в����������װ�ã�װ��ͼ������������ȷ����__________��

��2��ʵ��������ȡ6.4gͭƬ��12mL 18mol��L-1Ũ�������Բ����ƿ�й��ȣ�ֱ����Ӧ��ϣ��������ƿ�л���ͭƬʣ�࣬��С���е�ͬѧ��Ϊ����һ����������ʣ�ࡣ
�� ��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��_____________________________________��
�������Լ��У���֤����Ӧֹͣ����ƿ��������ʣ�����___________����д��ĸ��ţ���
A����������Һ | B��BaCl2��Һ | C������ | D��Na2CO3��Һ |
��Ϊʲô��һ����������ʣ�൫δ��ʹͭƬ��ȫ�ܽ⣿����Ϊԭ����__________________________��
��3��Ϊ��ȷ����Ӧ���ɵ���Ҫ����ɷ֣���������ʵ��װ��A��B֮�䲹��������ͼDװ�ã�����ϴ��ƿ�п���ʢ��__________���Լ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���W �ڹ�ҵ�ϳ������ܼ������ϣ���ϳɷ������£�
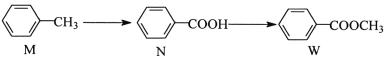
����˵����ȷ���ǣ�������
A. M��N��W ���ܷ����ӳɷ�Ӧ��ȡ����Ӧ
B. N��W ��������һ��CH2ԭ���ţ����Ի�Ϊͬϵ��
C. W �������࣬����ˮ��ͼ���ˮ�������ͬ
D. 1mol N����4mol H2�����ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com