
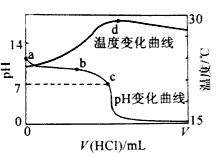
【题目】室温下,将1.000mol/L 盐酸滴入20.00mL1.000 mol/L 氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。
下列有关说法不正确的是( )
A. a 点由水电离出的c(H+)>1.0×10-14mol/L
B. b 点: c(NH4+)>c(Cl-)
C. c 点: c(Cl-)=c(NH4+)
D. d 点后,溶液温度略下降的主要原因是NH3·H2O 电离吸热
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】血液化验单中“葡萄糖”一项的结果为4.94×10﹣3 molL﹣1 . 这里的“4.94×10﹣3 molL﹣1”表示葡萄糖的( )
A.物质的量
B.摩尔质量
C.质量分数
D.物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.凡是放热反应的发生均无需加热B.物质发生化学反应都伴随着能量变化
C.凡是需要加热后才能发生的反应是吸热反应D.伴有能量变化的物质变化都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.Na+、Mg2+、Cl﹣、SO42﹣
B.Cu2+、Cl﹣、NO3﹣、OH﹣
C.Ca2+、Na+、CO32﹣、NO3﹣
D.K+、Fe3+、NO3﹣、SCN﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】初中阶段:物质得氧和失氧的反应是氧化还原反应;高中阶段:凡是有元素化合价升降的化学反应都是氧化还原反应。元素化合价升高的为还原剂,发生氧化反应;元素化合价降低的为氧化剂,发生还原反应;氧化反应和还原反应同时发生的,这样的反应称为氧化还原反应。请回答下列问题:
(1)根据化合价改变判断下列四种基本反应类型,一定不是氧化还原反应的是____。(选填宇母序号)
A.化合反应B.分解反应C.置换反应 D.复分解反应
(2)在化学反应Fe+CuSO4=Cu+FeSO4中,该反应的还原剂是_____(填化学式)。
(3)下列反应中,氧化反应与还原反应在同一元素中进行的是________。(多选,选填字母序号)
A.C12+2NaOH=NaCl+NaClO+H2OB.4P+5O2![]() 2P2O5
2P2O5
C.Zn+CuCl2=Cu+ZnCl2 D.3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量V2O5 及一定量Ag2SO4 固体置于恒容真空密闭容器,在一定温度下发生反应: Ag2SO4(s)![]() Ag2O(s) + SO3(g) 2SO3(g)
Ag2O(s) + SO3(g) 2SO3(g)![]() 2SO2(g) + O2(g),10min 后反应达平衡,此时c(SO3)=0.4mol/L,c(SO2)=0.1mol/L。下列说法中,不正确的是
2SO2(g) + O2(g),10min 后反应达平衡,此时c(SO3)=0.4mol/L,c(SO2)=0.1mol/L。下列说法中,不正确的是
A. 平衡时,容器内气体密度为40g/L。
B. 10min 内氧气的平均反应速率为0.005mol·(L·min)-1
C. 再加入少量AgSO4 固体,则反应均向正反应方向移动
D. 该温度下,2Ag2SO4(s)![]() 2Ag2O(s) +2SO2(g) +O2(g)的平衡常数为5×10-4
2Ag2O(s) +2SO2(g) +O2(g)的平衡常数为5×10-4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀有金属钌(Ru)的性质很稳定,耐腐蚀。实验室用H2还原RuO2来制备金属钌的装置如图所示。下列说法错误的是
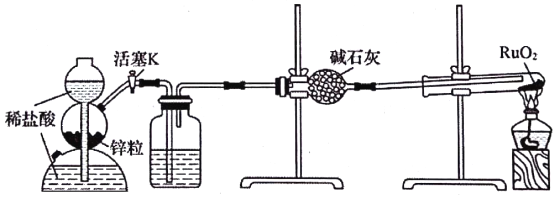
A. 加热RuO2前,应先收集气体并点燃,通过声音判断气体纯度
B. 洗气瓶中盛装的可能是NaOH溶液,用于除去挥发出来的HCl气体
C. 结束反应时,先停止加热,待试管冷却到室温后再关闭活塞K
D. 启普发生器也可用于碳酸钠晶体与稀硫酸反应制备二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种常见的食用香料。实验室由链状二烯烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为_______,D的化学名称是_______。
(2)③的反应方程式为_______。
(3)④的反应试剂和反应条件分别是_______,⑤的反应类型是_______。
(4)F中官能团名称为_______,G的分子式为_______。
(5)H是E的同分异构体,其分子中含有苯环,苯环上只有2个取代基且处于对位,遇氯化铁溶液显紫色,则H可能的结构有_______种。
(6)已知:①反应物分子的环外双键比环内双键更容易被氧化;
②RHC=CHR RCHO+RCHO(R、R代表烃基或氢原子)。写出由有机物A制备
RCHO+RCHO(R、R代表烃基或氢原子)。写出由有机物A制备 的合成路线:_____________(无机试剂任选)。
的合成路线:_____________(无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com