
| 酒化酶 |
| ||
| 酒化酶 |
| ||


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
| A、1L 0.1 mol?L-1的H2SO4溶液中粒子数为0.15NA |
| B、标准状况下,22.4L乙醇中含有的氧原子数为NA |
| C、1mol CO2分子中共用电子对数为2NA |
| D、23g Na与足量的O2完全反应,失去的电子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 |
| B、若金属全部溶解,则溶液中一定含有Fe3+ |
| C、溶液中可能只有Cu2+ |
| D、溶液中可能只有Fe2+ 和Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用标准氢氧化钠溶液滴定待测醋酸,选用酚酞作指示剂 |
| B、配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再加水稀释到所需的浓度 |
| C、测定某溶液的pH时,用pH试纸蘸取待测液,然后和比色卡对比得出pH |
| D、将淀粉溶液加到饱和食盐水中,检验食盐是否是加碘食盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
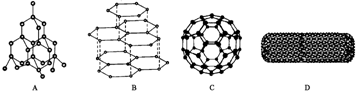
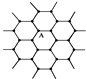 可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为
可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为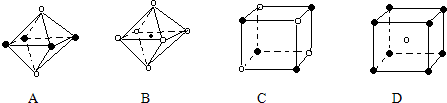
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com