
【题目】NA是阿伏加德罗常数的值。下列说法正确的是( )
A.常温常压下,11.2 L SO2含有的氧原子数小于NA
B.0. 1 mol Na2O2和Na2O的混合物中含有的离子总数等于0.4NA
C.10 g质量分数为34%的H2O2溶液含有的氢原子数为0.2NA
D.100 mL 0.1 mol/L醋酸中含有的醋酸分子数是0.01NA
【答案】A
【解析】
A.常温常压下,气体摩尔体积大于22.4 L/mol,故11.2 L二氧化硫的物质的量小于0.5 mol,则含有的氧原子个数小于NA,故A正确;
B.由Na2O2的电子式为![]() ,Na2O的电子式为
,Na2O的电子式为![]() 可知,1 mol Na2O中含3 mol离子,1 mol Na2O2中含3 mol离子,则0.1 mol Na2O和Na2O2混合物中离子为0.3 mol,即含有的阴、阳离子总数是0.3NA,故B错误;
可知,1 mol Na2O中含3 mol离子,1 mol Na2O2中含3 mol离子,则0.1 mol Na2O和Na2O2混合物中离子为0.3 mol,即含有的阴、阳离子总数是0.3NA,故B错误;
C.H2O2溶液中,除了H2O2,水也含氢原子,故10 g质量分数为34%的H2O2溶液中溶质的质量10 g×34%=3.4g,物质的量n=![]() =
=![]() =0.1mol,一个过氧化氢分子中含有两个氢原子,1mol过氧化氢分子中含有2mol氢原子,0.1mol过氧化氢分子中含有0.2mol氢原子,0.2mol氢原子个数等于0.2NA,水也含氢原子,氢原子的个数大于0.2NA,故C错误;
=0.1mol,一个过氧化氢分子中含有两个氢原子,1mol过氧化氢分子中含有2mol氢原子,0.1mol过氧化氢分子中含有0.2mol氢原子,0.2mol氢原子个数等于0.2NA,水也含氢原子,氢原子的个数大于0.2NA,故C错误;
D.醋酸为弱酸,在水中不完全电离,100 mL 0.1 mol/L醋酸的物质的量n=cV=0.1mol/L×0.1L=0.01mol,含有的醋酸分子数小于0.01NA,故D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】可逆反应![]() ,有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为
,有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为![]() ;在相同条件下,向乙容器中加入2molC达到平衡后吸收热量为
;在相同条件下,向乙容器中加入2molC达到平衡后吸收热量为![]() ,已知
,已知![]() 下列叙述正确的是
下列叙述正确的是![]()
A.甲中反应达到平衡时,![]()
B.达到平衡后,甲中C的体积分数比乙大
C.达到平衡后,再向乙中加入![]() 、
、![]() 、
、![]() ,平衡向生成C的方向移动
,平衡向生成C的方向移动
D.乙中的热化学反应方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2l恒温恒容容器中加入2molMgSO4并充入 2molCO,发生反应:MgSO4(s)+ CO(g)![]() MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是
MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是

A. 0 ~2min内平均反应速率v(SO2)= 0.3 mol·l-1 ·min-1
B. 2 ~4min内容器内气体的密度没有变化
C. 该温度下,反应的平衡常数为1.8
D. 保持其他条件不变,起始时向容器中充入1.00 mol MgSO4和1.00 molCO,反应达到平衡时,n(CO2)> 0.60 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示。下列说法正确的是

A. 石墨电极上发生氧化反应 B. 通甲烷的电极反应式:CH4+4CO32--8e-=5CO2+2H2O
C. 通空气的电极反应式为O2+4e-=2O2- D. 甲烷燃料电池中CO32-向空气一极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)基态Fe原子有______个未成对电子,Fe3+的电子排布式为______。可用硫氰化钾检验Fe3+,形成的配合物的颜色为______。
(2)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。1mol乙醛分子中含有的键的数目为______。乙醛中碳原子的杂化轨道类型为______,乙酸的沸点明显高于乙醛,其主要原因是______。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______个铜原子。
(3)Al单质为面心立方晶体,其晶胞边长a0.405nm,晶胞中铝原子的配位数为______。列式表示Al单质的密度______ gcm-3。(阿伏加德罗常数用NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法不正确的是( )
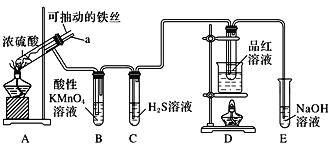
A.装置B中酸性KMnO4溶液逐渐褪色,体现了二氧化硫的还原性 |
B.实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的Fe3+ |
C.装置D中品红溶液褪色可以验证SO2的漂白性 |
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液由弱酸(HR)及其盐(NaR)组成,浓度均为1 molL-1,25℃时向该溶液通入HCl气体或滴入NaOH溶液,溶液pH随加入的H+或OH-的物质的量发生变化的情况如图。下列说法不正确的是
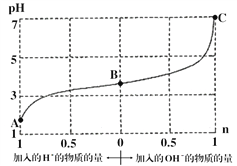
A. A、B、C三点所表示的溶液中水的电离程度依次增大
B. 加入1 mol NaOH后,溶液中c(Na+)=c(R-)
C. 通入HCl, R-的水解程度增大,HR的电离常数减小
D. 未加HCl和NaOH时,溶液中c(R-)>c(Na+)>c(HR)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五倍子是一种常见的中草药,其有效成分为X,在一定条件下X可分别转化为Y、Z。
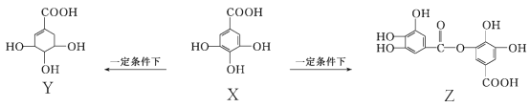
下列说法错误的是
A. 1 mol Z最多能与8 mol NaOH发生反应
B. 1 mol X与H2完全加成产物的分子式为C7H12O5
C. 向Y中滴加FeCl3溶液呈紫色
D. 1 mol Y与足量的金属钠反应放出2 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个绝热的恒容密闭容器中,可逆反应![]() 达到平衡状态的标志是( )
达到平衡状态的标志是( )
①![]() ②各组分的物质的量不变 ③体系的压强不再发生变化 ④混合气体的密度不变 ⑤体系的温度不再发生变化 ⑥
②各组分的物质的量不变 ③体系的压强不再发生变化 ④混合气体的密度不变 ⑤体系的温度不再发生变化 ⑥![]() ⑦3mol H-H键断裂的同时有2mol N-H键也断裂
⑦3mol H-H键断裂的同时有2mol N-H键也断裂
A.①②③⑤⑥B.②③④⑤⑥
C.②③⑤⑥D.②③④⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com