
【题目】CuSO4用途广泛,以Cu为原料制CuSO4有多种方法。
(1)实验室可用Cu与浓硫酸反应制CuSO4。
① Cu与浓硫酸反应的化学方程式是________。
② 该方法制CuSO4存在的不足是________(写出任意一条)。
(2)实验小组采取如下方法制CuSO4。

实验表明,Fe3+能加快生成CuSO4的反应速率,加快原理可表述为:
i. 2Fe3+ + Cu = 2Fe2+ + Cu2+
ii. ……
ii的离子方程式是________。
(3)用电解的方法制CuSO4,如图所示。

① 与直流电源a 端相连的电极材料是________(填“铜片”或“石墨”)。
② 将进口处较浓硫酸替换为Na2SO4溶液进行实验,发现得到的CuSO4溶液pH比替换前升高,结合化学用语解释pH升高的原因是________。
【答案】
(1)①Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
②反应产生SO2,对环境有污染或氧化剂浓硫酸利用率不高
(2)4Fe2++O2+4H+=4Fe3++2H2O;
(3)①铜片②替换为Na2SO4后,阴极区发生反应2H++2e-=H2↑,阴极区c(OH-)>c(H+),OH-也可以通过阴离子交换膜运动到阳极区,导致CuSO4溶液pH升高
【解析】
试题分析:(1)① Cu与浓硫酸反应的化学方程式为Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+2H2O,故答案为:Cu + 2H2SO4(浓)
CuSO4 + SO2↑+2H2O,故答案为:Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+2H2O;
CuSO4 + SO2↑+2H2O;
②该方法制CuSO4存在的不足有:反应中产生SO2,对环境有污染或氧化剂浓硫酸利用率不高,故答案为:反应中产生SO2,对环境有污染或氧化剂浓硫酸利用率不高;
(2)根据反应流程,Fe3+为催化剂,因此Fe3+能加快生成CuSO4的反应速率,加快原理可表述为:i. 2Fe3+ + Cu = 2Fe2+ + Cu2+;ii4Fe2+ + O2 + 4H+ =4Fe3+ + 2H2O,故答案为:4Fe2+ + O2 + 4H+ =4Fe3+ + 2H2O;
(3)①用电解的方法制CuSO4,铜电极需要与直流电源正极相连,根据硫酸根离子的移动方向,a为直流电源正极,因此与直流电源a 端相连的电极材料是铜片,故答案为:铜片;
② 替换为Na2SO4后,阴极区发生反应2H++2e-=H2↑,阴极区c(OH-)>c(H+),OH-也可以通过阴离子交换膜运动到阳极区,导致CuSO4溶液pH升高,故答案为:替换为Na2SO4后,阴极区发生反应2H++2e-=H2↑,阴极区c(OH-)>c(H+),OH-也可以通过阴离子交换膜运动到阳极区,导致CuSO4溶液pH升高;


科目:高中化学 来源: 题型:
【题目】碱式碳酸铜可用于有机催化剂、杀虫剂及饲料中铜的添加剂,还可用于烟火和颜料制造。CuSO4溶液与Na2CO3溶液反应能否得到碱式碳酸铜?某班同学进行相关探究。
【沉淀制备】
称取12.5 g胆矾溶于87.4 mL蒸馏水中,滴4滴稀硫酸,充分搅拌后得到CuSO4溶液。向其中加入适量Na2CO3溶液,将所得蓝绿色悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤。
(1)滴加稀硫酸的作用是 。所得硫酸铜溶液的溶质质量分数为 。
(2)用无水乙醇洗涤的目的是 。
【实验探究】
同学们设计了如下装置,用制得的蓝绿色固体进行实验:
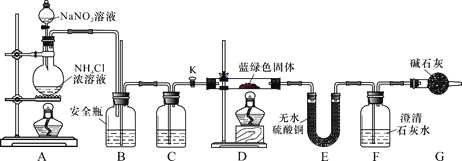
(3)D装置加热前,需要首先打开活塞K,用A装置制取适量N2,然后关闭K,点燃D处酒精灯。A中产生N2的作用是 ,C中盛装的试剂应是 。
(4)装置A中发生反应的离子方程式为 。
(5)若蓝绿色固体的组成为xCuCO3·yCu(OH)2,实验能观察到的现象是 。
(6)同学们查阅文献知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,经讨论认为需要用Ba(OH)2代替Ca(OH)2来定量测定蓝绿色固体的化学式,其原因是 。
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是 。若定量分析所取蓝绿色固体质量为27.1 g,装置F中使用Ba(OH)2溶液,实验结束后,装置E的质量增加2.7 g,F中产生沉淀19.7 g。则该蓝绿色固体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验氯化氢气体中是否混有Cl2,可采用的方法是( )
A. 用干燥的蓝色石蕊试纸
B. 用干燥有色布条
C. 将气体通入硝酸银溶液
D. 用湿润的淀粉碘化钾试纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关过氧化氢的叙述中不正确的是 ( )
A. 氧原子采取的是sp2杂化
B. 分子中有3个σ键
C. 过氧化氢是极性分子
D. 每个氧原子上有两个孤对电子对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在以离子键为主的化学键中常含有共价键的成分.下列各对原子形成化学键中共价键成分最少的是( )
A. Na,F B. Al,O C. Li,Cl D. Mg,S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
一种工业合成氨的简易流程图如下:
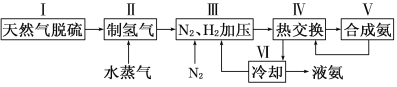
(1)在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应)当反应达到平衡时,N2和H2的浓度比是 。升高平衡体系的温度(保持体积不变),该反应 (填“逆向移动”正向移动”或“不移动”) 。
2NH3(g)(正反应为放热反应)当反应达到平衡时,N2和H2的浓度比是 。升高平衡体系的温度(保持体积不变),该反应 (填“逆向移动”正向移动”或“不移动”) 。
(2)氨水、氯水中均存在多种微粒和多个平衡,请写出氯水中存在的一个化学平衡反应的离子方程式 。
(3)步骤Ⅱ中制氢气原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是___________。
a.升高温度 b.增大压强
c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若2 mol CO和H2的混合气体(H2的体积分数为80%)与H2O反应,得到2.28mol CO、CO2和H2的混合气体,则CO转化率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来验证元素周期律.
用过氧化氢的水溶液和二氧化锰制备氧气,并将其通入到氢硫酸(H2S的水溶液)中.

(1)过氧化氢的电子式:_______________;
(2)从图1中选择氧气的制备装置______,反应前需要的操作是:________________;
(3)该实验如何证明O的非金属性强于S(用化学方程式表示)_____________;
(4)你认为能证明Cl的非金属性强于S的是___________
a.S在常温下为固体而Cl2为气体 b.H2S不如HCl稳定
c.H2SO3的酸性弱于HClO3 d.S与H2化合不如Cl2与H2化合剧烈
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com