
【题目】二氧化碳的回收利用对温室气体的减排具有重要的意义。在2L密闭容器中,加入2.00molCO2和2.0 mol H2以及催化剂发生反应:CO2(g)+H2 (g)![]() HCOOH(g) ΔH,测得,n(H2)/mol在不同温度随时间的变化如下表:
HCOOH(g) ΔH,测得,n(H2)/mol在不同温度随时间的变化如下表:
60 min | 90 min | 120 min | 150 min | 180 min | ||
实验I | Tl/K | 1.50 mol | 1.32 mol | 1.28 mol | 1.26 mol | 1.26 mol |
实验Ⅱ | T2/K | 1.45 mol | 1.20 mol | 1.10 mol | 1.10 mol | 1.10 mol |
(1)比较实验温度T1___T2(填“>”、“<”),该反应的ΔH___0(填“>”、“=”、“<”)。
(2)实验I中0~60 min内用HCOOH表示的该反应的平均反应速率为_____。
(3)实验Ⅱ反应开始时体系压强为P0,第90min时体系压强为Pl,则Pl∶P0=___。
(4)比较实验I、Ⅱ在80min时的逆反应速率大小vl___vⅡ(填“>”、“<”或“无法判断”),原因是_____。
【答案】< > 4.17×l0-3mol/(Lmin) 4∶5 < 80min时,实验Ⅱ反应的温度高,生成物HCOOH的浓度大,故实验Ⅱ的逆反应速率比实验I大
【解析】
(1)根据表格数据,反应速率越快,建立平衡需要的时间越少,结合温度对反应速率的影响分析判断;
(2)根据表格数据,首先计算实验I中0~60 min内用H2表示的反应速率,再根据方程式CO2(g)+H2 (g)![]() HCOOH(g),计算用HCOOH表示的反应速率;
HCOOH(g),计算用HCOOH表示的反应速率;
(3)同温同体积时,气体的压强之比等于物质的量之比,根据三段式分析解答;
(4)根据(1)的分析判断出T1、T2的大小,结合温度对反应速率的影响分析判断。
(1)根据表格数据,实验II建立平衡需要的时间较少,反应速率快,说明实验温度T1<T2;温度由T1变化为T2,即升高温度,平衡时n(H2)较少,说明平衡正向移动,因此正反应为吸热反应,ΔH>0,故答案为:<;>;
(2)根据表格数据,实验I中0~60 min内用H2表示的反应速率为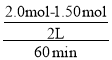 =4.17×l0-3mol/(Lmin),根据方程式CO2(g)+H2 (g)
=4.17×l0-3mol/(Lmin),根据方程式CO2(g)+H2 (g)![]() HCOOH(g),用HCOOH表示的反应速率与用H2表示的反应速率相等为4.17×l0-3mol/(Lmin),故答案为:4.17×l0-3mol/(Lmin);
HCOOH(g),用HCOOH表示的反应速率与用H2表示的反应速率相等为4.17×l0-3mol/(Lmin),故答案为:4.17×l0-3mol/(Lmin);
(3) CO2(g)+H2 (g)![]() HCOOH(g)
HCOOH(g)
起始(mol) 2 2 0
反应(mol) 0.8 0.8 0.8
90min(mol) 1.2 1.2 0.8
同温同体积时,气体的压强之比等于物质的量之比,实验Ⅱ反应开始时体系压强为P0,第90min时体系压强为Pl,则Pl∶P0=(1.2+1.2+0.8)mol∶(2+2)mol=4∶5,故答案为:4∶5;
(4)根据(1)的分析,T1<T2,实验Ⅱ反应的温度高,建立平衡之前,相同时间内生成物HCOOH的浓度大,故实验Ⅱ的逆反应速率比实验I大,故答案为:<;80min时,实验Ⅱ反应的温度高,生成物HCOOH的浓度大,故实验Ⅱ的逆反应速率比实验I大。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】由H、C、O、N、S、Cu等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价电子有____种运动状态,未成对电子占据原子轨道的形状为______。
(2)碳和氢形成的最简单碳正离子CH3+,其中心原子碳原子的杂化类型为___________,该阳离子的空间构型为___________。
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是_________________________________。
(4)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_____,离子反应方程式为____;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为___________,中心原子的配位数为___________。
(5)金属晶体铜的晶胞如图所示。其堆积模型是___________,铜原子间的最短距离为apm,密度为ρg·cm-3,NA为阿伏加德罗常数。铜的相对原子质量为___________(用a、ρ、NA表示,写出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)对于下列反应:2SO2 + O2 ![]() 2SO3 , 如果2min内SO2的浓度由8 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_____________。
2SO3 , 如果2min内SO2的浓度由8 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_____________。
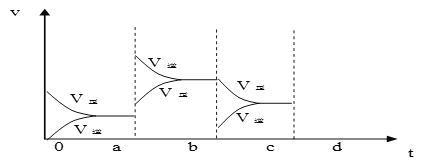
(2)下图表示在密闭容器中反应:2SO2+O2![]() 2SO3 ΔH<0 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是____________;b c过程中改变的条件可能是____________; 若增大压强时,反应速度变化情况画在c-d处__________.
2SO3 ΔH<0 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是____________;b c过程中改变的条件可能是____________; 若增大压强时,反应速度变化情况画在c-d处__________.
(3)对于下列电离平衡:NH3·H2O![]() NH4+ + OH -,能使c(NH4+)增大的措施是:_________
NH4+ + OH -,能使c(NH4+)增大的措施是:_________
①升高温度 ②加氨气 ③水 ④ NH4Cl溶液 ⑤NaOH溶液 ⑥适量的盐酸
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________;
(2)该反应为____________反应(选填吸热、放热);
(3)某温度下,平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为____________℃;
(4)830℃时,向该容器中加入1LCO2与1LH2,平衡时CO2的体积分数是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向仅含SO32-、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
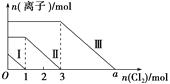
A.曲线Ⅱ代表Br-的变化情况
B.曲线Ⅰ对应的反应:SO32-+Cl2+H2O=2H++SO42-+2Cl-
C.通入的氯气为5 mol时,溶液中的主要阴离子为Cl-、SO32-
D.溶液中n(Na+)=n(SO32-)+n(I-)+n(Br-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1 mol/L二元弱酸H2A溶液中滴加0.1mol/LNaOH溶液,溶液中的H2A、HA-、A2 -的物质的量分数δ(x)随pH的变化如图所示。下列说法错误的是

A.pH =1.9时,c(Na+)<c(HA-)+2c(A2-)
B.当c(Na+)=c(H2A)+c(HA-)+c(A2-)时,溶液pH>7
C.pH=6时,c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.lg[Ka2(H2A)]=-7.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.0g铜与60.0mL一定浓度的硝酸发生如下反应:Cu+4HNO3 = Cu(NO3)2+2NO2↑+2H2O;3Cu+8HNO3 = 3Cu(NO3)2+2NO↑+4H2O。铜完全溶解产生的混合气体体积为8.96L(标况)。请计算(各数据保留两位有效数字):
(1)NO的体积为______
(2)该混合气体的平均摩尔质量约为______
(3)待产生的气体全部释放后,向溶液加入100mL 2.0mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,金属单质X和非金属单质Y能够反应,生成化合物Z,Z能与水发生水解反应生成气体G和白色沉淀P(如下框图所示),已知气体G与空气之密度比约为1.17。请填空:
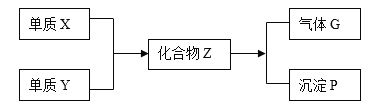
(1)组成单质X和Y的元素分别属第____________族和第___________族;
(2)Z与水发生水解反应方程式_____________________;
(3)每生成1mol的化合物Z,反应中转移_________________mol的电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的制备、性质、收集说法正确的是( )
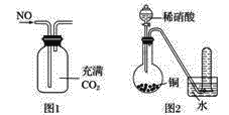
A.汽车尾气中有NOx,主要是汽车打火时氮气和氧气反应引起的
B.可以用图1所示装置收集到干燥的NO气体
C.根据图2装置收集到的气体为无色能够验证铜和稀硝酸反应的产物中气态物质只有NO
D.可以用湿润的淀粉碘化钾试纸鉴别红棕色气体NO2和溴蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的是( )
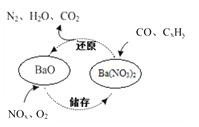
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1mol N2,转移电子数为1 mol
D.三效催化剂能有效实现汽车尾气中CO、CxHy、NOx三种成分的净化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com