
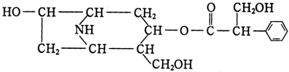
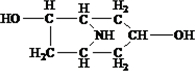
 和
和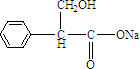 ,C含苯环是芳香化合物,应为
,C含苯环是芳香化合物,应为 ;
; 用稀盐酸酸化得到
用稀盐酸酸化得到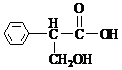 ;
; 和
和 ,C中含苯环是芳香化合物,应为
,C中含苯环是芳香化合物,应为 ,则B为
,则B为 ,
, ;
; 用稀盐酸酸化得到E为
用稀盐酸酸化得到E为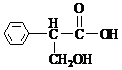 ,故E的结构简式是
,故E的结构简式是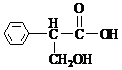 ,
,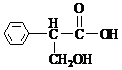 ;
;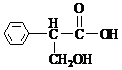 +O2
+O2| Cu |
| △ |
 +2H2O,
+2H2O, +O2
+O2| Cu |
| △ |
 +2H2O.
+2H2O.


科目:高中化学 来源: 题型:
| A、绿色荧光蛋白质(GFP)是高分子化合物,不可降解,其水溶液有丁达尔效应 |
| B、天宫一号使用的碳纤维是一种新型有机高分子材料 |
| C、顺丁橡胶、腈纶、涤纶和“人造棉花”都属于合成纤维 |
| D、因为氨易液化,液氨在气化时会吸收大量的热量,所以液氨可作制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:r(A)>r(B)>r(D)>r(C) |
| B、单质的还原性:A>B>D>C |
| C、离子半径:r(C3-)>r(D-)>r(B+)>r(A2+) |
| D、原子序数:d>c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,15g甲基(-14CH3)所含的电子数为9NA |
| B、常温下,2L pH=12的Na2CO3溶液中含有的OH-数目为0.02NA |
| C、6.8g液态KHSO4中含有0.1NA个阳离子 |
| D、1mol乙酸和1mol乙醇充分反应生成的水分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 【化学一选修3:物质结构与性质】
【化学一选修3:物质结构与性质】| 元素 | X | Y | Z |
| 电负性 | 1.5 | 1.2 | 1.8 |
| 第一电离能(kJ/mol) | 578 | 738 | 787 |
| 第二电离能(kJ/mol) | 1817 | 1451 | 1577 |
| 第三电离能(kJ/mol) | 2745 | 7733 | 3232 |
| 第四电离能(kJ/mol) | 11575 | 10540 | 4355 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com