
����Ŀ����������������ǣ� ��
A.��NH4Cl������Һ�м������þ���Եõ���������
B.pH=12 Ba(OH)2��Һ��c(OH-)��0.001 mol/L NaOH��Һc(OH-)��10��
C.�����£�CH3COONa��CH3COOH�Ļ����Һ��(pH=7)��c(Na+)=c(CH3COO-)��c(CH3COOH)��c(H+)=c(OH-)
D.�����£�Cd(OH)2��Co(OH)2�Ļ������Һ�У�c(Cd2+)��c(Co2+)��4������֪��Ksp[Cd(OH)2]=7.2��10-15��Ksp[Co(OH)2]=1.8��10-15
���𰸡�B
��������
A����NH4Cl������Һ�м������þ��þ��笠�����ˮ�����ɵ������ӷ�Ӧ�����������ٽ���笠����ӵ�ˮ�⣬笠�����ˮ�������һˮ�ϰ��ֽ����������ˮ�����ͬʱ�����ɰ�����A��ȷ��
B��û�и����¶ȣ���pH=12 Ba(OH)2��Һ�е�����������Ũ�Ȳ�һ��Ϊ0.01 mol/L�����ж�����Һ�е�����������Ũ�ȴ�С��B����
C�������£�CH3COONa��CH3COOH�Ļ����Һ��(pH=7)����c(H+)=c(OH-)����ϵ���غ�ɵã�c(Na+)=c(CH3COO-)��CH3COONa��ǿ����ʣ�����Һ����ȫ����Ϊ���ӣ�CH3COOHΪ������ʣ���Ҫ�Ե���ʷ��Ӵ��ڣ�ˮ�Ǽ����ĵ���ʣ����������H+��OH-Ũ�Ⱥ�С������Һ������Ũ�ȴ�СΪ��c(Na+)=c(CH3COO-)��c(CH3COOH)��c(H+)=c(OH-)��C��ȷ��
D�������£�Cd(OH)2��Co(OH)2�Ļ������Һ������������Ũ����ͬ��c(Cd2+)��c(Co2+)��֮�������ܶȻ�֮�����=![]() =4��D��ȷ��
=4��D��ȷ��
�ʺ���ѡ����B��


 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У���Ӧ�������Լ����ͻ���۶���ȷ�����߾��������ϵ����
ѡ�� | ʵ�� | ���� | ���ͻ���� |
A | ��������Ũ�����м�����Ƭ��һ��ʱ������ͭ�� | ���������ɣ���Һ������ɫ | Ũ���ὫFe����Ϊ |
B | �ֱ��� | ���а�ɫ�������� | �����ԣ� |
C | �����ڵ��������ݵ�ʢ��ʳ��ˮ�����������У����������Ӵ� | ������ù������� | ����ԭ��أ����������������õ��ӱ���ԭ�ɵ����� |
D | �� | ��ɫ������Ϊdz��ɫ |
|
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���������ÿ�����þ��Ϊԭ�ϣ���ȡ��������þ(Mg3N2)����֪��һ�����п��ܷ������з�Ӧ��
��2Mg+O2![]() 2MgO ��3Mg+N2
2MgO ��3Mg+N2![]() Mg3N2
Mg3N2
��2Mg+CO2![]() 2MgO+C��Mg+H2O(����)=MgO+H2
2MgO+C��Mg+H2O(����)=MgO+H2
��Mg3N2+6H2O=3Mg(OH)2+2NH3�ɹ�ѡ���������ҩƷ����ͼ��ʾ���Ҽ�����ȷ����ʱ��װ�����������ķ�Ӧ����ȫ�ġ�
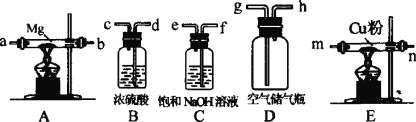
�Իش��������⣺
(1)ʵ�鿪ʼʱ���ȵ�ȼ________װ���еľƾ��ƣ�ԭ����________���ٽ���g���ӵ�����ˮ��ͷ���γ���h�������������������������������ĵ���Ϊ(����ĸ����)��h��________��
(2)���Ƿ�ѡ����Bװ�ã�������ʲô________________________ ��
(3)���Ƿ�ѡ����Cװ�ã�������ʲô________________________��
(4)���ͬʱ��ȼA��Eװ�õľƾ��ƣ���ʵ����������Ӱ��________ Ϊʲô___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.Ksp(AB2)С��Ksp(CD)��˵��AB2���ܽ��һ��С��CD���ܽ��
B.������Ԫ���⣬������Ԫ�ص�����ϼ�����ֵ�϶����ڸ�Ԫ��������������
C.2C+SiO2![]() Si+2CO�����˷�Ӧ�ܹ���������Ϊ̼�Ļ�ԭ�Աȹ�ǿ
Si+2CO�����˷�Ӧ�ܹ���������Ϊ̼�Ļ�ԭ�Աȹ�ǿ
D.����Ҳ����ͨ�����ֽⷴӦ��ǿ�ᣬ�磺H2S+CuSO4=H2SO4+CuS��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ,��Ca(OH)2��CaWO4(�����)�ij����ܽ�ƽ��������ͼ��ʾ(��֪![]() =0.58)�����з�������ȷ����
=0.58)�����з�������ȷ����

A. a���ʾCa(OH)2��CaWO4��δ�ﵽ�ܽ�ƽ��״̬
B. ����Ca(OH)2��Һ�ͱ���CaWO4��Һ��������: c(OH-)>c(H+)>c(Ca2+)>c(WO42-)
C. ����Ca(OH)2��Һ�м�������Na2O����Һ�����
D. ʯ������0.1mol/LNa2WO4��Һ��Ϻ�����Ӧ:Ca(OH)2+WO42-=CaWO4+2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ɰ�����������г��� Karl Fischer���Dzⶨ������ˮ�������÷���������I2��SO2��Ӧ��������ˮ��Ϊԭ��(���������������ɷֲ��μӷ�Ӧ)���ݴ˻ش��������⣺
(1)д���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��_______________________��
����I����Ӧ��Ʒ�е�ˮ
��ͼ��ijͬѧ��ʵ����ģ��Karl Fischer����ʵ��װ��ͼ��
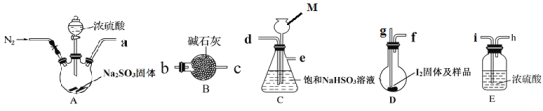
(2)װ�����ӵ�˳��Ϊa��____________(��ӿ���ĸ˳��)��M����������Ϊ________________������ʵ������е������ǣ�____________��
(3)��������Ϊ��������װ�ò����װ�������ԣ���װ��ҩƷ��____________________���۹رյ��ɼУ���Һ©���������ܷ�Ӧ�����رշ�Һ©������������ͨ��N2����ȡ��Dװ�ã�������
������м���ͨ��N2��Ŀ����________________________________
���� II���ⶨʣ��ĵ�
��Ӧ���Dװ�ü�������ˮ�����ˣ����ϴ�ӣ����ϲ�ϴ��Һ����Һ���������250.00mL��Һ��ȡ25.00mL��0.20mol��L-1 Na2S2O3��Һ�ζ�ʣ���I2���ʣ���֪��Ӧ���£�2S2O32��+I2=S4O62��+2I����
(4)Na2S2O3��ҺӦװ��_____________(������ʽ��������ʽ��)�ζ����У����������У��ϲ�ϴ��Һ����Һ��Ŀ����__________________________��
(5)�ζ�ʵ���ظ��Ĵεõ���������:
ʵ�� | �� | �� | �� | �� |
���ĵı�Һ�����/mL | 18.37 | 20.05 | 19.95 | 20.00 |
����ʵ�鿪ʼʱ����Dװ���м���10.00 g������Ʒ��10.16��I2(��֪I2����)������Ʒ������ˮ�ĺ���Ϊ_________%��
����Na2S2O3��Һ�Ѳ����������ʣ���ˮ�����ⶨ�����____________(����ƫ�������� ƫ��������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ϴ���(��ZnO��CuO��Fe2O3��ʯī��MnO2��)�л��ս�������ȡ��������п�Ĺ�����������(��֪��Zn������������������������Al������Ӧ��������������)��

��1���ϴ�������������Ŀ����____________________________________________��
��2����������ʱMn2+�����������ӷ���ʽΪ_________________________________��
��3�����к͡�������ʱ����pH���ߣ����ʽ̼��п�IJ���ƫС��д���䷴Ӧ�����ӷ���ʽ(��дһ������)��____________________________________________��
��4���������ͭ������ͭ������������ʵ�鲽�����£�
I.ȷ��ȡ��ͭ��mg���������������H2O2��Һʹ����ȫ�ܽ⡣
��.����Һ���1~2min����ȥ������H2O2��
��.�������ڱμ��ų�Fe3+�ĸ��š�Ȼ������Թ�����KI��Һ(��Ӧ��2Cu2++4I��=2CuI��+I2)���ټ��뼸�ε�����Һ��ָʾ������ c mol ��L��1Na2S2O3����Һ�ζ�����ɫ��ʧ(I2+2S2O32��=2I��+S4O62��)�Ұ�����ڲ���ɫ��������Na2S2O3����ҺVmL��
��ͭ����������Ϊ______________________��
��ȱ�ٲ��������ʹ��õ�ͭ����������___________(����ƫ��������ƫС��������������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�����ֲ�����������������Ľ�������ʮ����Ҫ�����á���ش��������}��
��1�����־�����������ο�ѧ�ķ���Ϊ_________________________________��
��2������Bԭ�ӻ�̬�ļ۲�����Ų�ͼ����ȷ����___________
A. B.
B.
C. D.
D.
��3��NaBH4����Ҫ�Ĵ������壬�����ӵ����幹��Ϊ___________��
��4������������(�ṹ����ͼ1��ʾ)��___________����(�������Ǽ���)��
��5��ͼ2��ʾ����������ӵ�һ����������ʽ�ṹ���仯ѧʽ�ɱ�ʾΪ___________��

��6�����ᾧ����Ƭ��ṹ������һ��Ľṹ��ͼ3��ʾ����������ˮ���ܽ�Ⱥ�С��������ˮ�нϴ�ԭ����_________________________________��
��7������������(BN)������ǿ����ĥ���ϣ�����Ϊ��������ı����㣬�侧���ṹ(����ͼ)����ʯ���ơ���֪�þ����ܶ�Ϊag/cm3������������Nԭ�Ӽ����С����Ϊ___________pm��(�ú�a�Ĵ���ʽ��ʾ��NA��ʾ�����ӵ�����)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪25 ��ʱ��Ksp(AgCl)��1.8��10��10��Ksp(AgI)��8.5��10��17����ش��������⣺
��25��ʱ������50 mL 0.018 mol��L��1��AgNO3��Һ�м���50 mL 0.020 mol��L��1�����ᣬ��Ϻ���Һ�е�c(Ag��)Ϊ________ mol��L��1��pHΪ________��
��25��ʱ��ȡһ��������I����Cl������Һ�������еμ�AgNO3��Һ����AgCl��AgIͬʱ����ʱ����Һ��![]() Ϊ________��
Ϊ________��
��֪��2CrO42����2H��![]() Cr2O
Cr2O![]() ��H2O��25 ��ʱ��Ksp(Ag2CrO4)��9.0��10��12��Ksp(Ag2Cr2O7)��2.0��10��7����Na2Cr2O7��Һ�м���AgNO3��Һ������ֻ����һ��ש��ɫ�������ó����Ļ�ѧʽ��__________��
��H2O��25 ��ʱ��Ksp(Ag2CrO4)��9.0��10��12��Ksp(Ag2Cr2O7)��2.0��10��7����Na2Cr2O7��Һ�м���AgNO3��Һ������ֻ����һ��ש��ɫ�������ó����Ļ�ѧʽ��__________��
��3����֪��25 ��ʱKsp(Ag2CrO4)��9.0��10��12��Ksp(AgCl)��1.8��10��10��˵��Ag2CrO4���ܽ��________(����ڡ���С�ڡ����ڡ�)AgCl�ġ�
��4��25 ��ʱ��Mg(OH)2������Һ________(��ܡ����ܡ�)ʹʯ����Һ����ɫ��(��֪Ksp[Mg(OH)2]��4.0��10��12��lg 5��0.7)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com