
【题目】汽车尾气中含有CO、NO、NO2等多种污染物。
(1)在汽车的排气管上装一个催化转换装置,能使CO和NO反应生成无污染的气体,写出该反应的化学方程式_____
(2)研究表明:增大催化剂(相同质量下比较)比表面积可提高化学反应速率,为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某科研小组设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验编号 | T/℃ | CO 初始浓度/mol·L-1 | NO 初始浓度/mol·L-1 | 催化剂的比表面积/m·g-1 |
Ⅰ | 300 | 4.5×10-3 | 1.5×10-3 | 100 |
Ⅱ | ______ | 4.5×10-3 | 1.5×10-3 | 200 |
Ⅲ | 500 | 4.5×10-3 | _________ | 200 |
请在上表格中填入剩余的实验条件数据,三组实验中的反应速率由快到慢的顺序为 ______(填实验编号)
(3)大众"检测门"事件让"尿素可用于汽车尾气脱氮”又科普了一把,其反应原理为:NO+NO2+H2O=2HNO2
2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O
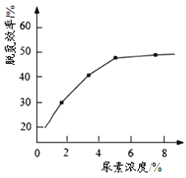
① 图为尿素含量对脱氮效率的影响,一般选择尿素浓度约5%左右,其原因是_______
②当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO):V(NO2)=3:1时,可通入一定量的空气,同温同压下,V(空气):V(NO2)=_____(空气中氧气的体积含量大约为 20%)
【答案】2CO+2NO ![]() 2CO2+N2 300 1.5×10-3 Ⅲ>Ⅱ>Ⅰ 浓度大于 5%后,脱氮效率不再明显提高,选择 5%的浓度,可以在保证脱氮效率的前提下节 约生产成本 5:2
2CO2+N2 300 1.5×10-3 Ⅲ>Ⅱ>Ⅰ 浓度大于 5%后,脱氮效率不再明显提高,选择 5%的浓度,可以在保证脱氮效率的前提下节 约生产成本 5:2
【解析】
(1)汽车尾气催化转换装置,能使CO和NO反应生成N2和CO2,由此可写出该反应的化学方程式。
(2)实验的目的是研究温度、催化剂比表面积对化学反应速率的影响规律,若研究温度对化学反应速率的影响规律,则只有温度变化,其它数据不变;当研究催化剂比表面积对化学反应速率的影响规律,则只有催化剂的比表面积改变,其它数据不变,由此可得出结论。
比较三组实验中的反应速率由快到慢的顺序时,温度越高,反应速率越快;催化剂的比表面积越大,反应速率越快。
(3)①分析选择尿素浓度约5%左右时,借助图中信息,从尿素浓度为5%、大于5%两个方面,分析对脱氮效率、成本的影响,从而找出原因。
②从反应方程式看,V(NO):V(NO2)=1:1时,汽车尾气脱氮效果最好,由此可利用反应2NO+O2==2NO2,计算所需O2与NO2的体积关系,从而求出同温同压下,V(空气):V(NO2)。
(1)汽车尾气催化转换装置,能使CO和NO反应生成N2和CO2,反应的化学方程式为2NO+2CO![]() N2+2CO2。答案为:2NO+2CO
N2+2CO2。答案为:2NO+2CO![]() N2+2CO2;
N2+2CO2;
(2)从表中可以看出,Ⅰ、Ⅱ两组实验中,催化剂的比表面积不同,则其它数据应相同,由此得出实验Ⅱ的温度应为300℃;Ⅱ、Ⅲ两组实验相比,温度不同,则NO的浓度应相同,应为1.5×10-3mol/L;实验Ⅱ的催化剂的比表面积大于实验Ⅰ,则反应速率Ⅱ>Ⅰ,实验Ⅲ的温度高于实验Ⅱ,则反应速率Ⅲ>Ⅱ,所以Ⅲ>Ⅱ>Ⅰ。答案为:300;1.5×10-3;Ⅲ>Ⅱ>Ⅰ;
(3)①图中信息显示,尿素浓度为5%时,脱氮效率基本达到最高点,且增大尿素浓度,虽然脱氮效率有所增大,但增大幅度很少,且会提高脱氮成本,所以选择5%,其原因是浓度大于5%后,脱氮效率不再明显提高,选择5%的浓度,可以在保证脱氮效率的前提下节约生产成本。答案为:浓度大于5%后,脱氮效率不再明显提高,选择5%的浓度,可以在保证脱氮效率的前提下节约生产成本;
②从反应方程式看,V(NO):V(NO2)=1:1时,汽车尾气脱氮效果最好。若烟气中V(NO):V(NO2)=3:1时,通入空气发生反应2NO+O2==2NO2,则所需O2与NO2的体积关系为1:2,从而求出同温同压下,V(空气):V(NO2)=![]() :2=5:2。答案为:5:2。
:2=5:2。答案为:5:2。


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数,下列说法正确的是
A. 1molCS2分子中含有1NA个π键
B. 31g白磷(P4)分子中所含的共价键数目为1NA
C. 电解精炼铜时,若阳极质量减少64g,则阴极转移的电子数目一定为2NA
D. 在1mol[Cu(H2O)4]2+中含有12NA个![]() 键
键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关性质的比较,不能用元素周期律解释的是
A.酸性:![]()
B.热稳定性:Na2 CO3![]() NaHCO3
NaHCO3
C.与水反应的速率:Na![]() Mg
Mg
D.非金属性:Cl![]() Br
Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)具有强还原性,可用作火箭燃料、抗氧剂等。
(1)肼可以由氨气反应制得,已知部分化学键键能如下表所示:
化学键 | H-H | N≡N | N-H |
键能/kJ·mol-1 | a | b | c |
工业上合成氨的反应 N2(g)+3H2(g) 2NH3(g) ΔH=_____kJ·mol-1.
(2)肼—空气燃料电池是一种环保型燃料电池,结构如图 1 所示
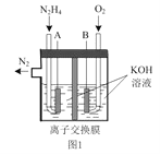
①肼—空气燃料电池的负极反应式为_____
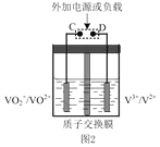
②全钒液流可充电电池结构如图 2 所示,将肼—空气燃料电池的 A 极与全钒液流可充电电池的 C 极相连,B 极与 D 极相连,写出阴极的电极反应____
(3)肼可用于处理高压锅炉水中的氧,防止锅炉被腐蚀,与使用 Na2SO3 处理水中溶解的 O2 相比,肼的优点是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用反应Cr2O7n-+CH3OH+H+→Cr3++CO2↑+H2O(未配平)来测定工业甲醇中甲醇的含量,下列说法中正确的是( )
A. 溶液的颜色从灰绿色变为橙色
B. Cr2O7n-发生氧化反应
C. 若配平后Cr3+和CO2的化学计量数比为2:1,则Cr2O7n-中的n=2
D. 若有3.2 g CH3OH参加反应,则转移的电子数为6.02×1022
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石与石墨是同素异形体。100 kPa时,1 mol石墨转化为金刚石的能量变化如图所示,下列说法正确的是

A.石墨转化为金刚石的反应为放热反应
B.石墨比金刚石更稳定
C.金刚石比石墨更稳定
D.破坏1 mol石墨的化学键所吸收的能量小于形成1 mol金刚石的化学键所放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下离子中的若干种:NH4+、Ba2+、Fe2+、Cl-、NO3-、CO32- 、SO42-.某同学收集了该地区的雾霾,经必要的预处理后得到试样溶液,设计并完成如下实验:

试回答下列问题:
(1)实验①中加入稀盐酸后,有无色气体A生成,溶液B依然澄清,且溶液中阴离子种类不变,据此可知原溶液中一定不含__________。(填离子符号)
(2)实验①中发生反应的离子方程式为__________________________________________。
(3)实验②中逐滴加入碳酸氢钠溶液,立即有气泡产生,一段时间后又有沉淀出现,这时的离子方程式为_______________________________________________ 。
(4)气体F的成分为______________。(填化学式)
(5)根据实验③现象该同学认为原溶液中一定含有SO42-,有其他同学认为其结论不合理,又进行了后续实验 ④,最终确认原溶液中含有SO42-,试写出实验④可行的操作方法及现象________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为( )
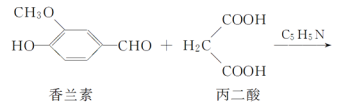

下列说法不正确的是( )
A. 不可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、氧化反应
D. 香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com