

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Al(OH)3 | Zn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 5.4 | 4.0 | 6.5 |
| 完全沉淀 | 3.7 | 9.6 | 6.4 | 5.2 | 8.0 |
| c(Fe2-) |
| c(Cu2-) |
| C(Fe2+) |
| C(Cu2+) |
| KSP(Fe(OH)2) |
| KSP(Cu(OH)2) |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、用NaOH除去溴苯中混有的溴杂质 |
| B、淀粉与稀H2S04充分反应后,加入适量新制Cu(OH)2溶液,加热产生红色沉淀 |
| C、只用一种试剂鉴别Na2S溶液、NaCl溶液、Na2SiO3溶液、Na2C03溶液 |
| D、用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
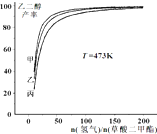 发展“碳一化学”,开发利用我国相对丰富的煤炭资源具有重要的战略意义和经济价值.以下是以焦炭为原料,经“碳一化学”途径制取乙二醇的过程:
发展“碳一化学”,开发利用我国相对丰富的煤炭资源具有重要的战略意义和经济价值.以下是以焦炭为原料,经“碳一化学”途径制取乙二醇的过程:| 水蒸气 |
| 高温 |
| 氧化偶联 |
| 催化还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com