
【题目】工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示:

已知:①菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。
②Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③焙烧过程中主要反应为MnCO3+2NH4Cl![]() MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。


(1)结合图1、2、3,分析焙烧过程中最佳的焙烧温度、![]() 、焙烧时间依次分别为_____、_____、_____。
、焙烧时间依次分别为_____、_____、_____。
(2)浸出液“净化除杂”过程如图:

①已知几种氧化剂氧化能力的强弱顺序为:H2O2>Cl2>MnO2>Fe3+,则氧化剂X宜选择__(填字母)。
A.H2O2 B.Cl2 C.MnO2
②调节pH时,pH可取的范围为______。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为____。
(4)上述流程中可循环使用的物质是_____。
【答案】500℃ 1.10 60min C 4.7≤pH<8.1 Mn2++2HCO3-=MnCO3↓+CO2↑+H2O NH4Cl
【解析】
根据流程:将菱镁矿粉(主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素)与氯化铵混合研磨后焙烧:MnCO3+2NH4Cl![]() MnCl2+2NH3↑+CO2↑+H2O,浸出,浸出液含有Mn2+、Fe2+、Al3+、Ca2+、Mg2+,加入MnO2将Fe2+氧化为Fe3+:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,然后调节溶液pH范围4.7≤pH<8.1使Fe3+,A13+沉淀完全,再加入NH4F沉淀Ca2+、Mg2+,过滤除去Fe(OH)3、Al(OH)3、CaF2、MgF2,净化液的成分主要含有MnCl2,加入碳酸氢铵碳化结晶,发生反应:Mn2++2HCO3-
MnCl2+2NH3↑+CO2↑+H2O,浸出,浸出液含有Mn2+、Fe2+、Al3+、Ca2+、Mg2+,加入MnO2将Fe2+氧化为Fe3+:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,然后调节溶液pH范围4.7≤pH<8.1使Fe3+,A13+沉淀完全,再加入NH4F沉淀Ca2+、Mg2+,过滤除去Fe(OH)3、Al(OH)3、CaF2、MgF2,净化液的成分主要含有MnCl2,加入碳酸氢铵碳化结晶,发生反应:Mn2++2HCO3-![]() MnCO3↓+CO2↑+H2O,过滤,得到MnCO3产品和滤液NH4Cl,将滤液NH4Cl蒸发结晶得到NH4Cl晶体可循环使用,据此分析作答。
MnCO3↓+CO2↑+H2O,过滤,得到MnCO3产品和滤液NH4Cl,将滤液NH4Cl蒸发结晶得到NH4Cl晶体可循环使用,据此分析作答。
(1)由图可知,锰的浸出率随着焙烧温度、氯化铵与菱镁矿粉的质量之比、焙烧时间增大而提高,到500℃、1.10、60min达到最高,再增大锰的浸出率变化不明显,故氯化铵焙烧菱镁矿的最佳条件是焙烧温度500℃,氯化铵与菱镁矿粉的质量之比为1.10,焙烧时间为60min;
(2)①对浸出液净化除杂时,需要将Fe2+转化为Fe3+,根据氧化剂氧化能力的强弱顺序为H2O2>Cl2>MnO2>Fe3+,则应选择加入MnO2将Fe2+转化为Fe3+,而不能用H2O2或Cl2,因为H2O2或Cl2除能氧化Fe2+,还能氧化Mn2+,故答案为C;
②已知:Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1,调节溶液pH使Fe3+,A13+沉淀完全,同时不使Mn2+沉淀,故pH范围为:4.7≤pH<8.1;
(3)净化液的成分主要含有MnCl2,碳化结晶时,发生反应的离子方程式为Mn2++2HCO3-![]() MnCO3↓+CO2↑+H2O;
MnCO3↓+CO2↑+H2O;
(4)根据分析和流程可知,可以循环使用的固体物质是NH4Cl。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是
A. 标准状况下,30.8gCCl4中所含的原子数为NA
B. 100g46%乙醇溶液中含有的H-O键的数目为NA
C. 1molNa2O2与足量的CO2充分反应,转移的电子数为NA
D. n(H2SO3)+n(HSO3-)=1mol的NaHSO3溶液中,含有Na+的数目大于NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应A(s)+ 3B(g)![]() 2C(g)+ D(g)来说,下列反应速率最快的是
2C(g)+ D(g)来说,下列反应速率最快的是
A. v(A)=0.3 mol/(Ls) B. v(B)=0.6 mol/(Lmin)
C. v(C)=0.5 mol/(Lmin) D. v(D)=0.01 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
A.常温常压下,14g有N2与CO组成的混合气体含有的原子数目为NA个
B.0.5molO3与11.2LO2所含的分子数一定相等
C.10gCaCO3和KHCO3的固体混合物含有0.1NA个阳离子
D.用16.25gFeCl3制备Fe(OH)3胶体,Fe(OH)3胶体粒子数小于0.1NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。
请用序号填空:
(1)上述状态下可导电的是___。
(2)属于电解质的是___。
(3)属于非电解质的是___。
(4)②在水溶液中的电离方程式为___,①与②以物质的量之比为1:2在溶液中反应的离子方程式为___。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,还原产物是___(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A~F之间的转化关系如下图所示(部分产物已略去),其中B的相对分子质量是D的2倍。
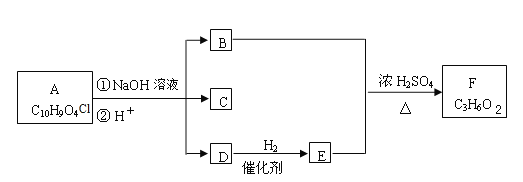
提示:![]() 会自动脱水形成R—CHO。
会自动脱水形成R—CHO。
根据以上信息回答下列问题:
(1)B的分子式是________________。
(2)检验D中官能团可使用的试剂名称是_________,写出D的相邻同系物与该试剂反应的化学方程式_______________________________。
(3)C遇FeCl3溶液显紫色,核磁共振氢谱中有四个峰,其峰面积比为1:2:2:1。写出C的结构简式_______________________。
(4)写出符合下列条件的C的同分异构体的结构简式_______、______、______、________。
①苯环上存在对位取代基;②遇FeCl3溶液显紫色;③能与银氨溶液反应。
(5)写出A的结构简式__________________________。
(6)若1molA和足量NaOH反应,最多能消耗___________mol NaOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应Fe(s)+CO2(g)![]() FeO(s)+CO(g),在温度为973 K时,平衡常数K=1.47,在1 173 K时,K=2.15。
FeO(s)+CO(g),在温度为973 K时,平衡常数K=1.47,在1 173 K时,K=2.15。
(1)写出该反应的平衡常数表达式_____。
(2)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件再达平衡后(填“增大”“减小”或“不变”):
①升高温度,CO2的平衡浓度_____,
②再通入CO2,CO2的转化率_____,
③增大容器的体积,混合气体的平均相对分子质量_____。
(3)该反应的逆反应速率随时间变化情况如图:

①从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是_____(填字母)。
a.升温b.增大CO2的浓度c.使用催化剂d.增压
②如果在t3时再增加CO2的量,t4时反应又处于新平衡状态,请在图上画出t3~t5时间段的v(逆)变化曲线_____。
(4)能判断该反应达到平衡的依据是_____。
A.容器内压强不变了 B.c(CO)不变了 C.v正(CO2)=v逆(CO) D.c(CO2)=c(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
![]()
(1) 写出有机物(a)的系统命名法的名称___________________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__________________。
(3) 上述有机物中与(c)互为同分异构体的是________(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____________。
(5) 上述有机物中不能与溴反应并使其褪色的有________(填代号)。
(6) (a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有________(填代号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com