
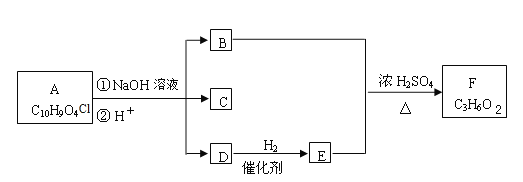
����Ŀ���л���A��F֮���ת����ϵ����ͼ��ʾ�����ֲ�������ȥ��������B����Է���������D��2����
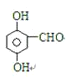
��ʾ��![]() ���Զ���ˮ�γ�R��CHO��
���Զ���ˮ�γ�R��CHO��
����������Ϣ�ش��������⣺
��1��B�ķ���ʽ��________________��
��2������D�й����ſ�ʹ�õ��Լ�������_________��д��D������ͬϵ������Լ���Ӧ�Ļ�ѧ����ʽ_______________________________��
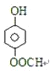
��3��C��FeCl3��Һ����ɫ���˴Ź������������ĸ��壬��������Ϊ1:2:2:1��д��C�Ľṹ��ʽ_______________________��
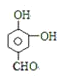
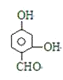
��4��д����������������C��ͬ���칹��Ľṹ��ʽ_______��______��______��________��
�ٱ����ϴ��ڶ�λȡ����������FeCl3��Һ����ɫ��������������Һ��Ӧ��
��5��д��A�Ľṹ��ʽ__________________________��
��6����1molA������NaOH��Ӧ�����������___________mol NaOH��
���𰸡�C2H4O2 ������Һ������Cu��OH��2����Һ CH3CHO+2Ag��NH3��2OH![]() CH3COONH4+2Ag+3NH3��+H2O��CH3CHO+NaOH+2Cu��OH��2
CH3COONH4+2Ag+3NH3��+H2O��CH3CHO+NaOH+2Cu��OH��2![]() CH3COONa+Cu2O��+3H2O
CH3COONa+Cu2O��+3H2O ![]()
![]() 4
4
��������
Aˮ�⡢�ữ�õ�B��C��D����A����������B��E��Ũ��������F��C3H6O2��ӦΪ������ת����ϵ��֪DΪȩ��EΪ����B����Է���������D��2����BΪCH3COOH��DΪHCHO��EΪCH3OH��FΪCH3COOCH3��C��FeCl3��Һ����ɫ�����з��ǻ������A�ķ���ʽ��֪C����7��Cԭ�ӣ�A�IJ����Ͷ�Ϊ=(2��10+2-9-1)/2=6������֪A�к���2��������������������γɵ�����������ˮ��õ���ȩ���ʴ���-COOCH2Cl�ṹ����C�л�����-COOH����C�ĺ˴Ź������������ĸ��壬������֮��Ϊ1��2��2��1����C�������������ڶ�λ����CΪ![]() ��AΪ
��AΪ![]() ��
��
��1��������������֪��BΪCH3COOH������ʽ��C2H4O2��
��2��DΪHCHO������D�й����ſ�ʹ���Լ�Ϊ��������Һ������Cu��OH��2����Һ��D������ͬϵ��ΪCH3CHO������Լ���Ӧ�Ļ�ѧ����ʽΪ��CH3CHO+2Ag��NH3��2OH![]() CH3COONH4+2Ag+3NH3��+H2O��CH3CHO+NaOH+2Cu��OH��2
CH3COONH4+2Ag+3NH3��+H2O��CH3CHO+NaOH+2Cu��OH��2![]() CH3COONa+Cu2O��+3H2O��
CH3COONa+Cu2O��+3H2O��
��3��������������֪��C�Ľṹ��ʽΪ��![]() ��
��
��4��C��![]() ����ͬ���칹����������������ٱ������ж�λȡ����������FeCl3��Һ����ɫ�����з��ǻ���������������Һ��Ӧ��˵������ȩ�������������ĵ���
����ͬ���칹����������������ٱ������ж�λȡ����������FeCl3��Һ����ɫ�����з��ǻ���������������Һ��Ӧ��˵������ȩ�������������ĵ��� ��
�� ��
�� ��
�� ��
��
��5��������������֪��A�Ľṹ��ʽΪ��AΪ![]() ��
��
��6����1molA������NaOH��Ӧ��1molA��2mol����Ҫ����2mol NaOH����ClҪ����1mol NaOH��ˮ������1mol��Ҫ����1mol NaOH�����������4mol NaOH��


 ������ȫ�̼����ĩ���100��ϵ�д�
������ȫ�̼����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��LiH2PO4���Ʊ���ص���Ҫԭ�ϡ������£�LiH2PO4��Һ��pH��c��ʼ��H2PO4�C���ı仯��ͼ1��ʾ��H3PO4��Һ��H2PO4�C�ķֲ���������pH�ı仯��ͼ2��ʾ��[![]() ]�����й�LiH2PO4��Һ��������ȷ����
]�����й�LiH2PO4��Һ��������ȷ����


A. ��Һ�д���3��ƽ��
B. ��PԪ�ص�������H2PO4�C��HPO42�C��PO43�C
C. ��c��ʼ��H2PO4�C��������Һ��pH���Ա�С
D. ��Ũ�ȴ���1 mol��L-1��H3PO4��Һ�ܽ�Li2CO3����pH�ﵽ4.66ʱ��H3PO4����ȫ��ת��ΪLiH2PO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼװ�ý���ʵ�飬����������ȷ���ǣ�Nװ���������缫��Ϊʯī����
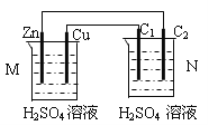
A. C1�Ϸ�����ԭ��Ӧ
B. Cu�缫��C2�缫�ϵĵ缫��Ӧ��ͬ
C. M װ����SO42������Cu�缫
D. ����һ��ʱ���װ��M ����ҺpH��С��װ��N����ҺpH���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I�� ������һ�ֳ��õĻ���ԭ�ϣ�Ӧ��ʮ�ֹ㷺��
��1����H2�ϳ�����CO(NH2)2���й��Ȼ�ѧ����ʽ�У�
��N2(g)��3H2(g)===2NH3(g) ��H1����92.4 kJ��mol��1
��NH3(g)��1/2CO2(g)===1/2NH2CO2NH4(s) ��H2����79.7 kJ��mol��1
��NH2CO2NH4(s)===CO(NH2)2(s)��H2O(l) ��H3����72.5 kJ��mol��1
��N2(g)��H2(g)��CO2(g)��Ӧ����CO(NH2)2(s)��H2O(l)���Ȼ�ѧ����ʽΪ_______________________________________________________��
II��ijͬѧ�����һ��绯ѧװ������ͼ��ʾ��������װ����XΪ�����ӽ���Ĥ���״�(CH3OH)���п�ȼ�ԡ�
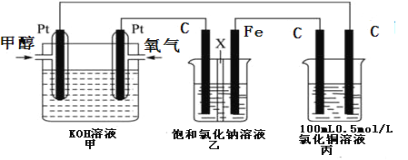
����Ҫ��ش�������⣺
��2��д��װ�ü��и����ĵ缫��Ӧʽ��_______________________________________��
��3��װ������ʯī�缫��C���ĵ缫��ӦʽΪ��_________________________________��
��4����װ�ü�������0.05molO2ʱ����װ��������������������___________L(�����)��װ��������Һ��pHΪ___________����Һ���Ϊ200mL���䣩��Ҫʹ���ձ��е���Һ�ָ���ԭ����״̬����Ҫ�����������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����Ȼ�隣������̿��Ʊ��ߴ�̼���̵�������ͼ��ʾ��

��֪�������̿����Ҫ�ɷ���MnCO3�����к�Fe��Ca��Mg��Al��Ԫ�ء�
��Al3+��Fe3+������ȫ��pH�ֱ�Ϊ4.7��3.2��Mn2+��Mg2+��ʼ������pH�ֱ�Ϊ8.1��9.1��
�۱��չ�������Ҫ��ӦΪMnCO3+2NH4Cl![]() MnCl2+2NH3��+CO2��+H2O��
MnCl2+2NH3��+CO2��+H2O��


��1�����ͼ1��2��3���������չ�������ѵı����¶ȡ�![]() ������ʱ�����ηֱ�Ϊ_____��_____��_____��
������ʱ�����ηֱ�Ϊ_____��_____��_____��
��2������Һ���������ӡ�������ͼ��

����֪��������������������ǿ��˳��Ϊ��H2O2��Cl2��MnO2��Fe3+����������X��ѡ��__(����ĸ)��
A��H2O2 B��Cl2 C��MnO2
�ڵ���pHʱ��pH��ȡ�ķ�ΧΪ______��
��3����̼���ᾧ�������У�����̼�����ʱ��Ӧ�����ӷ���ʽΪ____��
��4�����������п�ѭ��ʹ�õ�������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҿ�����һ�ֵͳɱ��������������״ʯīϩ������ԭ����Na2O+2CO  Na2CO3+C(ʯīϩ����Ȼ���ȥNa2CO3,�����Ƶ÷���״ʯīϩ������˵������ȷ���ǣ� ��
Na2CO3+C(ʯīϩ����Ȼ���ȥNa2CO3,�����Ƶ÷���״ʯīϩ������˵������ȷ���ǣ� ��
A.������ʯīϩ�ķ�Ӧ����������ԭ��Ӧ
B.ʯīϩ����ʯ��Ϊͬ��������
C.Na2O���ڼ��������CO�������������Na2CO3������
D.��Ȼ������Ԫ���Ի���̬��ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(CuSO4��5H2O)��ͭ����Ҫ������ڹ�ҵ������Ӧ�ù㷺��ʵ�����Ʊ��������������£�

(1) ϡ���ᡢϡ������ͭ�۷�Ӧ����һ����ɫ���壬��������_____(д��ѧʽ)���Ƶõĵ��������п��ܴ��ڵ�������_____(д����)��
(2) ʵ���ҿɲ��ó������ⶨ���õ���������CuSO4��5H2O�ĺ������������£�
��ȡ�����������ڼ�ˮ����ܽ⣻�ۼ���BaCl2��Һ���ܹ��ˡ�ϴ�ӡ�����ݳ��������㡣�ڹ���ǰ����Ҫ����SO42-�Ƿ������ȫ�����鷽����____________________________________________
(3) ���ı䷴Ӧ�����ɻ�û�ѧʽΪCux(OH)y(SO4)z��nH2O�ľ��壬�����ط����Ƕ�Cux(OH)y(SO4)z��nH2O������з������ƶϸþ���Ļ�ѧʽ��ȡ3.30 g������Ʒ�������ط��������ù��������ı仯��������ͼ��ʾ����֪����ϵ�¶���650 �漰����ʱ���ų�������ֻ��ˮ������ʵ�����¶���650 ��ʱ�������������ɿ���ΪaCuO��bCuSO4���¶���1 000 ������ʱ���õ��Ĺ���ΪCu2O��
��ش��������⣺
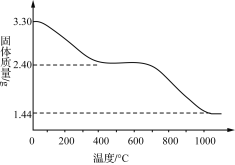
���¶�650��1 000 ������������У�n(O)��n(S)____(����>����<����������)3��
��ͨ�������ƶ�Cux(OH)y(SO4)z��nH2O����Ļ�ѧʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
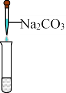
����Ŀ��ʵ������ʧȥ��ǩ����ɫ��Һ���Ȼ��ء��������ƺ�ϡ���ᣬ����һ�ֳ������ָʾ��X��Na2CO3һ�μ������ǡ������йز����������Լ���գ�
��1��������Һ����ɫ����ȡ����Һ����Na2CO3��Һ�У������������ƶ��Լ�XΪ_____��
![]()
��2��������Һ����ɫ����ȡ����Һ����Na2CO3��Һ�У�����Ϊ______________,�йط�Ӧ�����ӷ���ʽΪ____________________��
![]()
��3�����������ݲ������йط�Ӧ�����ӷ���ʽΪ________________________����ȡ����Һ�����Լ�X������Һ��___________�����ɫ��������ɫ������ɫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ�����������������ȷ����(����)

A. ʵ������ͼ1װ���Ʊ�Cl2
B. ���Ⱥ�ͼ2����Һ��ɫ�ָ���ɫ
C. ��ͼ3װ�ó�ȥCl2�к��е�����HCl
D. ʵ������ͼ4װ����ȡ��������ˮ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com