
| A. | 充电时,电解质溶液中K+向阳极移动 | |
| B. | 放电时,电解质溶液中K+向正极移动 | |
| C. | 充电时,阳极反应为:Zn(OH)${\;}_{4}^{2-}$+2e-═Zn+4OH- | |
| D. | 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况) |
分析 根据2Zn+O2+4OH-+2H2O═2Zn(OH)42-可知,O2中元素的化合价降低,被还原,应为原电池正极,Zn元素化合价升高,被氧化,应为原电池负极,充电时阳离子向阴极移动,放电时阳离子向正极移动,以此解答该题.
解答 解:A.充电时阳离子向阴极移动,即K+向阴极移动,故A错误;
B.放电时,为原电池,溶液中阳离子向正极移动,即K+向正极移动,故B正确;
C.充电时,阳极上发生失电子的氧化反应,阴极上发生得电子的氧化反应,则阴极反应为:Zn(OH)${\;}_{4}^{2-}$+2e-═Zn+4OH-,故C错误;
D.放电时,电路中通过4mol电子,消耗氧气1mol,其体积为22.4L(标准状况),故D错误.
故选B.
点评 本题考查原电池与电解池的基础知识,正确判断正负极、阴阳极,注意电极反应式的书写及电子转移的计算,正确判断化合价的变化为解答该题的关键,题目难度中等.


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:推断题
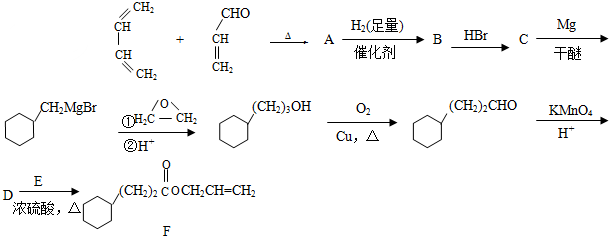
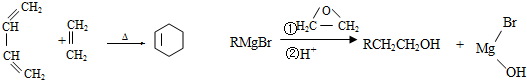
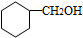 .
. .
. .
.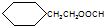
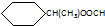 .
.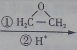 CH3CH2CH2CH2OH(其他试剂任选).
CH3CH2CH2CH2OH(其他试剂任选).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
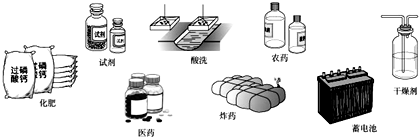
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖可用于补钙药物的合成 | |
| B. | 次氯酸钠溶液可用于环境的消毒杀菌 | |
| C. | 聚乙烯塑料制品可用于食品的包装 | |
| D. | 生石灰可用作食品抗氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | |||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ④ | ⑨ |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com