
【题目】下列用来表示物质变化的化学用语中,正确的是( )
A. 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣=Fe2+
B. HS﹣的水解方程式:HS﹣+H2O![]() S2﹣+H3O+
S2﹣+H3O+
C. CO32﹣的水解方程式:CO32﹣+H2O![]() HCO3﹣+OH﹣
HCO3﹣+OH﹣
D. AlCl3溶液与Na2CO3溶液混合:2Al3++3CO32﹣=Al2(CO3)3↓
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】活性炭可处理大气污染物NO。为模拟该过程,T℃时,在3L密闭容器中加入NO和活性炭粉,反应体系中各物质的量变化如下表所示。下列说法正确的是
活性炭/mol | NO/mol | X/mol | Y/mol | |
起始时 | 2.030 | 0.100 | 0 | 0 |
10min达平衡 | 2.000 | 0.040 | 0.030 | 0.030 |
A. X一定是N2,Y一定是CO2
B. 10min后增大压强,NO的吸收率增大
C. 10min后加入活性炭,平衡向正反应方向移动
D. 0~10min的平均反应速率v(NO)=0.002 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O![]() 2Zn(OH)
2Zn(OH) ![]() 。下列说法正确的是 ( )
。下列说法正确的是 ( )
A. 充电时,电解质溶液中K+向阳极移动
B. 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
C. 充电时,阳极反应为:Zn(OH) ![]() +2e–=== Zn+4OH–
+2e–=== Zn+4OH–
D. 放电时,电解质溶液中K+向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一种重要的有机合成中间体,经常用来合成多种高分子化合物。已知A分子中不含甲基。由A合成的两种高分子化合物的路线如下图所示:

(1)写出C中含有的官能团名称___________________ 。
(2)由A生成B的反应类型为______________________________________。
(3)C的核磁共振氢谱有________组峰
(4)写出A生成D的化学方程式_______________________________________。
(5)F的结构简式是___________________。
(6)苯环上的二取代芳香化合物W是D的同分异构体,且W分子中只具有一个官能团,则W的结构共有_____________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 新发现的核素![]() 中,电子数比中子数多179
中,电子数比中子数多179
B. 白磷和红磷互为同分异构体
C. 氕、氘、氚互为同素异形体
D. CH3CH2CH2CH3 和C(CH3)4互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是常用的定影剂、还原性分析试剂。Na2S2O3·5H2O是无色晶体,易溶于水,不溶于乙醇,在潮湿的空气中易潮解,Na2S2O3和甲醛能形成难被碘溶液氧化的化合物。甲、乙两个兴趣小组用下列装置在实验室制备硫代硫酸钠。
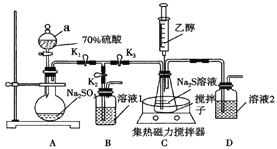
回答下列问题:
(1)仪器a的名称是____________;溶液1是____________。
(2)甲小组按上图连接好装置,打开K1、K3,关闭K2,打开仪器a的活塞;片刻后,打开集热式磁力搅拌器加热;将气体通入锥形瓶中,溶液出现黄色浑浊后逐渐消失,相关的化学反应方程式为:①_________________;②Na2SO3+S![]() Na2S2O3。
Na2S2O3。
(3)加热浓缩至出现少量晶膜,停止加热,打开K2,关闭K3,用注射器注入无水乙醇后有大量晶体析出。加入乙醇的作用是__________________________________。
(4)乙小组在制备Na2S2O3时进行了改进。将C装置中的溶液换为Na2CO3和Na2S混合液,其反应为:Na2CO3+Na2S+4SO2=3Na2S2O3+CO2。配制该混合溶液的过程中,先将Na2CO3完全溶解,再将Na2S溶解于Na2CO3的溶液中,其目的是__________________。
(5)测定乙小组产品纯度。取3.000gNa2S2O3·5H2O晶体,配成100mL溶液,取20.00mL于锥形瓶,调节溶液的pH至6,加入适量甲醛溶液和Zn(CH3COO)2溶液,过滤,洗涤,在滤液中滴加几滴淀粉溶液,用0.1000mol/L标准碘溶液滴定,消耗标准碘溶液10.00mL。
①加入适量甲醛溶液和Zn(CH3COO)2溶液的目的是_________________________________。
②该产品中Na2S2O3·5H2O的质量分数为_____________。 (已知:2Na2S2O3+I2=Na2S4O6+2NaIKsp(ZnS)=1.6×10-24 M(Na2S2O3·5H2O)=248g/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。

(1)O和S中,原子半径较大的是________;(填元素符号或化学,以下同)
(2)CH4和NH3中,热稳定性较强的是________;
(3)新制氯水有漂白作用,是因为其中含有________;
(4)元素最高价氧化物对应水化物中,两性氢氧化物是________________;
(5)上表元素中,存放最高价氧化物对应水化物的碱性最强的溶液的试剂瓶盖不能用玻璃塞,请写出该反应的离子方程式_______________。
Ⅱ.现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)元素T在元素周期表中的位置是________________。
(2)元素Y与元素Z相比,金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是______(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)上述四种元素中有2种元素能形成一种淡黄色的固体,该化合物的电子式是________________,所含化学键的类型有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,发展前景广阔。
(1)利用甲醇可制成微生物燃料电池(利用微生物将化学能直接转化成电能的装置)。某微生物燃料电池装置如右图所示:A极是________极(填“正”或“负”),其电极反应式是________。

(2)研究表明CO2加氢可以合成甲醇。CO2和H2可发生如下两个反应:
I.CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH1
CH3OH(g) + H2O(g) ΔH1
II.CO2(g) + H2(g)![]() CO(g) + H2O(g) ΔH2
CO(g) + H2O(g) ΔH2
①反应I的化学平衡常数表达式K=________。
②有利于提高反应I中 CO2的平衡转化率的措施有________(填序号)。
a.使用催化剂 b.加压 c.增大CO2和H2的初始投料比
③研究温度对于甲醇产率的影响。在210 ℃~290 ℃,保持原料气中CO2和H2的投料比不变,按一定流速通过催化剂甲,主要发生反应I,得到甲醇的实际产率、平衡产率与温度的关系如右图所示。

ΔH1________0(填“>”、“=”或“<”),其依据是________。
④某实验控制压强一定,CO2和H2初始投料比一定,按一定流速通过催化剂乙,经过相同时间测得如下实验数据(反应未达到平衡状态):
T(K) | CO2实际转化率(%) | 甲醇选择性(%)【注】 |
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
【注】甲醇选择性:转化的CO2中生成甲醇的百分比
表中实验数据表明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com