
【题目】下列各组混合物中,能用分液漏斗进行分离的是
A.氯化钠和水B.碘和四氯化碳C.水和四氯化碳D.汽油和植物油
科目:高中化学 来源: 题型:
【题目】α丙氨酸是组成人体蛋白的氨基酸之一,如图是α丙氨酸的分子结构模型图,下列对α丙氨酸的叙述不正确的是( )
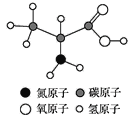
A. α丙氨酸分子由碳、氢、氧、氮四种原子构成
B. α丙氨酸中氧元素的质量分数最大
C. α丙氨酸的分子式为C3H7O2N
D. α丙氨酸与CH3CH2CH2NO2以及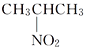 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2 mol某金属单质与足量的盐酸反应,放出67.2L H2(标准状况),并转变为具有Ne原子电子层结构的离子,该金属元素在元素周期表中的位置是
A. 第三周期第ⅠA族B. 第三周期第ⅡA族
C. 第三周期第ⅢA族D. 第四周期第ⅢA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃,,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 1 | 2 | 0 |
平衡浓度/(mol·L-1) | 0.6 | 1.2 | 0.8 |
下列说法错误的是( )
A. 反应达到平衡时,X的转化率为40%
B. 反应可表示为X(g)+2Y(g) ![]() 2Z(g),其平衡常数为0.74
2Z(g),其平衡常数为0.74
C. 其它条件不变时,增大压强能使平衡向生成Z的方向移动,平衡常数也增大
D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制适合的条件,将反应Fe3++AgFe2++Ag+设计成如下图所示的原电池(盐桥装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后,观察到电流计指针向右偏转。下列判断不正确的是( )。
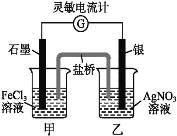
A. 在外电路中,电子从银电极流向石墨电极
B. 盐桥中的K+移向甲烧杯
C. 电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转
D. 一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,推出图中标记的11种元素,回答下列问题:
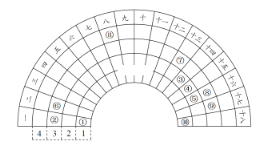
(1)⑤元素形成的简单阴离子的结构示意图为________。
(2)④的气态氢化物的电子式为_____。
(3)在11种元素中,单质的化学性质最不活泼的是_______。(填化学式)
(4)⑧⑨两种元素形成的最高价氧化物的水化物中,酸性较强的是________。(填化学式)
(5)③的单质可以和⑧的最高价氧化物的水化物的浓溶液反应,请写出有关反应的化学方程式____________。
(6)⑦在元素周期表中的位置是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要除去氯气中少量的HCl和水蒸气,可将气体依次通过
A.浓硫酸,饱和食盐水B.NaOH溶液,浓硫酸
C.饱和食盐水,碱石灰D.饱和食盐水,浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关电解质溶液叙述错误的是
A. 某H2SO4溶液中c(OH-)/c(H+)=1.0×10-8,由水电离出的c(H+)=1×10-11mol·L-1
B. 将0.02mol·L-1盐酸与0.02mol·L-1Ba(OH)2溶液等体积混合后溶液pH约为12
C. 将一定体积稀盐酸与稀氨水混合,当溶质为NH3·H2O和NH4Cl时,溶液的pH一定大于7
D. 向0.1mol·L-1Na2CO3溶液中逐滴滴加0.1mol·L-1稀盐酸,溶液中c(HCO)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:

(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)===Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ·mol–1
Mg2SiO4(s)+4H+(aq)="==2" Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ·mol–1
酸溶需加热的目的是_____ _;所加H2SO4不宜过量太多的原因是____ __。
(2)加入H2O2氧化时发生发应的离子方程式为__________
(3)用如图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。

①实验装置图中仪器A的名称为__________。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂, 、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水, ,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O。
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com