
【题目】下列事实不能用勒夏特列原理解释的是
A.溴水中存在Br2+H2O![]() HBr+HBrO,加入AgNO3溶液,溴水褪色
HBr+HBrO,加入AgNO3溶液,溴水褪色
B.对于平衡2SO2+O2![]() 2SO3,使用催化剂有利于SO3的合成
2SO3,使用催化剂有利于SO3的合成
C.醋酸稀溶液加热后溶液pH降低(不考虑醋酸受热挥发)
D.合成氨时适当增大压强有利于提高氮气的转化率
【答案】B
【解析】
勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着减弱这种改变的方向移动,使用勒夏特列原理时,必须是可逆反应,且存在平衡移动的现象,否则勒夏特列原理不使用。
A.加入AgNO3溶液,生成AgBr 沉淀,HBr浓度减小,平衡正向移动,溴水褪色,可用勒夏特列原理解释,故A正确;
B.使用催化剂会提高反应的速率,但是正逆反应速率相等,平衡不移动,所以不能用勒夏特列原理解释,故B错误;
C.醋酸存在电离平衡,该可逆反应是吸热反应,加热,平衡正向移动,氢离子浓度增大,pH降低,可用勒夏特列原理解释,故C正确;
D.氮气与氢气合成氨是一个可逆反应,增大压强,会使平衡向系数减小的方向移动,平衡正向移动,有利于提高氮气的转化率,可用勒夏特列原理解释,故D正确;
答案选B。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)在25℃、101Kpa下,1gCH3OH(l)燃烧生成CO2(g)和H2O(l)时放热22.68kJ。则CH3OH燃烧的热化学方程式为__________________。
(2)若以(1)中反应原理设计成甲醇燃料电池,电解质溶液为20%~30%的 KOH溶液,则该燃料电池的负极电极反应式为___________________。
(3)惰性电极电解400mL2mol/LCuSO4溶液,一段时间阴极增重1.28g (该极无气体放出),电解后溶液体积不变,则溶液的pH 为_____,阳极可收集标况下气体____mL。写出电解的离子方程式:_____
(4)某温度下,反应2NH3(g)![]() N2(g)+3H2(g)于恒容密闭容器中达到平衡状态。(填“正向”、“逆向”或“不”)。若某时刻向该容器内通入一定量氨气,则化学平衡________移动。若某时刻容器内所有物质的浓度均增加为原来的2倍,则化学平衡________移动。
N2(g)+3H2(g)于恒容密闭容器中达到平衡状态。(填“正向”、“逆向”或“不”)。若某时刻向该容器内通入一定量氨气,则化学平衡________移动。若某时刻容器内所有物质的浓度均增加为原来的2倍,则化学平衡________移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. NaCl的摩尔质量是58.5g
B. 在1L水中溶解5.85gNaCl,即可配制得0.1mol/L的NaCl溶液
C. 标准状况下,22.4L H2O含有氢原子的数目为2NA
D. 17g NH3中含有分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油通过裂解可以得到乙烯,乙烯的产量可以用来衡量一个国家石油化工发展水平。下图是由乙烯为原料生产某些化工产品的转化关系图。

(1)乙烯生成B的反应类型是_______________________。
(2)A的名称是_______________________________ 。
(3)C中含有的官能团是 _________________________(填名称)。
(4)写出B+D→E的化学反应方程式:___________________________。
(5)写出与D同类的E的两种同分异构体的结构简式_____________;_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是
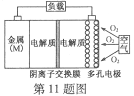
A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C. M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D. 在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2X2(g)+Y2(g)![]() 2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
2Z(g) ΔH1=-akJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和lmolY2,在500℃时充分反应达平衡后Z的浓度为Wmol·L-1,放出热量bkJ。
(1)此反应平衡常数表达式为___;若将温度降低到300℃,则反应平衡常数将___(填增大、减少或不变)。
(2)能说明反应己达平衡状态的是___
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内的密度保持不变
(3)若将上述容器改为恒压容器![]() 反应器开始体积相同
反应器开始体积相同![]() ,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将____(填变大、变小或不变)。
,相同温度下起始加入2molX2和lmolY2达到平衡后,Y2的转化率将____(填变大、变小或不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国规定饮用水质量标准必须符合下表所示要求:
项目 | pH | Ca2+、Mg2+总浓度 | 细菌个数 |
相关值 | 6.5~8.5 | <0.0045mol·L-1 | <100个·mL-1 |
下图是源水处理成自来水的工艺流程示意图。
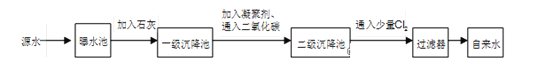
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,在一级沉降池中所得沉淀的主要成分为 _____ 和_______ (化学式)。
(2)FeSO4·7H2O是常用的凝聚剂,它在水中最终生成胶状Fe(OH)3沉淀。凝聚剂除去悬浮固体颗粒的过程______________(填写编号)。
①只是物理过程; ②只是化学过程; ③是物理和化学过程。
(3)Cl2的作用是______ ,这种作用是基于Cl2和水反应的产物具有 _______ 性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化
温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)甲同学认为,该溶液的pH值升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为_________。
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度_________(填“大于”或“小于”)NaHCO3。
(3)丙同学认为甲、乙的判断都不充分。丙认为:
①只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则_________(填“甲”或“乙”)判断正确。试剂X是_____________(填序号)。
a.Ba(OH)2溶液 b.BaCl2溶液 c.NaOH溶液 d.澄清石灰水
②将加热后的溶液冷却到10℃,若溶液的pH____________(填“高于”、“低于”或“等于”)8.3,则甲判断正确。
(4)常温下,在测得pH都等于9的NaOH溶液和Na2CO3溶液中,由水电离出的OH-浓度分别为a mol/L和b mol/L。则a:b=________。
(5)25℃时,浓度均为0.1 mol/L的Na2CO3和NaHCO3溶液。
①下列判断不正确的是________(填序号)。
a.两种溶液等体积混合后:3c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)]
b.两种溶液中存在的粒子种类不相同
c.两种溶液中c(H+)·c(OH-)=10-14
d.两种溶液中分别加入少量NaOH固体,恢复到原温度,c(CO32-)均增大
②等体积混合后溶液中离子浓度由大到小的顺序是:__________;
③常温下,等体积混合后的溶液中滴加稀盐酸至中性时,溶质的主要成分有:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组进行Na2O2与水反应的实验,如下图所示,该小组对试管c中红色褪去的原因进行探究。
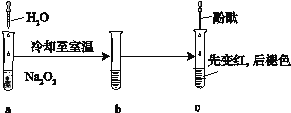
(1)Na2O2中含有的化学键类型:__________;请写出a中反应的化学方程式______。
查阅资料:
①当NaOH溶液pH≥13时,可以使酚酞由红色褪为无色;
②Na2O2与水反应分两步进行:Na2O2+ H2O =" NaOH" + H2O22H2O2= 2H2O + O2↑
(2)请设计实验验证Na2O2与水反应后的溶液中有H2O2残留:取少量b溶液于试管中,____________,证明溶液中有H2O2残留。
(3)结合资料,该小组同学针c中溶液红色褪去的原因提出以下假设:
①_____________________;
② 溶液中H2O2破坏酚酞的结构;
③ NaOH和H2O2共同作用结果。
(4)该小组同学测出c中溶液的pH为14,认为还不能排除假设②、③,于是又进行了如下实验,请完成下表空白处:
实验 | 操作 | 现象 | 结论 |
1 | 向少量H2O2中滴加2滴酚酞,放置一段时间,再加入NaOH溶液至pH=12 | 加入NaOH后,无色溶液先变红,后褪色 | ①___________ |
2 | 向少量 NaOH溶液(pH=14)中滴加2滴酚酞;再加适量稀盐酸至溶液 pH=12 | 溶液先变红,后褪色;加盐酸后,又出现红色,且不褪色 |
|
3 | 向Na2O2与水反应后的溶液(pH=14)中滴加2滴酚酞;再加适量稀盐酸至溶液 pH=12…… | ②_____________________________…… | 溶液pH大于13时,NaOH使变红的溶液褪色;pH在8~13时, NaOH和H2O2共同作用使溶液褪色 |
(5)某同学按取(4)中述实验2褪色后的溶液,加水稀释至pH=12,没有观察到溶液变红。该同学推测实验2加盐酸后溶液变红还可能与温度有关,请写出理由:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com