

| 3.96g |
| 44g/mol |
| 0.99g |
| 18g/mol |
| 0.112L |
| 22.4L/mol |
| 0.48g |
| 16g/mol |
| 1.81g |
| 181g/mol |
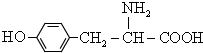 ,
,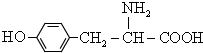 ;
;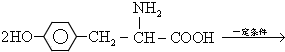
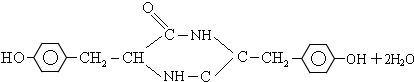 ,
,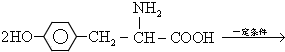
 ;
;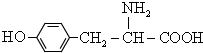 ,①苯环上含三个间位取代基,且有一个为氨基(与苯环直接相连);②能与FeCl3溶液发生显色反应,该有机物分子中含有酚羟基;③属于酯类,其分子中含有酯基,且可与新制Cu(OH)2反应产生砖红色沉淀,该酯为甲酸酯,满足条件的有机物的结构简式为:
,①苯环上含三个间位取代基,且有一个为氨基(与苯环直接相连);②能与FeCl3溶液发生显色反应,该有机物分子中含有酚羟基;③属于酯类,其分子中含有酯基,且可与新制Cu(OH)2反应产生砖红色沉淀,该酯为甲酸酯,满足条件的有机物的结构简式为: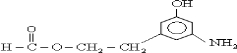 、
、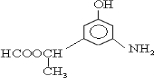 ,
,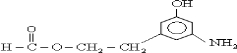 、
、 .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向KHSO4溶液中滴人Ba(OH)2溶液使溶液pH=7,对应的离子方程式;SO42-+2H++Ba2++2OH-=BaSO4↓+2H2O |
| B、明矾水解的离子方程式:Al3++3 H2O═Al(OH)3↓+3H+ |
| C、Mg(HCO3)2 溶液与盐酸溶液反应的离子方程式:HCO3-+H+═CO2↑+H2O |
| D、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图,从表中选出正确选项( )
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图,从表中选出正确选项( )| 锥形瓶中液体 | 滴定试管中液体 | 选用指示剂 | 选用滴定管 | |
| ① | 碱 | 酸 | 石蕊 | (乙) |
| ② | 酸 | 碱 | 酚酞 | (甲) |
| ③ | 碱 | 酸 | 甲基橙 | (甲) |
| ④ | 酸 | 碱 | 酚酞 | (乙) |
| A、①② | B、①③ | C、②④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com