
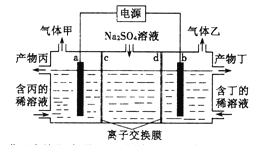
【题目】电解硫酸钠溶液生产硫酸和烧碱的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1:2,下列有关说法正确的是(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
A. a电极反应式为:2H++2e—=H2↑ B. 产物丙为硫酸
C. d为阴离子交换膜 D. Na2SO4溶液浓度增大
【答案】B
【解析】试题分析:电解硫酸钠溶液时,阳极上生成氧气,电极反应式为2H2O-4e-=O2↑+4H+,阴极反应式为 2H2O+2e-=H2↑+2OH-,测得同温同压下,气体甲与气体乙的体积比约为1:2,则甲是氧气、乙是氢气,则a是阳极、b是阴极,阳极区域生成硫酸、阴极区域生成NaOH;A.a为阳极,电极反应式为2H2O-4e-=O2↑+4H+,故A错误;B.通过以上分析知,a为阳极,同时生成硫酸,所以产物丙是硫酸,故B正确;C.产物丁是NaOH,则离子交换膜d是阳离子交换膜,故C错误;D.根据以上分析,阳极区域生成硫酸、阴极区域生成NaOH,所以Na2SO4溶液浓度减小,故D错误;故选B。


 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 24gNaH中阴离子所含电子总数为2NA
B. 标准状况下,44.8LNO与22.4LO2充分混合后,气体中分子总数为2NA
C. 在0.lmol/L的K2CO3溶液中,因CO32-的水解,阴离子数目大于0.1NA
D. 300mL 2mol/L乙醇溶液中所含分子数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s) ![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )

A. 反应CO2(g)+C(s)===2CO(g)的ΔS>0、ΔH<0 B. 体系的总压强p总:p总(状态Ⅱ)= 2p总(状态Ⅰ)
C. 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) D. 逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.淀粉、纤维素、葡萄糖均能发生水解反应
B.使用青霉素前一定要进行皮肤敏感试验
C.利用油脂在碱性溶液中的水解可制取肥皂
D.甲醛,氯乙烯,乙二醇均可做聚合反应的单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙和X是四种中学化学中常见的物质,其转化关系如下图,则甲和X不可能是( )

A. 甲为C,X是O2 B. 甲为SO2,X是NaOH溶液
C. 甲为Cl2,X为Fe D. 甲为Al,X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,向盛有50 mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示。下列叙述正确的是( )

A. HA溶液的物质的量浓度为0.01 mol·L-1
B. b→c的过程中,温度降低的原因是溶液中发生了吸热反应
C. 25 ℃时,HA的电离平衡常数K约为1.43×10-2
D. b点处,酸碱恰好中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一种泉水,取0.5L这种泉水作为样品,经测定该样品中含有0.48g的Mg2+ . 那么,该泉水中Mg2+的物质的量的浓度是多少?为使该泉水样品所含的Mg2+全部沉淀,应加入1mol/L NaOH溶液的体积是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学帮助水质检测站配制480mL 0.5molL﹣1 NaOH溶液以备使用.
(1)该同学应选择mL的容量瓶.
(2)其操作步骤如图所示,则图A操作应在①~⑥图中的(填选项字母)之间. 
A.②与③
B.①与②
C.④与⑤
(3)该同学应称取NaOH固体g;
(4)(2)中⑤的具体操作是
(5)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会(填“偏大”“偏小”或“无影响”,下同).
②容量瓶中原来有少量蒸馏水,浓度会 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com