
【题目】用 0.1000 mol·L1 NaOH 溶液分别滴定 20.00 mL 0.1000 mol·L1 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
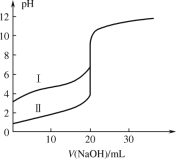
A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.V(NaOH) = 10.00 mL 时,醋酸溶液中c(CH3COOH)<c(CH3COO)
C.pH = 7 时,滴定盐酸消耗的 NaOH 溶液体积小于滴定醋酸消耗的 NaOH 溶液体积
D.V(NaOH) = 20.00 mL 时,两溶液中 c(CH3COO)=c(Cl)
【答案】B
【解析】
A. 0.1000 mol·L1的盐酸和醋酸,盐酸的pH =1,醋酸的pH值大于1,因此Ⅰ、Ⅱ分别表示醋酸和盐酸的滴定曲线,故A错误;
B. V(NaOH) = 10.00 mL 时,所得溶液为等物质的量浓度的醋酸和醋酸钠的混合液,根据图中信息,溶液显酸性,醋酸电离程度大于醋酸根水解程度,因此溶液中c(CH3COOH)<c(CH3COO),故B正确;
C. pH = 7 时,滴定盐酸消耗的 NaOH 溶液体积为20.00mL,滴定醋酸消耗的 NaOH 溶液体积为20.00mL时,溶质为醋酸钠,溶液显碱性,要使得溶液的pH= 7 ,则加入的NaOH溶液体积小于20.00mL,因此滴定盐酸消耗的 NaOH 溶液体积大于滴定醋酸消耗的 NaOH 溶液体积,故C错误;
D. V(NaOH) = 20.00 mL 时,两溶液溶质分别为NaCl和CH3COONa,醋酸根水解,因此溶液中c(CH3COO)<c(Cl),故D错误;
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】我国是全钒液流电池最大生产国,产品出口美、欧、日等发达国家,市 场占有率全球第一。全钒液流电池充电时间短,续航能力强,被誉为“完美电池”,工作原理如图1所示,反应的离子方程式为:VO2++V3++H2O![]() VO2++V2++2H+。以此电池电解Na2SO3溶液(电极材料为石墨),可再生NaOH,同时得到H2SO4,其原理如图2所示。下列说法正确的是
VO2++V2++2H+。以此电池电解Na2SO3溶液(电极材料为石墨),可再生NaOH,同时得到H2SO4,其原理如图2所示。下列说法正确的是
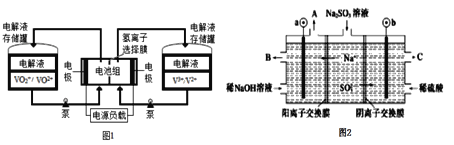
A.电解Na2SO3溶液时,a极与电池负极相连,图1中H+从电池右边移向左边
B.电解时b的电极反应式为SO32-+H2O-2e-=SO42-+2H+
C.电池放电时,负极电解液的pH升高
D.若电解过程中图2所有液体进出口密闭,则消耗12.6gNa2SO3阴极区变化的质量为4.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)2C(g)。若经2 s时测得C的浓度为0.6 mol·L-1,填写下列空白:
(1)用物质A表示反应的平均速率为_________。
(2)用物质B表示反应的平均速率为_________。
(3)2 s时物质A的转化率为_________。
(4)2 s时物质B的体积分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从下列实验事实或操作所引出的相应结论正确的是( )
选项 | 实验事实或操作 | 结论 |
A | 其他条件相同, | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
C | 物质的量浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应 | 开始时的反应速率相同 |
D | 在容积可变的密闭容器中发生反应 | 正反应速率加快,逆反应速率不变 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200mL 1molL—1的氯化铝溶液中加入一定体积的2molL—1的NaOH溶液,最终产生7.8g沉淀,则加入的NaOH溶液的体积可能为
①350mL ②90mL ③150mL ④200mL
A. 只有① B. ①③ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是
A. ![]() B.
B. ![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m<p<
m<p<![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有14.4 g CO和CO2的混合气体,在标准状况下所占的体积约为8.96 L。将混合气体依次通过如图装置,最后收集在气球中。下列结论不正确的是( )
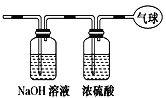
A.原混合气体所含氧原子总数为0.6 NA(用NA表示阿伏加德罗常数的值)
B.标况下气球中收集到的气体体积为4.48L
C.原混合气体的平均摩尔质量为32g/mol
D.原混合气体CO和CO2的体积比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒压下,对于反应:A(g)+3B(g)![]() 3C(g),达到平衡状态的标志是( )
3C(g),达到平衡状态的标志是( )
A.v正(A)=3v逆(C)
B.密闭容器内气体的密度不再改变
C.单位时间内消耗3nmolC的同时,生成3n molB
D.密闭容器内A、B、C气体的浓度之比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面四种变化中,有一种变化与其他三种变化类型不同的是( )
A.CH3CH2OH + CH3COOH ![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
B.CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
C.2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O
CH3CH2OCH2CH3 + H2O
D.CH3CH2OH + HBr→CH3CH2Br + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com