
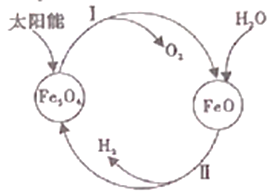
【题目】(1)工业上尝试用太阳能分解水制取H2,其过程如下:
已知:2H2O(l)=2H2(g)+O2(g) △H=+571.6kJ/mol
2Fe3O4(s)![]() 6FeO(s)+O2(g) △H=+313.8kJ/mol
6FeO(s)+O2(g) △H=+313.8kJ/mol
①过程I中,需将O2及时分离出去,目的是_________。
②过程II的热化学方释式是_________。
③整个过程中,Fe3O4的作用是_________。
(2)工业上利用H2合成氢的反应原理为:3H2(g)+N2(g) ![]() 2NH3(g)。现有甲、乙两个容积为1L的密闭容器.在相同条件下,按不同的反应物投入量进行合成氢反应相关数据如下表示:
2NH3(g)。现有甲、乙两个容积为1L的密闭容器.在相同条件下,按不同的反应物投入量进行合成氢反应相关数据如下表示:
容器 | 甲 | 乙 |
反应物投入量 | 2molH2、2molN2 | 4malH2.4molN2 |
平衡时N2的浓度(mol/L) | c1=1.5 | c2 |
NH3的体积分数 | ω1 | ω2 |
混合气体的密度(g/L) | ρ1 | ρ2 |
①下列情况下,反应达到平衡状态的是_____(填序号)
a.3molH-H共价键断裂同时有6molN-H共价键形成
b.3v正(N2)=v逆(H2)
c.混合气体的平均相对分子质量保持不变
②反应的平衡常数K=_______(结果保留3位有效数字).
③分析上表中的数据,有以下关系:c2________3mol/L;ω1________ω2(填“>”、“<”、“=”);若ρ1=ag/L,则ρ2________g/L(用含a的式子表示)
(3)利用氨水吸收工业废气中的SO2,既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4,其氧化速率与温度关系如下图:
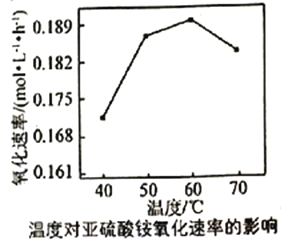
试解释在温度较高时,(NH4)2SO3氧化速率下降的原因是_________。
【答案】 提高Fe3O4的转化率 3FeO (s)+H2O (l)=Fe3O4 (s)+H2 (g) ΔH=+128.9kJ·mol-1 催化剂 bc 5.33 < < 2a 温度过高(NH4)2SO3会分解,浓度减小(或温度升高氧气在溶液中溶解度降低)
【解析】(1)①过程I的反应中,分离出O2,可以使反应正向移动,提高Fe3O4的转化率。
②过程II反应物为FeO 和H2O ,生成物为Fe3O4 和H2,
已知i.2H2O(l)=2H2(g)+O2(g) △H=+571.6kJ/mol
ii.2Fe3O4(s)![]() 6FeO(s)+O2(g) △H=+313.8kJ/mol
6FeO(s)+O2(g) △H=+313.8kJ/mol
根据盖斯定律,(i-ii)![]() 得,3FeO (s)+H2O (l)=Fe3O4 (s)+H2 (g) ΔH=+128.9kJ·mol-1
得,3FeO (s)+H2O (l)=Fe3O4 (s)+H2 (g) ΔH=+128.9kJ·mol-1
③整个过程总反应是水的分解反应,Fe3O4的作用是催化剂。
(2)a.3molH-H共价键断裂同时有6molN-H共价键形成,表示的都是正反应速率,无法判断正逆反应速率是否相等,a错误;b.达到平衡时3v正(N2)=v逆(H2),b正确;c.混合气体的平均相对分子质量保持不变,说明气体的物质的量不变,达到平衡状态,c正确;本题答案为bc。
②用“三行式”求平衡时浓度,
3H2(g)+N2(g) ![]() 2NH3(g)
2NH3(g)
起始浓度(mol/L) 2 2 0
变化浓度(mol/L)1.5 0.5 1
平衡浓度(mol/L)0.5 1.5 1
K=![]() =5.33
=5.33
③甲、乙等温等容,起始投料乙是甲的二倍,可以假想乙是两个分别进行的甲,再合二为一,这就等同于加压,平衡正向移动,因甲平衡时N2的浓度为c1=1.5,则乙平衡时N2的浓度c2<2![]() 1.5mol/L,即c2<3mol/L;NH3的体积分数ω1<ω2;若ρ1=ag/L,体积不变,混合气体的质量乙是甲的二倍,根据
1.5mol/L,即c2<3mol/L;NH3的体积分数ω1<ω2;若ρ1=ag/L,体积不变,混合气体的质量乙是甲的二倍,根据![]() 则ρ2=2ag/L。
则ρ2=2ag/L。
(3)由图中曲线可知,温度超过60℃,氧化速率反而降低,原因是温度过高(NH4)2SO3会分解,浓度减小,也可能是温度升高氧气在溶液中溶解度降低。因此,本题答案为温度过高(NH4)2SO3会分解,浓度减小(或温度升高氧气在溶液中溶解度降低)。


科目:高中化学 来源: 题型:
【题目】有机物D的结构简式:![]() ,学名肉桂酸,又名β-苯丙烯酸,主要用于香精香料、食品添加剂、医药工业、美容、农药、有机合成等方面,其合成路线(部分反应条件略去)如下所示:
,学名肉桂酸,又名β-苯丙烯酸,主要用于香精香料、食品添加剂、医药工业、美容、农药、有机合成等方面,其合成路线(部分反应条件略去)如下所示:
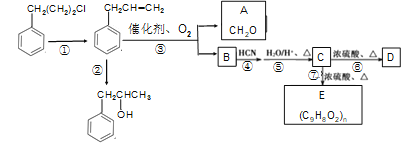
已知: ⅰ CH3CH=CH2![]() CH3CHO + HCHO;
CH3CHO + HCHO;
ⅱ RCHO![]()
![]()
![]()
![]()
完成下列填空:
(1)C中含氧官能团名称是___________________,E的结构简式为____________________。
(2)反应②的反应类型是_________________,A的名称是__________________。
(3)反应①发生所需的试剂是____________________________________。反应⑥的化学方程式为___________________________________________________。
(4)D的分子式是_______________________,与D具有相同官能团的同分异构体有多种,
其中一种的结构简式为______________________。
(5)设计一条以溴乙烷为原料合成乳酸(![]() )的路线(其它试剂任选,合成路线常用的表示方式为:
)的路线(其它试剂任选,合成路线常用的表示方式为:![]() )。___________________________________________。
)。___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应
B. 在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热
C. 物质燃烧都需要氧气
D. 物质燃烧放出热量的多少与外界条件有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:3C+2K2Cr2O7 +8H2SO4===3CO2↑+2K2SO4
+2Cr2(SO4)3 +8H2O。
(1)请用双线桥法标出电子转移方向和数目________________________________。
(2)上述反应中氧化剂是______(填化学式),被氧化的元素是________(填元素符号)。
(3)H2SO4 在上述反应中表现出来的性质是____________(填序号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的固定有三种途径:生物固氮、自然固氮和工业固氮。根据最新“人工固氮”的研究报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分平衡时实验数据见下表(光照、N2压力1.0×105Pa、反应时间1 h):
T/K | 303 | 313 | 323 | 353 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
相应的化学方程式:2N2(g)+6H2O(l)![]() 4NH3(g)+3O2(g) ΔH=a kJ·mol-1
4NH3(g)+3O2(g) ΔH=a kJ·mol-1
回答下列问题:
(1)此合成反应的a________0;(填“>”、“<”或“=”)
(2)从323 K到353 K,氨气的生成量减少的可能原因是_______________________________;(3)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议__________________________________________________。
(4)工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,分别研究在T1、T2和T3(T1<T2<T3)三种温度下合成氨气的规律。下图是上述三种温度下不同的H2和N2的起始组成比(起始时N2的物质的量均为1 mol)与N2平衡转化率的关系。请回答:
2NH3(g) ΔH=-92.4 kJ·mol-1,分别研究在T1、T2和T3(T1<T2<T3)三种温度下合成氨气的规律。下图是上述三种温度下不同的H2和N2的起始组成比(起始时N2的物质的量均为1 mol)与N2平衡转化率的关系。请回答:

①在上述三种温度中,曲线X对应的温度是________。
②a、b、c三点中H2的转化率最小的是_______点、转化率最大的是________点。
③在容积为1.0 L的密闭容器中充入0.30 mol N2(g)和0.80 molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。该条件下反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数为__________________。
N2(g)+3H2(g)的平衡常数为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙烯并进行性质实验,装置如图,下列说法错误的是
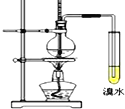
A. 乙醇发生消去反应生成乙烯
B. 实验中溴水褪色即可证明产生了乙烯
C. 制取乙烯反应中浓硫酸的主要作用为催化剂和脱水剂
D. 控制该反应温度在170℃左右,有利于减少副反应发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,对于pH=11的氨水,下列判断正确的是
A. 该氨水的浓度为1.0×10-3mol·L-1
B. 加水稀释,溶液中所有离子的浓度均减小
C. 加水稀释,溶液中c(NH4+)/c(NH3·H2O)变大
D. 与pH=3的盐酸等体积混合,反应后溶液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习.下列物质的分类不正确的是( )
A.SO2(氧化物)
B.碘酒(单质)
C.HNO3(含氧酸)
D.氯水(混合物)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com