
【题目】某酸件废水可能含有Fe2+、Fe3+、Al3+、Mg2+、Na+、K+、CO32-、SO42-。取废水祥品分别进行如图所示①~④四个实验。下列推断正确的是
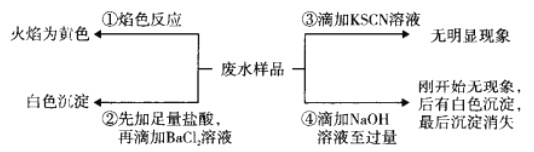
A. 废水含有Na+,不含K+
B. 废水含有SO42-和CO32-
C. 废水不含Fe3+,可能含Fe2+
D. 废水一定含有Na+、Al3+、SO42-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】苯酚(结构简式如图所示),俗称石炭酸。是一种重要的化工原料,广泛用于制适酚醛树脂、染料、医药、农药等。下列说法不正确的是( )
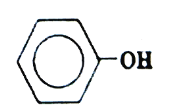
A.分子中所有原子可能共平面
B.固体苯酚分子间可能形成氢键
C.![]() 该分子充分燃烧,会消耗
该分子充分燃烧,会消耗![]()
D.![]() 该分子与足量的氢气加成后,环上的一氯取代物有3种
该分子与足量的氢气加成后,环上的一氯取代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中,发生以下反应:2A(g)+ B(g) ![]() 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是( )
A. 1.6 mol B. 2.8 mol
C. 2.4 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应:3A(g)![]() 2B(g)+D(g)在四种不同条件下进行,B、D的起始浓度为0,反应物A的浓度c随时间t的变化情况如表:
2B(g)+D(g)在四种不同条件下进行,B、D的起始浓度为0,反应物A的浓度c随时间t的变化情况如表:
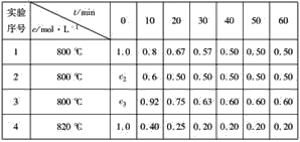
根据上述数据,完成下列填空:
(1)c2=______ mol·L-1。
(2)在实验1和2中,有一个实验使用了催化剂,根据表中数据判断,使用催化剂的实验为_______________,理由是__________________________
(3)求在实验4中,反应在0~10 min内反应物A的平均反应速率为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)![]() 2C(g) △H>0,其他条件不变,只有温度改变时,某量随温度变化的关系如图所示。则下列说法正确的是
2C(g) △H>0,其他条件不变,只有温度改变时,某量随温度变化的关系如图所示。则下列说法正确的是
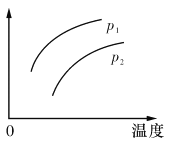
A.P1>P2,纵坐标可表示A的质量分数
B.P1<P2,纵坐标可表示C的质量贫数
C.P1>P2,纵坐标可表示混合气体的平均摩尔质量
D.P1<P2,纵坐标可表示A的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.( ![]() -
-![]() ) mol/LB.(2b-a) mol/L
) mol/LB.(2b-a) mol/L
C.(5b-![]() ) mol/LD.(10b-5a) mol/L
) mol/LD.(10b-5a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如下实验探究铁钉在不同溶液中的吸氧腐蚀。
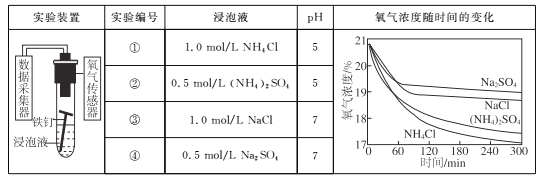
下列说法不正确的是
A. 上述正极反应均为O2+4e-+2H2O=4OH-
B. 在不同溶液中,Cl是影响吸氧腐蚀速率的主要因素
C. 向实验④中加入少量(NH4)2SO4固体,吸氧腐蚀速率加快
D. 在300 min内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,锂电池已扩展到镍酸锂、钴酸锂、硅碳负极、磷酸铁锂等电池体系。请回答下列问题:
(1)基态Ni原子的价电子排布式为________,与Ni同周期且基态原子核外的成单电子数与Ni相同的元素还有__________种。
(2)酞菁钴分子的结构简式如图所示,中心离子为钴离子,分子中氮原子的杂化类型为___。
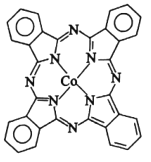
(3)Li+过度脱出易导致锂电池结构坍塌产生O2而爆炸。实验证实O2因具有单电子而成为顺磁性分子。下列结构式(黑点代表电子)中最有可能代表O2分子结构的是__(填字母)。
A ![]() B
B ![]() C
C ![]() D
D ![]()
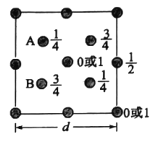
(4)如图为SiO2晶胞中Si原子沿z轴方向在xy平面的投影图(即俯视投影图),其中O原子略去,Si原子旁标注的数字表示每个Si原子位于z轴的高度,则SiA与SiB的距离是______。
(5)PCl5晶体的晶胞如图所示,该晶体熔融时形成一种能导电的液体,实验测得其中含有一种正四面体阳离子和一种正八面体阴离子,且P—Cl键的键长只有198pm和206pm两种,试用电离方程式解释PCl5熔体能导电的原因____,正四面体形阳离子中键角大于PCl3的键角原因为_____。已知该晶体的晶胞边长为apm,NA为阿伏伽德罗常数的值,则该晶体的密度为__________g·cm-3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com