
【题目】下列说法正确的是
A.32![]() 中含有的氧原子数是2×6.02×1023
中含有的氧原子数是2×6.02×1023
B.N2和CO共1mol的混合气体中含有的分子总数是2×6.02×1023
C.2.3 g Na与O2完全反应生成3.6 g产物时失电子数是0.1×6.02×1023
D.1.0 L 0.1 mol·L-1NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,密闭容器中的H2在催化剂的催化下可高效转化酸性溶液中的硝态氮(![]() )以达到消除污染的目的。其工作原理的示意图如图:
)以达到消除污染的目的。其工作原理的示意图如图:
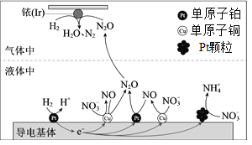
下列说法正确的是
A.导电基体上的正极产物仅有NO和![]()
B.若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量
C.若导电基体上只有单原子铜,![]() 能全部转化为N2O
能全部转化为N2O
D.若Ir的表面处理1molN2O,理论上负极消耗89.6LH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
A. ![]() ,
,![]() 完全反应转移的电子数为
完全反应转移的电子数为![]()
B. 用电解粗铜的方法精炼铜,当电路中通过的电子数为![]() 时,阳极应有
时,阳极应有![]() 转化为
转化为![]()
C. 常温下,![]() 的
的![]() 溶液中,水电离出的
溶液中,水电离出的![]() 数为
数为![]()
D. ![]() 浓度为
浓度为![]() 的
的![]() 溶液中,阴离子数为
溶液中,阴离子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝的气体Y,Y为纯净物;取![]() ,用含
,用含![]() 的盐酸完全溶解得溶液A,将溶液A分成
的盐酸完全溶解得溶液A,将溶液A分成![]() 和
和![]() 两等份,完成如下实验(白色沉淀C可溶于
两等份,完成如下实验(白色沉淀C可溶于![]() 溶液):
溶液):
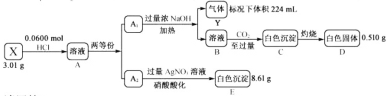
请回答:
(1)组成X的四种元素是N、H和_______(填元素符号),X的化学式是_________。
(2)溶液B通入过量![]() 得到白色沉淀C的离子方程式是______________。
得到白色沉淀C的离子方程式是______________。
(3)写出一个化合反应(用化学方程式或离子方程式表示)_____________。要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“![]() ”相同。
”相同。
Ⅱ.某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有白雾,烧杯中出现白色沉淀。请回答:
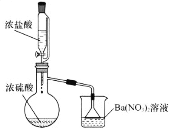
(1)将浓硫酸和浓盐酸混合可产生![]() 气体的原因是________。
气体的原因是________。
(2)烧杯中出现白色沉淀的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(用元素符号或化学式回答下列问题)
(1)在这些元素中,化学性质最不活泼的是_______,其原子结构示意图是_________。
(2)用电子式表示元素④与⑦组成的化合物的形成过程:________,该化合物属于_______(填“共价”或“离子”)化合物。
(3)常温下呈液态的非金属单质是_______。
(4)表中能形成两性氢氧化物的元素是_________,该元素的单质与⑨的最高价氧化物的水化物反应的化学方程式是___________。
(5)①、⑥、⑦三种元素的最高价氧化物对应的水化物中,按酸性增强的顺序排列为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电子排布的表述正确的是( )
A.![]() 可表示单核8电子粒子基态时电子排布
可表示单核8电子粒子基态时电子排布
B.![]() 此图错误,违背了洪特规则
此图错误,违背了洪特规则
C.2p3表示基态氮原子的外围电子排布式
D.![]() 表示处于激发态的硼原子的电子排布图
表示处于激发态的硼原子的电子排布图
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
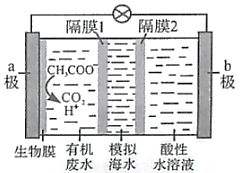
A.负极反应为 ![]()
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________。
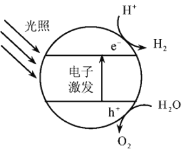
(2)若将该催化剂置于Na2SO3溶液中,产物之一为![]() ,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):![]()
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a molL-1和3 a molL-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为___________。
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。
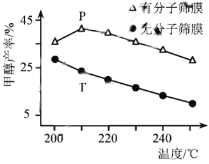
①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5) ![]() 的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,
的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,![]() =1:_______:__________。
=1:_______:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com