
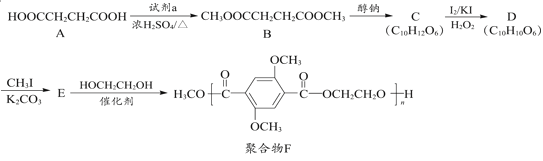
【题目】有机物A是一种重要的化工原料,用A制取新型聚合物F的合成路线如图:
已知:
ⅰ.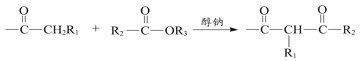 +R3OH
+R3OH
ⅱ. +R1I
+R1I +HI
+HI
ⅲ.R1COOR2+R3OH![]() R1COOR3+R2OH
R1COOR3+R2OH
回答下列问题:
(1)A中官能团的结构简式为___。
(2)试剂a的名称___。1molD与足量的氢氧化钠溶液反应所需氢氧化钠的物质的量___。
(3)C中含有一个六元环,C的结构简式为___。
(4)C→D的反应类型为___。
(5)E→F的化学方程式是___。
(6)下列说法正确的是___(填序号)。
a.A能与NaHCO3溶液反应
b.醇钠可由醇与氢氧化钠反应制得
c.用FeCl3溶液不能鉴别D和E
d.HOCH2CH2OH俗称甘油
【答案】羧基 甲醇 4 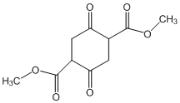 氧化反应
氧化反应 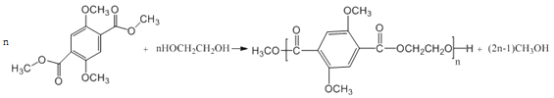 a
a
【解析】
比较B和A的结构简式可知,A发生酯化反应生成B,所以试剂a为CH3OH,根据C的化学式及B到C的条件可知,B发生信息i中的反应得C为: ,C发生氧化反应得D为
,C发生氧化反应得D为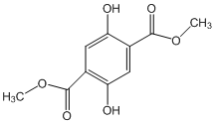 ,D发生信息ii中的反应生成E为
,D发生信息ii中的反应生成E为 ,E发生缩聚反应得F。
,E发生缩聚反应得F。
(1)根据A的结构简式可知,A中官能团的名称为羧基,故答案为:羧基;
(2)根据上面的分析可知,a为CH3OH,名称为甲醇;由分析可知D的结构为: ,能与NaOH溶液反应的官能团有酚羟基、酯基,1molD与足量的氢氧化钠溶液反应所需氢氧化钠的物质的量为4mol故答案为:甲醇;4;
,能与NaOH溶液反应的官能团有酚羟基、酯基,1molD与足量的氢氧化钠溶液反应所需氢氧化钠的物质的量为4mol故答案为:甲醇;4;
(3)根据上面的分析可知,C的结构简式为 ;
;
(4)C发生氧化反应得D,C→D的反应类型为氧化反应,故答案为:氧化反应;
(5)E发生缩聚反应得F,E→F的化学方程式是:
 ;
;
(6)a.A中含有羧基,A能与NaHCO3溶液反应,故a正确;
b.醇与金属钠反应得到醇钠和氢气,醇与NaOH不反应,故b错误;
c.D中有酚羟基,而E中没有,所以可用FeCl3溶液鉴别D和E,故c错误;
d.HOCH2CHOHCH2OH俗称甘油,故d错误,
故答案为:a。


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】从海水中提取金属镁的工艺流程可简单图示如下:

(1)步骤①的目的是将海水中的Mg2+沉淀为Mg(OH)2,若浓缩海水中c(Mg2+)=2.0 mol·L-1,Mg2+开始形成沉淀时溶液的pH约为________(已知Ksp[Mg(OH)2]=1.8×10-11,log3=0.48)
(2)步骤③的操作由蒸发浓缩,______,过滤,_______四个环节组成。
(3)步骤④是在HCl气流中加热晶体得到无水MgCl2,简要说明HCl气体的作用_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:

(1)通入氧气的电极为_____(填“正极”或“负极”),通氢气一极的电极反应式为_________________;
(2)铁电极为_______(填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________。
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为______g;
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH:
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe3+ | 1.9 | 3.2 |
Fe2+ | 7.0 | 9.0 |
Cu2+ | 4.7 | 6.7 |
①步骤I中加入试剂A的目的是_____________________________,试剂A应选择______(填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因_____________________________________________________;
②步骤II中试剂B为_________,调节pH的范围是___________;
③步骤III的操作是加热浓缩、_______、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,反应室(容积恒定为2L)中有反应:A(g)+2B(g)=C(g)。不能说明上述反应达到平衡状态的是( )
A.反应中A与B的物质的量浓度之比为1:2
B.混合气体总物质的量不再变化
C.混合气体的平均摩尔质量不随时间的变化而变化
D.2v正(A)=v逆(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计能达到相应实验目的是![]()
选项 | 实验设计 | 实验目的 |
A | 在热的NaOH溶液中滴入饱和 | 制备 |
B | 将 | 验证 |
C | 向含少量 | 除去 |
D | 将 | 比较 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂用闪锌矿制备锌及颜料 A(红棕色固体)的工艺流程如下图所示。(闪锌矿的主要成分为 ZnS,同时含有 10%的 FeS 及少量 CuS)
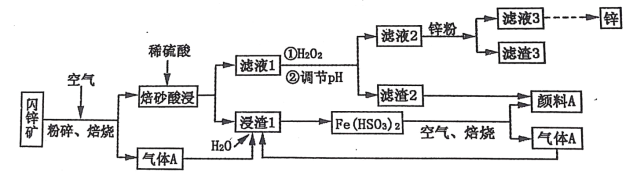
已知:①闪锌矿在焙烧时会生成副产物 ZnFeO4,ZnFeO4 不溶于水及硫酸。Fe(HSO3)2 难溶于水。②Ksp[Fe(OH)3]=1×10-39。
完成下列问题
(1)闪锌矿粉碎的目的是_______________________________________________________。
(2)“滤液 1”中选用足量的 H2O2,理由是_____________________。假设“②调节 pH"前,滤液 1 中 c(Fe3+)=1molL-1 ,则 Fe3+ 完全沉淀时的 pH 至少为____________________。(离子浓度≤ 10-6mol·L-1 规为完全除去)。
(3)“滤渣 3”的成分为__________________________________ (写化学式)。
(4)设计一种检验“颜料 A”中是否含有 Fe2+的实验方案_______________________________________________________。
(5)“气体 A”与“浸渣 1”反应的化学方程式为_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某高能锂离子电池的总反应为:2Li+FeS= Fe +Li2S,电解液为含LiPF6.SO(CH3)2的有机溶液(Li+可自由通过)。某小组以该电池为电源电解废水并获得单质镍,工作原理如图所示。

下列分析正确的是
A. 该锂离子电池正极反应为FeS+2Li++2e-=Fe +Li2S
B. X与电池的Li电极相连
C. 电解过程中c(BaC12)保持不变
D. 若去掉阳离子膜将左右两室合并,则X电极的反应不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.NH3的摩尔质量等于NA个氨分子的质量之和
B.标准状况下,22.4L单质溴所含的分子数为NA
C.标准状况下,1mol Cl2与足量Fe完全反应,转移的电子数为3NA
D.常温常压下,48g O2和O3的混合气体含有氧原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 聚合物![]() 可由单体CH3CH=CH2和CH2=CH2加聚制得
可由单体CH3CH=CH2和CH2=CH2加聚制得
B. 戊烷(C5H12)有两种同分异构体
C. 乙烯、聚乙烯和苯分子均含有碳碳双键
D. 糖类、油脂和蛋白质均可发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com