
【题目】测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与 I-反应生成 I3-,并在溶液中建立如下平衡: I2+I-![]() I3-。通过测平衡体系中 c(I2)、 c(I-)和 c(I3-),就可求得该反应的平衡常数。
I3-。通过测平衡体系中 c(I2)、 c(I-)和 c(I3-),就可求得该反应的平衡常数。
Ⅰ.某同学为测定上述平衡体系中 c(I2),采用如下方法:取 V1 mL 平衡混合溶液,用cmol·L-1的Na2S2O3溶液进行滴定(反应为 I2+2Na2S2O3=2NaI+Na2S4O6),消耗 V2 mL 的Na2S2O3溶液。根据V1、V2和c可求得c(I2)。
(1)上述滴定时,可采用________做指示剂,滴定终点的现象是_____________________。
(2)下列对该同学设计方案的分析,正确的是________(填字母)。
A.方案可行。能准确测定溶液中的 c(I2)
B.不可行。因为 I-能与 Na2S2O3发生反应
C.不可行。只能测得溶液中 c(I2)与 c(I3-)之和
Ⅱ.化学兴趣小组对上述方案进行改进,拟采用下述方法来测定该反应的平衡常数(室温条件下进行,溶液体积变化忽略不计):

已知: ①I-和 I3-不溶于 CCl4; ②一定温度下, 碘单质在四氯化碳和水混合液体中,碘单质的浓度比值即![]() 是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
(3)操作Ⅰ使用的玻璃仪器中,除烧杯、玻璃棒外,还需要的仪器是________(填名称)。试指出该操作中应注意的事项为________。 (任写一条)
(4)上述测定过程均正常操作,下层液体中碘单质的物质的量浓度是________;若终点读数时俯视滴定管, 则会造成所测浓度________ (填“等于”、 “大于”或“小于”)该值。
(5)实验测得上层溶液中 c(I3-)=0.0049 mol·L-1,结合上述有关数据,计算室温条件下反应 I2+I-![]() I3-的平衡常数 K=________(用具体数据列出计算式即可)。
I3-的平衡常数 K=________(用具体数据列出计算式即可)。
【答案】
(1)淀粉 ;溶液由蓝色变为无色,且半分钟后颜色不再改变
(2)C;
(3)分液漏斗;分液时上层液体应从上口倒出,下层液体应从下口放出(或分液漏斗末端应紧靠烧杯内壁或打开上口活塞,使分液漏斗内外压强相等便于液体流下等。其他合理答案也给分)
(4)0.085 mol/L;小于;
(5)49000/51(或 961) L· mol-1;
【解析】
试题分析:(1)取V1 mL平衡混合溶液,用c molL-1的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),指示剂选择淀粉,滴入最后一滴溶液由蓝色变化为无色,半分钟不变化证明反应达到终点,故答案为:淀粉;溶液由蓝色变无色,且半分钟后颜色不再改变;
(2)碘单质能与I-反应成I3-,并在溶液中建立如下平衡:I2+I-![]() I3-;A.方案不可行.依据操作的化学平衡分析可知,测定的是碘单质和I3-的含量,不能准确测定溶液中的c(I2),故A错误;B.不可行.因为I-不能与Na2S2O3发生反应,是碘单质和Na2S2O3发生反应,故B错误;C.不可行.依据操作的平衡可知,实验只能测得溶液中c(I2)与c(I3-)之和,不能测定离子浓度,故C正确;故答案为:C;
I3-;A.方案不可行.依据操作的化学平衡分析可知,测定的是碘单质和I3-的含量,不能准确测定溶液中的c(I2),故A错误;B.不可行.因为I-不能与Na2S2O3发生反应,是碘单质和Na2S2O3发生反应,故B错误;C.不可行.依据操作的平衡可知,实验只能测得溶液中c(I2)与c(I3-)之和,不能测定离子浓度,故C正确;故答案为:C;
(3)步骤Ⅰ是分液操作,需要用到的玻璃容器,除烧杯、玻璃棒外,还有分液漏斗,用分液漏斗分液时上层液体应从上口倒出,下层液体应从下口放出;分液漏斗末端应紧靠烧杯内壁或打开上口活塞,使分液漏斗内外压强相等便于液体流下等,故答案为:分液漏斗;分液时上层液体应从上口倒出,下层液体应从下口放出;分液漏斗末端应紧靠烧杯内壁或打开上口活塞,使分液漏斗内外压强相等便于液体流下等;
(4)依据化学反应可知设碘单质物质的量为x;
I2+2Na2S2O3=2NaI+Na2S4O6,
1 2
x 0.1mol/L×0.017L
x=0.00085mol ,浓度=![]() =0.085mol/L,若终点读数时俯视滴定管,导致消耗的标准液的体积偏小,则会造成所测浓度小于0.085mol/L,故答案为:0.085mol/L;小于;
=0.085mol/L,若终点读数时俯视滴定管,导致消耗的标准液的体积偏小,则会造成所测浓度小于0.085mol/L,故答案为:0.085mol/L;小于;
(5)依据![]() =85,计算得到水溶液中碘单质的浓度c(I2)=0.001mol/L;10ml溶液中c(I3-)=0.049molL-1,物质的量0.00049mol,所以反应的碘离子物质的量为0.00049mol,平衡状态碘离子物质的量=0.1mol/L×0.01L=0.001mol-0.00049mol=0.00051mol,浓度c(I-)=0.051mol/L,I2+I-I3-;平衡常数K=
=85,计算得到水溶液中碘单质的浓度c(I2)=0.001mol/L;10ml溶液中c(I3-)=0.049molL-1,物质的量0.00049mol,所以反应的碘离子物质的量为0.00049mol,平衡状态碘离子物质的量=0.1mol/L×0.01L=0.001mol-0.00049mol=0.00051mol,浓度c(I-)=0.051mol/L,I2+I-I3-;平衡常数K=![]() =
=![]() =961L/mol,故答案为:961L/mol。
=961L/mol,故答案为:961L/mol。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(12分)A~G各物质间的关系如下图,其中B、D为气态单质。
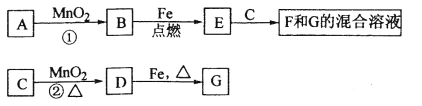
请回答下列问题:
(1)物质C和E的名称分别为 、 ;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为 ;
若只能在加热情况下进行,则反应物A的化学式(分子式)为 ;
(3)反应②的化学方程式为 ;
(4)新配制的F溶液应加入 以防止其转化为G。检验G溶液中阳离子的常用试剂是 (填化学式),实验现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂
D.侯德榜创立联合制碱法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下,回答下列问题:
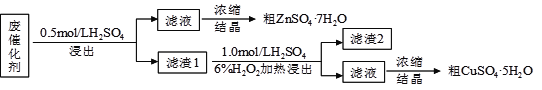
已知:ZnS与稀硫酸反应,且化合价不变; CuS既不溶解于稀硫酸,也不与稀硫酸反应
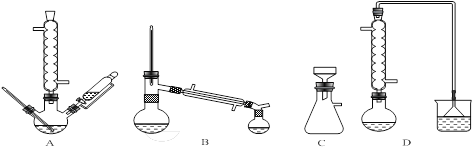
(1)在下列装置中,第一次浸出反应装置最合理的___________(填标号)。
(2)滤液1中含有Fe2+,选用提供的试剂进行检验,检验方法如下: 。
(提供的试剂:稀盐酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水)
(3)本实验要用到抽滤,设所用的洗涤剂为X,抽滤洗涤沉淀的操作 。
(4)写出第二次浸出的化学反应方程式 ,向盛有滤渣1的反应器中加H2SO4和H2O2溶液,应先加 。
(5)滤渣2的主要成分是 。浓缩、结晶得到硫酸锌晶体的主要仪器名称是 。
(6)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,容积为2 L的恒容密闭容器中,通入2 mol N2、3 mol H2进行反应N2(g)+3H2(g) ![]() 2NH3(g),20 min后,N2的物质的量为1.9 mol,1 h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是:
2NH3(g),20 min后,N2的物质的量为1.9 mol,1 h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是:
A.当容器内压强不改变时,说明反应已达到平衡状态
B.增加H2的浓度或降低温度,平衡将向正反应方向移动,且反应速率均加快
C.前20 min用NH3表示的反应速率为0.01 mol·L-1·min-1
D.1 h后反应进行完全,容器中的N2浓度为0.55 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1 : 1的化合物N是常见的有机溶剂。
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为____________,属于___________分子(填“极性”或“非极性”),E的基态原子的外围电子排布式为____________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为____________。
(3)C元素形成含氧酸酸性强弱:HNO3____________HNO2(填“>”或“<”)NO3—的空间构型是___________,NO2—中心原子的杂化方式为___________
(4)下列叙述正确的是____________(填序号)。
A. M是极性分子,N是非极性分子
B. M和BD2分子中的中心原子均采用sp2杂化
C. N分子中含有6个σ键和1个大π键
D. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5)已知:①E的一种氧化物Q,其晶胞结构如图所示:

①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECl4和BD气体的热化学方程式:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同一温度下,强电解质溶液a、弱电解质溶液b、金属导体c三者的导电能力相同,若升高温度后,它们的导电能力强弱顺序是( )
A. b>a>c B. a=b=c
C. c>a>b D. b>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 1 L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1 mol/L
B. 从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C. 配制500mL0.1 mol·L-1的CuSO4溶液,需8.0g 无水CuSO4
D. 中和100mL1mol/L的H2SO4溶液,需NaOH为4.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A经如图所示的过程转化为D。已知D为强酸或强碱,请回答下列问题:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)若常温下C是红棕色的气体,则:
①A的化学式可能是:A__________,C转化D的过程中,氧化剂和还原剂的质量之比为______
②若A能使湿润的红色石蕊试纸变蓝,则A转化为B反应的化学方程式为____________________________________ 。
③D的浓溶液在常温下可与铜反应,请写出该反应的离子方程式________________________
(2)若A为金属单质,C为淡黄色固体,则C的电子式为_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com