
【题目】某研究小组以绿矾(FeSO47H2O)为原料制备化合物A[K3Fe(Ⅲ) (C2O4)xyH2O]并通过如下实验步骤确定A的化学式:
步骤1:准确称取A样品4.91g,干燥脱水至恒重,残留物质量为4.37g;
步骤2:将步骤1所得固体溶于水,经测定含Fe3+0.0l00mol;
步骤3:准确称取A样品4.91g置于锥形瓶中,加入足量的3. 00mol-L'1的H2SO4,溶液和适量蒸馏水,用0.500molL-1的KMnO4溶液滴定,当MnO4-恰好完全被还原为 Mn2+时,消耗KMnO4溶液的体积为24.00 mL。
请回答下列问题:
(1)绿矾(FeSO47H2O)若保存不当或长期放置,易与空气中的氧气反应,该反应中 FeSO4表现的性质为_____(填字母)。
A.氧化性 B.还原性 C.氧化性和还原性 D.酸性
(2)用物质的量浓度为18.0 molL-1的浓硫酸配制100mL3.00 molL-1的H2SO4溶液时,量取浓硫酸需要的量筒规格为_____(填字母)。
A.10mL B.25mL C.50mL D.l00mL
(3)步骤2发生的离子反应如下,将该离子方程式配平:_____MnO4-+_____ C2O42-+_____H+=_____Mn2++_____CO2↑+_____H2O。
通过计算确定化合物A中x、y的值(请写出计算过程)。_____________
【答案】B B 2 5 16 2 10 8 n(H2O)=(4.910g-4.370g)/18g·mol-1=0.03000mol,由方程式确定n(C2O42-)=5/2×n(KMnO4)=5/2×0.5000mol·L-1×0.02400L=0.03000mol n(Fe3+):n(C2O42-):n(H2O)=0.01000mol:0.03000mol:0.03000mol=1:3:3 ,解之得:x=3 、y=3。
【解析】
(1)FeSO47H2O与空气中的氧气反应,铁元素化合价从+2→+3,铁元素别氧化,FeSO4表现的性质为还原性。
(2)物质的量浓度为18.0 molL-1的浓硫酸配制100mL3.00 molL-1的H2SO4溶液时,利用 c1V1=c2V2,18.0 molL-1×V1=3.00 molL-1×100mL,V1=16.7mL。
(3)反应中MnO4-反应为Mn2+,锰元素从+7价变为+2价,C2O42-反应为CO2,碳元素从+3价变为+4价,在该反应中,利用氧化还原反应总化合价得失相等、电子得失数目相等进行计算。
化合物A[K3Fe(Ⅲ) (C2O4)xyH2O]中各部分物质的量n(H2O)=(4.910g-4.370g)/18g·mol-1=0.03000mol,n(Fe3+)=0.01mol,n(C2O42-)=![]() ×n(KMnO4)=
×n(KMnO4)=![]() ×0.5000mol·L-1×0.024L=0.03mol。
×0.5000mol·L-1×0.024L=0.03mol。
(1)绿矾与空气中的氧气反应,铁元素化合价从+2→+3,该反应中 FeSO4表现的性质为还原性。答案为B。
(2)用物质的量浓度为18.0 molL-1的浓硫酸配制100mL3.00 molL-1的H2SO4溶液时,由稀释定律可知, 18.0 molL-1×V1=3.00 molL-1×100mL,解之得V1=16.7mL,可以选择25mL的量筒。答案为:B。
(3)反应中MnO4-反应为Mn2+,锰元素从+7价变为+2价,每个MnO4-得到5个电子,C2O42-反应为2CO2,碳元素从+3价变为+4价,每个C2O42-失去2个电子,最小公倍数为10。离子方程式配平为:2MnO4-+5C2O42-+16H+ = 2Mn2++10CO2↑+8H2O。
通过计算可知化合物A[K3Fe(Ⅲ) (C2O4)xyH2O]中各部分物质的量n(H2O)=(4.910g-4.370g) ÷18g·mol-1=0.03mol,n(Fe3+)=0.01mol,n(C2O42-)=![]() ×n(KMnO4)=
×n(KMnO4)=![]() ×0.5000mol·L-1×0.024L=0.03mol。n(Fe3+):n(C2O42-):n(H2O)=0.01mol:0.03mol:0.03mol=1:3:3 ,解之得:x=3 、y=3。
×0.5000mol·L-1×0.024L=0.03mol。n(Fe3+):n(C2O42-):n(H2O)=0.01mol:0.03mol:0.03mol=1:3:3 ,解之得:x=3 、y=3。
答案为:2MnO4-+5C2O42-+16H+ = 2Mn2++10CO2↑+8H2O;n(H2O)=(4.910g-4.370g) ÷18g·mol-1=0.03mol,n(Fe3+)=0.01mol,n(C2O42-)=![]() ×n(KMnO4)=
×n(KMnO4)=![]() ×0.5000mol·L-1×0.024L=0.03mol。n(Fe3+):n(C2O42-):n(H2O)=0.01mol:0.03mol:0.03mol=1:3:3 ,解之得:x=3、 y=3。
×0.5000mol·L-1×0.024L=0.03mol。n(Fe3+):n(C2O42-):n(H2O)=0.01mol:0.03mol:0.03mol=1:3:3 ,解之得:x=3、 y=3。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】2002年诺贝尔化学奖表彰了两项成果,其中一项是瑞士科学家库尔特·维特里希“发明了利用核磁共振技术测定溶液中生物大分子三维结构的方法”。在化学上经常使用的是氢核磁共振谱,它是根据不同化学环境的氢原子在氢核磁共振谱中给出的信号不同来确定有机物分子中氢原子种类的。下列有机物分子中,在氢核磁共振谱中信号强度(个数比)是1:3的是
A. 1,2,3-三甲基苯 B. 丙烷
C. 异丙醇 D. 甲酸叔丁酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于蛋白质在人体内的生理功能的说法中,不正确的是
A. 构成和修补人体组织 B. 构成骨骼的主要成分
C. 构成酶和激素的主要成分 D. 构成抗体的主要成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol·L-1NaOH溶液滴定新配制的25.0mL0.02 mol·L-1FeSO4溶液,应用手持技术测定溶液的pH与时间(t)的关系,结果如右图所示。下列说法错误的是
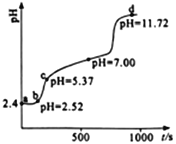
A. ab段,溶液中发生的主要反应:H++OH-=H2O
B. bc段,溶液中c(Fe2+) > (Fe3+) >c(H+)>c(OH-)
C. d点,溶液中的离子主要有Na+、SO42-、OH-
D. 滴定过程发生了复分解反应和氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过二硫酸钾(K2S2O8) 在科研与工业上有重要用途。
(1)S2O82-的结构式为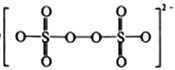 ,其中S元素的化合价为_________________。在Ag+催化下,S2O82-能使含Mn2+的溶液变成紫红色,氧化产物是___________(填离子符号)。
,其中S元素的化合价为_________________。在Ag+催化下,S2O82-能使含Mn2+的溶液变成紫红色,氧化产物是___________(填离子符号)。
(2)某厂采用湿法K2S2O8氧化脱硝和氨法脱硫工艺综合处理锅炉烟气,提高了烟气处理效率,处理液还可以用作城市植被绿化的肥料。
①脱硫过程中,当氨吸收液的pH=6时,n(SO32-)∶n(HSO3-) =________。
[巳知:25℃时,Ka1(H2SO3)=1.5×10-2,K a2(H2SO3)=1.0×10-7]
②脱硝过程中依次发生两步反应:第1步,K2S2O8将NO氧化成HNO2,第2步,K2S2O8继续氧化HNO2,第2步反应的化学方程式为______________________________________;
一定条件下,NO去除率随温度变化的关系如右图所示。80℃时,若NO初始浓度为450mg·m-3,t min达到最大去除率,NO去除的平均反应速率:
v(NO) =____mol·L-1·min-1(列代数式)
(3)过二硫酸钾可通过“电解→转化→提纯”方法制得,电解装置示意图如右图所示。
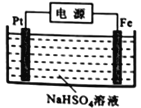
①电解时,铁电极连接电源的_________________极。
②常温下,电解液中含硫微粒的主要存在形式与pH的关系如下图所示。
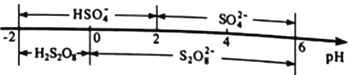
在阳极放电的离子主要是HSO4-,阳极区电解质溶液的pH范围为_________,阳极的电极反应式为________________________。
③往电解产品中加入硫酸钾,使其转化为过二硫酸钾粗产品,提纯粗产品的方法_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:

(1)两种物质混合能发生反应且都是电解质的是________(填分类标准代号,下同),两种物质都是氧化物的是________。
(2)分类标准代号A表示______________(多项选择)
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:__________________________________。
(4)用洁净的烧杯取25 mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热得红褐色胶体,该反应的化学方程式为: ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是混合物分离的实验,请回答有关问题
实验:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示
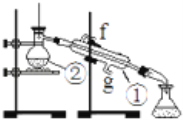
(1)写出下列仪器的名称:①________②________。
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是________,图中装置中进水口是________。(填“f”或“g”)
(3)仪器①中常加入碎瓷片,这样做的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓硫酸和乙醇制乙烯的装置如图所示,对下列操作或现象描述正确的是( )
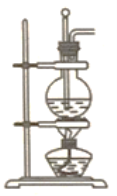
A. 圆底烧瓶中先加浓硫酸再加入乙醇
B. 实验得到的气体能使溴水褪色说明有乙烯生成
C. 反应中圆底烧瓶内会产生黑色固体
D. 用排水法或向下排空气法收集乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com