



 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
 柠檬酸铁可用作食品铁质强化剂、营养增补剂,用于饼干、钙质奶粉等,它可以由柠檬酸(熔点为153°C)与氢氧化铁制得.其结构如图.
柠檬酸铁可用作食品铁质强化剂、营养增补剂,用于饼干、钙质奶粉等,它可以由柠檬酸(熔点为153°C)与氢氧化铁制得.其结构如图.查看答案和解析>>
科目:高中化学 来源: 题型:
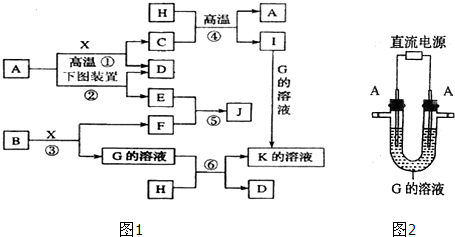
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据△H可以判断此反应是放热反应还是吸热反应 |
| B、根据化学反应速率可以判断反应物转变为生成物的难易 |
| C、根据熵变还不可以判断化学反应能否自发进行 |
| D、根据化学平衡常数可以判断化学反应进行的限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol-CH3和1 mol OH-都含有10 nA个电子 |
| B、标准状况下3.36 L CCl4含碳原子数为0.15nA |
| C、2 molHF溶于水配成溶液中含F-2nA |
| D、46gNO2和N2O4混合气体中含氧原子数为2nA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y |
| Z | W |
| A、非金属性:Z<X<Y |
| B、W的原子序数可能是Y的原子序数的2倍 |
| C、气态氢化物稳定性:Y<W |
| D、四种元素中不可能有金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com