
����Ŀ����������Ҫ�ɷ��Ƕ���������ij��ѧʵ��С��ȡ1.0g��������Ʒ�ڿ����г������ʱ������Ӧ4FeS2+11O2![]() 2Fe2O3+8SO2(�������ʲ��μӷ�Ӧ)�����ɵ�SO2����ǡ�ñ�50mLFe2(SO4)3��Һ��ȫ���գ���������Һ�м�������BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ������13.98g���塣�ش��������⣺
2Fe2O3+8SO2(�������ʲ��μӷ�Ӧ)�����ɵ�SO2����ǡ�ñ�50mLFe2(SO4)3��Һ��ȫ���գ���������Һ�м�������BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ������13.98g���塣�ش��������⣺
(1)FeS2�ڿ���������ʱ�����ϼ����ߵ�Ԫ����__________��SO2��Fe2(SO4)3��Ӧ�Ļ�ѧ����ʽ��_________________��
(2)ԭFe2(SO4)3��Һ�����ʵ���Ũ��Ϊ_______����������FeS2����������Ϊ______��
(3)��ҵ������10 t��������������SO2�������������ᣬ�����Ͽ��Ƶ�98����Ũ������ٶ�______��(��ʽ����)
���𰸡�Fe��S SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4 0.3mol/L 90% 15 t
��������
(1)�ڷ�Ӧ4FeS2+11O2![]() 2Fe2O3+8SO2�У�FeԪ�ػ��ϼ��ɷ�ӦǰFeS2�е�+2�۱�Ϊ��Ӧ��Fe2O3�е�+3�ۣ����ϼ����ߣ�SԪ�ػ��ϼ��ɷ�ӦǰFeS2�е�-1�۱�Ϊ��Ӧ��SO2�е�+4�ۣ����ϼ����ߣ�OԪ�ػ��ϼ����ɷ�ӦǰO2�е�0�۱�Ϊ��Ӧ��Fe2O3��SO2�е�-2�ۣ����ϼ۽��͡�����FeS2�ڿ��������շ�Ӧ�У����ϼ����ߵ�Ԫ����Fe��SԪ�أ�SO2��Fe2(SO4)3����Һ�з�Ӧ����FeSO4��H2SO4������������ԭ��Ӧ�Ļ�ѧ����ʽ��SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4��
2Fe2O3+8SO2�У�FeԪ�ػ��ϼ��ɷ�ӦǰFeS2�е�+2�۱�Ϊ��Ӧ��Fe2O3�е�+3�ۣ����ϼ����ߣ�SԪ�ػ��ϼ��ɷ�ӦǰFeS2�е�-1�۱�Ϊ��Ӧ��SO2�е�+4�ۣ����ϼ����ߣ�OԪ�ػ��ϼ����ɷ�ӦǰO2�е�0�۱�Ϊ��Ӧ��Fe2O3��SO2�е�-2�ۣ����ϼ۽��͡�����FeS2�ڿ��������շ�Ӧ�У����ϼ����ߵ�Ԫ����Fe��SԪ�أ�SO2��Fe2(SO4)3����Һ�з�Ӧ����FeSO4��H2SO4������������ԭ��Ӧ�Ļ�ѧ����ʽ��SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4��
(2)��Ӧ������13.98g BaSO4�����ʵ���Ϊ��n(BaSO4)=![]() =0.06 mol��SO42-��Fe2(SO4)3��SO2��������Һ�з����ķ�ӦSO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4���������ݷ���ʽ��֪Fe2(SO4)3�뷴Ӧ������SO42-�����ʵ�����ϵ��1��4������ԭ50 mL��Һ�к���Fe2(SO4)3�����ʵ���Ϊn[Fe2(SO4)3]=
=0.06 mol��SO42-��Fe2(SO4)3��SO2��������Һ�з����ķ�ӦSO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4���������ݷ���ʽ��֪Fe2(SO4)3�뷴Ӧ������SO42-�����ʵ�����ϵ��1��4������ԭ50 mL��Һ�к���Fe2(SO4)3�����ʵ���Ϊn[Fe2(SO4)3]=![]() n(BaSO4)=
n(BaSO4)=![]() ��0.06 mol=0.015 mol������Fe2(SO4)3��Ũ��c[Fe2(SO4)3]=
��0.06 mol=0.015 mol������Fe2(SO4)3��Ũ��c[Fe2(SO4)3]=![]() =0.3 mol/L�����ݷ���ʽ�����ʷ�Ӧ��ϵ��֪n[Fe2(SO4)3]��n(SO2)=1��1����n(SO2)= n[Fe2(SO4)3]=0.015 mol����4FeS2+11O2
=0.3 mol/L�����ݷ���ʽ�����ʷ�Ӧ��ϵ��֪n[Fe2(SO4)3]��n(SO2)=1��1����n(SO2)= n[Fe2(SO4)3]=0.015 mol����4FeS2+11O2![]() 2Fe2O3+8SO2��֪n(FeS2)=
2Fe2O3+8SO2��֪n(FeS2)=![]() n(SO2)=
n(SO2)=![]() ��0.015 mol=0.0075 mol��������m(FeS2)=0.0075 mol��120 g/mol=0.9 g����û�������FeS2����������Ϊ
��0.015 mol=0.0075 mol��������m(FeS2)=0.0075 mol��120 g/mol=0.9 g����û�������FeS2����������Ϊ![]() ��100%=90%��
��100%=90%��
(3)����SԪ���غ�ɵù�ϵʽFeS2��2SO2��2H2SO4��1 mol FeS2��Ӧ����2 mol H2SO4����120��FeS2��ȫ��Ӧ�����2��98��H2SO4��������������FeS2�ĺ�����90%��10 t����������ȫ��Ӧ���Ƴ�98%����������Ϊx���ɵñ���ʽ![]() �����x=15 t��
�����x=15 t��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ijԪ�ص�ȫ��������(��λ��eV)���£�
I1 | I2 | I3 | I4 | I5 | I6 | I7 | I8 |
13.6 | 35.1 | 54.9 | 77.4 | 113.9 | 138.1 | 739.1 | 871.1 |
д����Ԫ�ؼ۵��ӹ����ʾʽ_______________��
(2)�����еĴ��� �����÷���![]() ��ʾ������ m ���������γɴ� �� ����ԭ������n ���������γɴ��� ���ĵ��������籽�����еĴ� �� ���ɱ�ʾΪ
��ʾ������ m ���������γɴ� �� ����ԭ������n ���������γɴ��� ���ĵ��������籽�����еĴ� �� ���ɱ�ʾΪ![]() ��
��
�����ж� SO2 �����һ����_______________�Թ¶Ե��ӡ�
��HN3��Ϊ�����ᣬ������Ϊ��ɫ�д̼�����ζ��Һ�塣N3-�ļ���Ϊ_______________��N![]() �еĴ��� ��Ӧ��ʾΪ_______________��
�еĴ��� ��Ӧ��ʾΪ_______________��
(3)���ݶԽ��߹���Be��Al �Ļ�ѧ�������ƣ�д�� Be(OH)2 �� NaOH ��Ӧ�����ӷ���ʽ��________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����0.1 mol��L��1NaOH��Һ�ֱ�ζ�20.00mL 0.1 mol��L��1������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ����
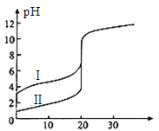
A.��ֱ��ʾ����ʹ���ĵζ�����
B.pH=7ʱ���ζ�����ʹ�������NaOH��Һ��������
C.V(NaOH)=10.00mLʱ��������Һ��c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
D.V(NaOH)=20.00mLʱ������Һ��c(CH3COO-)> c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����ǵ������������������Դ���õ�ϢϢ��ء��ش��������⣺
(1)�Ȼ��������ھ�ˮ��д��������ˮ�ĵ��뷽��ʽ��________�����Ȼ�����Һ�м������ۣ�������Ӧ�����ӷ���ʽ��___________�����Ȼ�����ˮ��Һ����μ�������������Һ���ɹ۲쵽��������__________��
(2)Ư�۳������ޡ��顢ֽ�ŵ�Ư��������������Ӿ�ؼ�������������Ư�۵���Ч�ɷ�Ϊ_________��д��Ư���ڿ�����ʧЧ���йػ�ѧ����ʽ��_________��________��
(3)pHС��5.6����Ȼ��ˮ��Ϊ���꣬�����������Ҫ������SO2��_________��ȼú�������Ч����������γɣ�ȼú�������ʯ�ҷ��⣬Ҳ������ú�м��뽬״Mg(OH)2��ʹȼ�ղ�����SO2ת��ΪMgSO4��д���÷�Ӧ�Ļ�ѧ����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W����������һ�������¾�������ͼ��ʾ��ת����ϵ�������жϴ������

A. ��ͼ�з�Ӧ��Ϊ��������ԭ��Ӧ����WΪһԪǿ��ʱ����Z������NaAlO2
B. ��ͼ�з�Ӧ��Ϊ������ԭ��Ӧ����WΪ�ǽ�������ʱ����Z������CO2
C. ��ͼ�з�Ӧ��Ϊ��������ԭ��Ӧ����WΪһԪǿ��ʱ��X������NH3
D. ��ͼ�з�Ӧ��Ϊ������ԭ��Ӧ����WΪ��������ʱ����Z������FeCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��E����ѧ������5�ֻ����A��B�����������֮���ת����ϵ����ͼ��ʾ��������˵����ȷ���ǣ� ��

A. X��A��Ӧ�Ļ�ѧ����ʽ�ǣ�Al2O3 + 2Fe ![]() Fe2O3 + 2Al
Fe2O3 + 2Al
B. ����D��Һ�еĽ��������ӵķ�Ӧ��Fe3++3SCN��= Fe(SCN)3��
C. ����Y��һ������������ˮ�����û���Ӧ
D. ���ڻ�����B��C���������ᷴӦ��������Ӧ�����Ծ������Ի�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na2FeO4��Һ������ˮ�еĻ�ԭ����Ⱦ��M��Ϊ�о�����Ч����������¶Ա�ʵ��̽���¶ȡ�Ũ�ȡ� pH�������Խ������ʺ�Ч����Ӱ�죬ʵ����M��Ũ����ʱ���ϵ��ͼ��ʾ������˵������ȷ���ǣ�������

ʵ���� | �¶ȡ� | pH |
�� | 25 | 1 |
�� | 45 | 1 |
�� | 25 | 7 |
�� | 25 | 1 |
A.ʵ�����15 min��M�Ľ�������Ϊ1.33��10��5mol/��L��min��
B.������������ͬ��ʵ��٢�˵�������¶ȣ�M������������
C.������������ͬ��ʵ��٢�֤��pHԽ�ߣ�Խ������M�Ľ���
D.ʵ���˵��M��Ũ��ԽС�����������Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�п��ܴ��ڵ���ƽ�⡢�ε�ˮ��ƽ��ͳ������ܽ�ƽ�⣬���Ƕ��ɿ�����ѧƽ�⡣�������ѧ��֪ʶ�ش�
��1��AΪ0.1mol��L-1��(NH4)2SO4��Һ���ڸ���Һ�и������ӵ�Ũ���ɴ�С˳��Ϊ__��
��2��BΪ0.1mol��L-1NaHCO3��Һ�������NaHCO3��Һ�Լ��Ե�ԭ��__��
��3��CΪFeCl3��Һ��ʵ����������FeCl3��Һʱ������__��������ˮ�⣬����B��C��Һ��ϣ����������ɫ��������ɫ���壬�÷�Ӧ�����ӷ���ʽΪ_��
��4��DΪ��������AgCl����ı�����Һ��AgCl��ˮ�д��ڳ����ܽ�ƽ�⣺AgCl(s)![]() Ag+(aq)+Cl-(aq)����25��ʱ��Ksp(AgCl)=1.8��10-10���ֽ������Ȼ����ֱ���룺
Ag+(aq)+Cl-(aq)����25��ʱ��Ksp(AgCl)=1.8��10-10���ֽ������Ȼ����ֱ���룺
��100mL����ˮ�У���100mL0.2mol��L-1AgNO3��Һ�У���100mL0.1mol��L-1�Ȼ�����Һ�У���100mL0.1mol��L-1�����У���ֽ������ͬ�¶���c(Ag+)�ɴ�С��˳����__(�����)������м��������Ȼ����������ӵ�Ũ��Ϊ__mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NO��O2��Na2CO3��Һ��Ӧ�Ʊ�NaNO2��װ����ͼ��ʾ�����й��ڸ�װ�õ���������ȷ���ǣ� ��
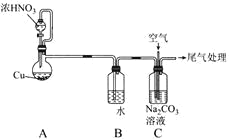
A.װ��A��Һ©���е�ҩƷѡ�ò�����Ӧѡ��ϡHNO3
B.ʵ������У�ͨ�����Ʒ�Һ©���Ļ������������ٶ�
C.װ��C�з�����Ӧ�Ļ�ѧ����ʽΪ2Na2CO3+4NO+O2=4NaNO2+2CO2��
D.ʵ������У�װ��CҺ���Ϸ����ܳ��ֺ���ɫ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com