
【题目】中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物。该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金”。下列有关说法中,你认为错误的是
A. 该反应可能在空气中进行B. 另一种化合物是NaCl
C. Na的还原性强于金刚石D. 这个反应是置换反应
科目:高中化学 来源: 题型:
【题目】燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是( )。
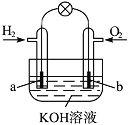
A.氢氧燃料电池是一种具有应用前景的绿色电源
B.a极是负极,该电极上发生氧化反应
C.总反应方程式为2H2+O2=2H2O
D.b极反应是O2+4OH--4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为苯的硝化反应实验装置:
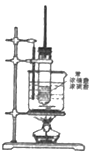
(1)写出该反应方程式__________________________,反应类型为_____________________。
(2)反应中采用的加热方式为________________,控制温度为_______________,试管上方长导管的作用是___________________________________。
(3)下列有关苯和硝基苯的叙述正确的是_______________。
a 密度都比水小 b 都不溶于水 c 互为同系物 d 都属于芳香烃
(4)有机反应主要分为取代、氧化、消去、加成、聚合五大类型。现有下列反应:
①由乙烯制氯乙烷 ②乙烷在空气中燃烧 ③乙烯使溴水褪色④乙烯通入酸性高锰酸钾溶液 ⑤由乙烯制聚乙烯 ⑥乙烷与氯气光照
其中属于取代反应的是___________________;属于氧化反应的是_____________________;
属于加成反应的是___________________;属于聚合反应的是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:
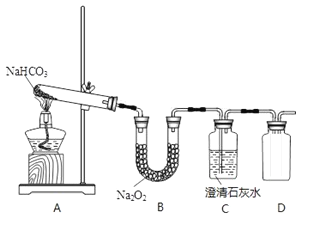
(1)写出装置A中反应的化学方程式________。
(2)写出装置B中反应的化学方程式________。
(3)拟用装置D收集气体产物,请将装置补充完整________。
(4)产物检验:检验气体产物的方法________。
(5)检验固体产物的方法:从B装置中取少量固体,溶于水配成溶液,________。
(6)有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3—环己二酮(![]() )常用作医药中间体,用于有机合成。下列是一种合成1,3—环己二酮的路线。
)常用作医药中间体,用于有机合成。下列是一种合成1,3—环己二酮的路线。

回答下列问题:
(1)甲的分子式为 __________。
(2)丙中含有官能团的名称是__________。
(3)反应①的反应类型是________;反应②的反应类型是_______。
(4)反应④的化学方程式_______。
(5)符合下列条件的乙的同分异构体共有______种。
①能发生银镜反应
②能与NaHCO3溶液反应,且1mol乙与足量NaHCO3溶液反应时产生气体22.4L(标准状况)。
写出其中在核磁共振氢谱中峰面积之比为1∶6∶2∶1的一种同分异构体的结构简式:________。(任意一种)
(6)设计以![]() (丙酮)、乙醇、乙酸为原料制备
(丙酮)、乙醇、乙酸为原料制备![]() (2,4—戊二醇)的合成路线(无机试剂任选)_______。
(2,4—戊二醇)的合成路线(无机试剂任选)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学物质丰富多彩,化学反应精彩纷呈,在生活和生产中应用广泛。
(1)盛放氢氧化钠的玻璃试剂瓶不用玻璃塞,请用化学方程式表示其中的原因:___;
(2)工业上制备粗硅的化学方程式为:___;
(3)可用氢氧化钠溶解铝土矿(主要成分Al2O3);其反应方程式为:___;
(4)铁锈(主要成分氧化铁)与稀盐酸反应___;
(5)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.CO2催化加氢制甲醇是极具前景的资源化研究领域,主要反应有:
i.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1
ii.CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
CO(g)+H2O(g) ΔH2=+41.2kJ·mol-1
iii.CO(g)+2H2(g)![]() CH3OH(g) ΔH3
CH3OH(g) ΔH3
(1)ΔH3=___kJ·mol-1。
(2)已知反应i的速率方程为v正=k正x(CO2)·x3(H2),v逆=k逆·x(CH3OH)·x(H2O),k正、k逆均为速率常数且只与温度有关,x为物质的量分数。其物质的量分数平衡常数Kx=___(以k正、k逆表示)。
(3)5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反应达平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
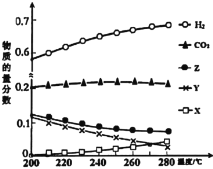
①图中Y代表___(填化学式)。
②250℃时反应ii的Kx___1(填“>”、“<”或“=”)
③下列措施中,一定无法提高甲醇产率的是___。
A.加入适量CO B.使用催化剂
C.循环利用原料气 D.升高温度
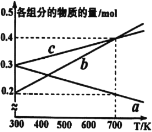
(4)在10MPa下将H2、CO按一定比例投料,平衡状态时各组分的物质的量与温度的关系如图所示。曲线b代表的物质为____(填化学式)。温度为700K时,该反应的平衡常数KP=___(MPa)-2(结果用分数表示)。
Ⅱ.在恒容容器中,使用某种催化剂对反应NO2(g)+SO2(g)![]() SO3(g)+NO(g) ΔH<0
SO3(g)+NO(g) ΔH<0
进行相关实验探究。改变投料比[n(SO2):n(NO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定SO2的平衡转化率[α(SO2)]实验结果如图所示。
已知:KR=16,KZ=![]() 。
。
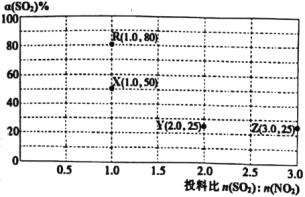
(5)如果要将图中R点的平衡状态改变为X点的平衡状态。应采取的措施是___。
(6)通过计算确定图中R、X、Y、Z四点中温度相等的点是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为反应2H2 (g)+O2(g)=2H2O(g)的能量变化示意图。下列说法正确的是( )
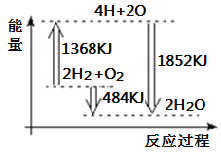
A. 由H、O原子形成2mol H2O(g),共吸收1852 kJ能量
B. 拆开2molH2 (g)和1mol O2 (g)中的化学键成为H、O原子,共放出1368kJ能量
C. 2molH2 (g)和1molO2 (g)反应生成2mol H2O(g),共放出484 kJ能量
D. 2molH2 (g)和1molO2 (g)反应生成2molH2O(l),共吸收484 kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com