
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g);△H=+QkJmol-1 (Q>0)某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
Si(s)+4HCl(g);△H=+QkJmol-1 (Q>0)某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强则化学反应速率降低
B.若反应开始时 SiCl4 为 1mol,则达到平衡时,吸收热量为 QkJ
C.反应至 4min 时,若HCl的浓度为 0.12molL-1,则 H2 的反应速率为 0.03mol/(Lmin)
D.当反应吸收热量为 0.025QkJ 时,生成的 HCl 通入 100mL1molL-1 的 NaOH 恰好反应
【答案】D
【解析】
A.有气体参加的反应,增大压强,反应速率增大,A错误;
B.由方程式可知:每1mol SiCl4完全反应,吸收热量为QkJ,但该反应是可逆反应,有限度,所以若反应开始时 SiCl4 为 1mol,则达到平衡时,所消耗SiCl4少于1mol,所吸收热量小于QkJ,B错误;
C.HCl是生成物,反应开始时浓度为0,当HCl的浓度为 0.12molL-1,HCl的物质的量浓度变化量=0.12molL-1,时间是4min,所以,v(HCl)=![]() =0.03 molL-1min-1,所以v(H2)=
=0.03 molL-1min-1,所以v(H2)=![]() =0.015 molL-1min-1,C错误;
=0.015 molL-1min-1,C错误;
D.由方程式可知:每生成4molHCl时,吸收QkJ热量,那么当反应吸收热量为 0.025QkJ 时,生成的 HCl的物质的量=0.1mol,可消耗0.1molNaOH,即通入 100mL1molL-1 的 NaOH溶液中恰好完全反应,D正确。
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用合成气制备甲醇。反应为![]() 某温度下,在容积为2L的密闭容器中进行该反应,其相关数据如图:
某温度下,在容积为2L的密闭容器中进行该反应,其相关数据如图:
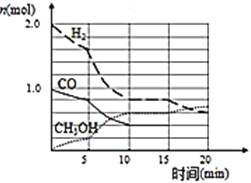
(1)从反应开始至平衡时,用CO表示化学反应速率为 ______ ,该温度下的平衡常数为 ______
(2)![]() 至10min时速率变化的原因可能是 ______ ;
至10min时速率变化的原因可能是 ______ ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D(A、B、C、D均是气体)反应中,表示该反应速率最快的是
3C+4D(A、B、C、D均是气体)反应中,表示该反应速率最快的是
A.υ(A)= 0.5 mol/(Ls)B.υ(B)= 0.3 mol/(Ls)
C.υ(C)= 0.8 mol/(Ls)D.υ(D)= 1 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.06g·L-1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
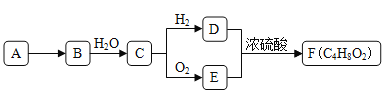
请回答:
(1)有机物D中含有的官能团名称是__________________。
(2) D+E→F的反应类型是_________________________。
(3)有机物A在高温下转化为B的化学方程式是_________________。
(4)下列说法正确的是___。
A.有机物E与金属钠反应比水与金属钠反应要剧烈
B.有机物D、E、F可用饱和Na2CO3溶液鉴别
C.实验室制备F时,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列哪种说法可以证明反应N2+3H2![]() 2NH3已达到平衡状态
2NH3已达到平衡状态
A.1个N≡N键断裂的同时,有3个H—H键形成
B.1个N≡N键断裂的同时,有3个H—H键断裂
C.1个N≡N键形成的同时,有3个N—H键形成
D.1个N≡N键形成的同时,有6个N—H键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.CH3—CH=CH2和CH2=CH2的最简式相同
B.![]() 与
与![]() 互为同系物
互为同系物
C.下列物质的沸点按由低到高顺序为:(CH3) 2CHCH3<(CH3) 4C<(CH3)2CHCH2CH3<CH3(CH2)3CH3
D.等质量的甲烷、乙醇、乙醛分别充分燃烧,所耗用氧气的量依次减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向一个容积为2 L的真空密闭容器中(事先装入催化剂)通入1 mol N2和3 mol H2,3 min后测得密闭容器内的压强是起始时的0.7倍,在此时间内v(H2)是
A. 0.1mol/(L·min) B. 0.2mol/(L·min)
C. 0.3mol/(L·min) D. 0.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由氢气和氧气反应生成1mol水蒸气放热241.8kJ,则反应2H2(g)+O2(g) ![]() 2H2O(g)的ΔH为( )
2H2O(g)的ΔH为( )
A.-483.6kJ·mol-1B.-241.8kJ·mol-1
C.-120.6kJ·mol-1D.+241.8kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某容器中加入足量的碳酸钙,发生反应CaCO3(s)![]() CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度为原来的2倍
B.增加CaCO3(s)的量,平衡正向移动
C.将体积增大为原来的2倍,再次达到平衡时,气体的密度不变
D.保持容器体积不变,充入He,平衡向逆反应方向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com