
| A、浓硝酸保存在棕色玻璃试剂瓶中 |
| B、少量的金属锂保存在煤油中 |
| C、氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 |
| D、少量液溴通常保存在棕色玻璃试剂瓶中,并在液溴上加少量水液封 |


科目:高中化学 来源: 题型:
| A、1molNa+含有质子数为10NA |
| B、标况下,2.24升CCl4物质的量为0.1mol |
| C、标准状况下,分子数为NA的CO、N2混合气体体积约为22.4L,质量为28g |
| D、5.6g金属铁与足量盐酸反应时,失去0.3NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol |
| B、0.15 mol |
| C、0.25 mol |
| D、0.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将蒸馏水沿烧杯内壁缓慢地注入浓硫酸中并不断搅拌 |
| B、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| C、配制1mol?L-1 300mL NaCl溶液可以选择一个50mL的容量瓶和一个250mL的容量瓶 |
D、可以用如图装置进行氯气的尾气处理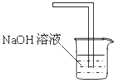 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)随温度的升高而增大 |
| B、水的电离过程是放热的 |
| C、水的电离平衡常数与浓度、温度有关 |
| D、在35℃时,c(H+)>c(OH─) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L0.1mol?L-1 Na2CO3溶液中有NA个CO32- |
| B、常温常压下,22gCO2中共有2NA个共用电子对 |
| C、0.1mol Na2O2与水完全反应,转移的电子数为0.2NA |
| D、2.8gN2、CO和C2H4组成的混合气体所占有的体积约为2.24L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2种 | B、4种 | C、6种 | D、5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com