
【题目】化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: 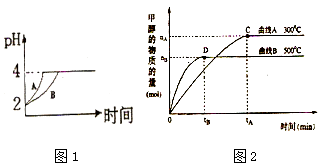
(1)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图1所示.则图中表示醋酸溶液中pH变化的曲线是 填“A”或“B”). 设盐酸中加入的Zn质量为m1 , 醋酸溶液中加入的Zn质量为 m2 . 则 m1 m2 ( 选填“<”、“=”、“>”).
(2)如图2所示,在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)CH3OH(g).升高温度,K值(填“增大”、“减小”或“不变”).在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= .
(3)某温度下Ksp=2×10 ﹣11 , 若该温度下某MgSO4溶液里c(Mg 2+)=0.002molL﹣1 , 如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于;该温度下,在0.20L的0.002mol/LMgSO4溶液中加入等体积的0.10mol/L的氨水溶液,该温度下电离常数Kb(NH3H2O)=2×10﹣5 , 试计算(填“有”或“无”) Mg(OH)2沉淀生成?
(4)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32﹣水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) .
【答案】
(1)B;<
(2)减小; ![]() mol/(L?min)
mol/(L?min)
(3)10;有
(4)取少量红色溶液中加入足量BaCl2溶液,如果溶液还显红色说明甲正确,红色褪去说明乙正确;或加热,如果红色不变说明甲正确,如果红色加深,说明乙正确
【解析】解:(1)由于醋酸是弱电解质,与Zn反应同时,电离出H+,所以pH变化较缓慢,所以B曲线是醋酸溶液的pH变化曲线.由图知盐酸和醋酸的pH变化都是由2到4,盐酸中氢离子浓度逐渐减小,但醋酸中存在电离平衡,氢离子和锌反应时促进醋酸电离,补充反应的氢离子,所以醋酸是边反应边电离H+,故消耗的Zn多,所以m1<m2.
所以答案是:B;<;(2)因化学平衡常数等于生成物的浓度系数次幂之积除以反应物的浓度系数次幂之积,所以K= ![]() ,化合反应一般为放热反应,升高温度,平衡逆向移动,K值变小,v(H2)=
,化合反应一般为放热反应,升高温度,平衡逆向移动,K值变小,v(H2)= ![]() =
= ![]() =
= ![]() mol/(Lmin),
mol/(Lmin),
所以答案是:减小; ![]() mol/(Lmin);(3)0.002molL﹣1MgSO4溶液中c(Mg2+)=0.0002mol/L,沉淀平衡时c(OH﹣)=
mol/(Lmin);(3)0.002molL﹣1MgSO4溶液中c(Mg2+)=0.0002mol/L,沉淀平衡时c(OH﹣)= ![]() =
= ![]() mol/L=10﹣4 mol/L,则c(H+)=10﹣10 mol/L,所以溶液的pH=﹣lgc(H+)=10,故应调整溶液pH大于10,在0.20L的0.002molL﹣1MgSO4溶液中加入等体积的0.10molL﹣1的氨水溶液,假设氨水的电离程度不变,则混合溶液中氢氧根离子浓度=
mol/L=10﹣4 mol/L,则c(H+)=10﹣10 mol/L,所以溶液的pH=﹣lgc(H+)=10,故应调整溶液pH大于10,在0.20L的0.002molL﹣1MgSO4溶液中加入等体积的0.10molL﹣1的氨水溶液,假设氨水的电离程度不变,则混合溶液中氢氧根离子浓度= ![]() ×10﹣3 mol/L=4.45×10﹣3 mol/L>10﹣4 mol/L,所以有沉淀生成,
×10﹣3 mol/L=4.45×10﹣3 mol/L>10﹣4 mol/L,所以有沉淀生成,
所以答案是:10;有;(4)酚酞遇碱变红色,该溶液呈红色说明是碱性溶液,要验证该溶液遇酚酞呈红色原因,可用以下方法,
方法一:向红色溶液中加入足量BaCl2溶液,如果溶液显红色,说明甲正确,如果红色褪去,说明乙正确;
方法二:加热,如果红色不变说明甲正确,如果红色加深,说明乙正确,
所以答案是:取少量红色溶液中加入足量BaCl2溶液,如果溶液还显红色说明甲正确,红色褪去说明乙正确;或加热,如果红色不变说明甲正确,如果红色加深,说明乙正确.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的短周期部分,表中字母分别表示一种元素。
请回答下列问题:
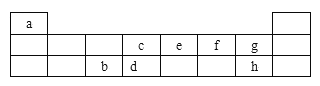
(1)上述所列元素中,最高价氧化物的水化物中酸性最强的是__________(填化学式)。
(2)d、e、f三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示) _______________________。
(3)a、c两种元素可形成多种化合物,其中化合物A的产量是衡量一个国家石油化工发展水平的标志,则:
①A的结构简式为____________;以A为原料,可制得当今世界上产量最大的塑料产品,该反应的化学方程式为____________________________________;
②A可与H2O反应生成化合物B,该反应类型为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
①3He和4He是同位素 ②金属性:K>Ca>Mg>Be
③四氯化碳的电子式:![]() ④离子键就是阴、阳离子的静电引力
④离子键就是阴、阳离子的静电引力
⑤通常活泼金属与活泼非金属元素形成离子化合物
⑥NaHSO4在熔融状态下电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:![]()
A. ①④⑥ B. ④⑤⑥ C. ③④⑥⑦ D. 全部都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3Cl2 +6NaOH→5NaCl+NaClO3 +3H2O中,被氧化和被还原的氯原子的个数比为( )
A.1︰1B.1︰2C.1︰5D.1︰6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.物质在溶解时,若达到饱和状态,则该物质不再溶解
B.晶体失去结晶水,一定是风化的结果
C.从饱和溶液中结晶析出的晶体都含有结晶水
D.某饱和溶液冷却而析出晶体后,该溶液仍为饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,可逆反应mA(g)+nB(g)pC(g)+qD(g);△H<0的平衡常数为K,下列说法正确的是( )
A.增加A的量,平衡正向移动,达到新平衡时K值增大
B.升高温度,K值增大
C.K越大,说明该反应的进行程度越大
D.该反应的K= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去MgCl2酸性溶液中的Fe3+ , 可在加热搅拌的条件下加入一种试剂过滤后,再加入适量的盐酸,这种试剂是( )
A.NH3H2O
B.NaOH
C.Na2CO3
D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要0.2molL﹣1的CuSO4溶液950mL,配制时应选用的容量瓶的规格和称取胆矾晶体(CuSO45H2O相对分子质量为250)的质量分别是( )
A. 1000mL 50.0g B. 950mL 47.5g
C. 950mL 30.4g D. 1000mL 32.0g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com