
【题目】煤化工中常需研究不同温度下平衡常数、投料比等问题。
已知:CO(g)+H2O(g)![]() H2(g)+CO2(g)平衡常数K随温度的变化如下表:
H2(g)+CO2(g)平衡常数K随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题
(1)该反应的平衡常数表达式K= ,△H 0(填“<”、“>”、“=”)
(2)已知在一定温度下,C(s)+CO2(g)![]() 2CO(g)平衡常数K1
2CO(g)平衡常数K1
C(s)+H2O(g)![]() H2(g)+CO(g)平衡常数K2,
H2(g)+CO(g)平衡常数K2,
则K、K1、K2,之间的关系是 。
(3)800℃时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时 间后反应达到平衡,此时CO的转化率为 ;若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40mol CO2,此时v正 v逆 (填“>”、“=”或“<”).
【答案】(1)K =![]() < (2)K=
< (2)K= ![]() (3) 80% =
(3) 80% =
【解析】
试题分析:(1)根据化学方程式可知,该反应的平衡常数表达式为K =![]() ;由于随着温度的升高,由于随着温度的升高,平衡常数减小,说明平衡逆向移动,因此该反应是放热反应,△H<0;
;由于随着温度的升高,由于随着温度的升高,平衡常数减小,说明平衡逆向移动,因此该反应是放热反应,△H<0;
(2)CO(g)+H2O(g)![]() H2(g)+CO2(g) K①;
H2(g)+CO2(g) K①;
C(s)+CO2(g)![]() 2CO(g) K1②;
2CO(g) K1②;
C(s)+H2O(g)![]() H2(g)+CO(g) K2③;
H2(g)+CO(g) K2③;
由于三个方程式的关系是:①=③-②,根据盖斯定律可知,K=![]() ;
;
(3)由题意可知,当温度为800℃时,CO与水蒸气反应的平衡常数K=1,据此进行计算:
CO(g)+H2O(g)![]() H2(g)+CO2(g)
H2(g)+CO2(g)
起始浓度(mol/L) 0.04 0.16 0 0
转化浓度(mol/L) x x x x
平衡浓度(mol/L) 0.04-x 0.16-x x x
K=![]() =1
=1
解得:x=0.032 mol/L,即CO转化了0.32mol,CO的转化率为:0.32/0.4=80%;
平衡时,各物质的浓度分别为:
CO(g)+H2O(g)![]() H2(g)+CO2(g)
H2(g)+CO2(g)
0.008 0.128 0.032 0.032
若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40mol CO2,通入的瞬间,各物质的浓度为:
CO(g)+H2O(g)![]() H2(g)+CO2(g)
H2(g)+CO2(g)
0.018 0.128 0.032 0.072
浓度熵Q=![]() =1=K,因此平衡不移动,故v正=v逆。
=1=K,因此平衡不移动,故v正=v逆。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】将甲烷与氯气按1:3的体积比混合于一试管中,倒立于盛有饱和食盐水的水槽,置于光亮处(如图所示),下列有关此实验的现象和结论的叙述不正确的是( )
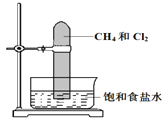
A. 试管中气体的黄绿色逐渐变浅,水面上升
B. 生成物只有三氯甲烷和氯化氢在标准状况下是气体
C. 试管内壁有油状液滴形成
D. 试管内有少量白雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年10月27日,世界工生组织国际癌症研究机构将三氯乙醛划为2A类致癌物,但它可用于生产氯霉素、合霉素等。某探究小组模拟备三氯乙醛自实验装置如图所示(夹持、加热装置均略去)。

已知:C2H5OH+4Cl2=CCl3CHO+5HCl,副反应是C2H5OH+HCl=C2H5Cl+H20。
容下列问题:
(1)写出装置A中发生反应的化学方程式:__________________。
(2)仪器b中冷凝水从________(填“p”或“q”,下同)口进,______口出。
(3)进入装置D的是纯净、干燥的Cl2,则装置B中的试剂为_____,装置C中的试剂为____。若撤去装置B,对实验的影响是____________________。
(4)实验时发现D中导管口处气泡速率过快,合理的解决方法是__________________。
(5)已知:CCl3CHO +OH-=CHCl3+HC00-; HC00-+I2=H++2I-+CO2↑ I2+2S2O32-=2I-+S4O62-
称取0.40g产品,配成待测溶液,加入20.00mL0.100mol/L碘标准溶液,再加入适量Na2C03溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020mol/L的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。滴定时所用指示剂是_______,达到滴定终点的现象是______,测得产品的纯度为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钠和氯化钠溶液等体积混合后,钠离子浓度为0.7mol·L-1, 硫酸根离子的浓度为0.2mol·L-1,则混合液中氯离子的浓度为:
A.0.15mol·L-1B.0.3mol·L-1C.0.45mol·L-1D.0.2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验的描述不正确的是( )
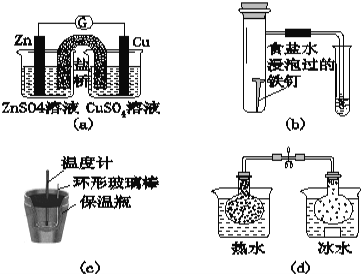
A.图(a)所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性
B.图(b)所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀
C.图(c)所示的实验:根据温度计读数的变化用稀盐酸和稀NaOH溶液反应测定中和热
D.图(d)所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g)![]() N2O4(g)是放热反应
N2O4(g)是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校的化学兴趣小组利用下列实验装置探究二氧化硫的性质,已知Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O,E中所装气体具有刺激性气味,能使湿润的红色石蕊试纸变蓝。

实验开始时关闭K2打开K1,从分液漏斗中向烧瓶内加入浓硫酸。
(1)B中的现象是________________。
(2)写出C中反应的化学方程式:_______________________________________。
(3)D的作用是___________________________________________________,
反应的离子方程式为_______________________________________________。
(4)A中反应完成后,关闭K1,打开K2,将E中的气体注入B中,观察到B中现象是________________________,
反应的离子方程式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取自来水的装置示意图,根据图示回答下列问题。
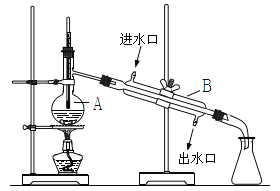
(1)图中的两处明显的错误是____________________、_____________________。
(2)A仪器的名称是______________,B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,还需加入少量___________,其作用是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种溶液可能含有下列阴离子中的一种或几种:![]() 、
、![]() 、Cl。
、Cl。
(1)当溶液中有大量H+存在时,则不可能有________存在。
(2)当溶液中有大量Ba2+存在时,溶液中不可能有________存在。
(3)当溶液中有________和________等阳离子存在时,上述所有阴离子都不可能存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
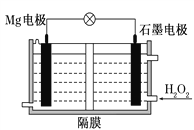
A. Mg电极是该电池的正极
B. H2O2在石墨电极上发生氧化反应
C. 石墨电极附近溶液的pH增大
D. 电子从石墨电极移向Mg电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com